Remsima SC 120 mg – nová generace biosimilárních léčiv
Milan Lukáš1
+ Pracoviště
V roce 2021 povolila Evropská léková agentura (EMA) novou formuli biosimilárního infliximabu CT-P13 určenou k podkožnímu podávání, a to ve všech indikacích původního produktu, včetně léčby ulcerózní kolitidy a Crohnovy nemoci [1]. Výsledky provedených studií jsou velmi zajímavé a otevírají nové možnosti této terapie do budoucnosti. Jaké jsou hlavní přínosy pro pacienty s idiopatickými střevními záněty (IBD)?
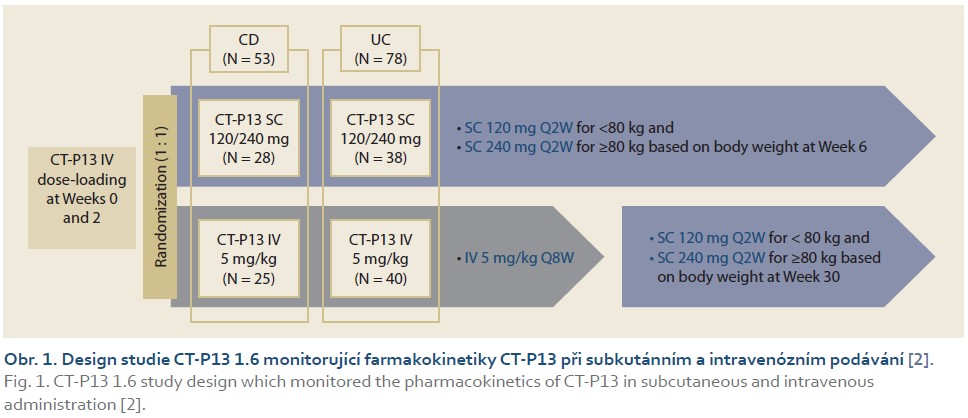
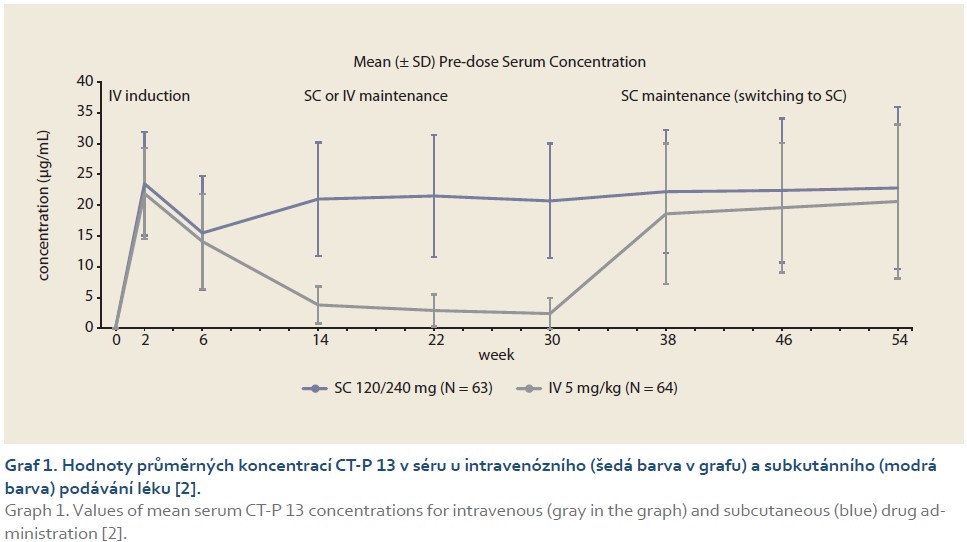
V pilotní studii CT-P13 1.6 dostali nemocní s IBD, kteří byli biologicky naivní, úvodní indukční dávku infliximabem CT-P13 intravenózně v dávce 5 mg/kg v týdnu 0 a 2. Ti nemocní, kteří vykazovali klinickou odpověď v týdnu 6, byli randomizováni do jednoho ramene, ve kterém byla další udržovací terapie vedena aplikací subkutánní formy 120 mg s.c. à 2 týdny u nemocných s tělesnou hmotností < 80 kg, nebo 240 mg s.c. à 2 týdny s tělesnou hmotností > 80 kg. Ve druhém rameni byli nemocní léčeni standardním podáváním infuzí 1× za 2 měsíce. V týdnu 30 byli pacienti na intravenózní léčbě převedeni na terapii subkutánní (obr. 1). Hlavním cílem studie bylo zjistit farmakokinetiku infliximabu CT-P13 s ohledem na koncentraci léku v séru (C-trough) a na přítomnost neutralizačních protilátek (ADA) v týdnech 30 a 52 a také farmakodynamický efekt léčby vyjádřený klinickými indexy aktivity a koncentrací biologických parametrů aktivity zánětu (CRP, fekální kalprotektin). Medián hodnoty C-trough ve skupině pacientů léčených v „klasickém“ intravenózním režimu před switchem v týdnu 30 byl 2,05 μg/ml, po provedení switche na konci sledování v týdnu 52 byla hodnota C-trough 21,10 μg/ml (graf 1). Ukázalo se, že u nemocných na subkutánním podávání léku nedochází ke kolísání hladiny infliximabu v průběhu celé léčby. Výskyt neutralizačních protilátek proti infliximabu (ADA) byl významně nižší u nemocných na subkutánní léčbě v porovnání s intravenózní aplikací léčiva (18 vs. 36 %). Významně lepší farmakokinetický profil léčiva měl také zásadní dopad na farmakodynamický efekt léčby. Po provedení switche z intravenózního na subkutánní podávání infliximabu CT-P13 došlo ke statisticky významnému snížení hodnoty klinických parametrů aktivity zánětu (CDAI a pMayo). Tento klinický „symptomový efekt“ byl také doprovázen snížením hodnoty CRP v krevním séru a hodnoty fekálního kalprotektinu ve stolici [2,3].
Změny ve farmakokinetice infliximabu CT-P13 jsou pro klinickou praxi velmi slibné. U nemocných, kteří jsou léčeni anti-TNF léky, se ukázala zřetelná závislost mezi koncentrací léčiva v těle pacienta a podílem pacientů, kteří dosáhnou klinické remise. S vyšší hodnotou C-trough narůstá počet nemocných, kteří dosahují klinické remise nejen po indukční fázi léčby, ale také v dlouhodobém výhledu. Tyto výsledky byly potvrzeny v reálné klinické praxi v britském projektu PANTS, který monitoroval výsledky léčby u více než 1 100 pacientů. Hladina anti-TNF léčiv infliximabu a také adalimumabu je významným prediktorem setrvalé klinické odpovědi. Bylo zjištěno, že v případě infliximabu by měla být hladina léčiva v udržovací fázi léčby (v týdnu 30) > 5 μg/ml a v případě adalimumabu > 12 μg/ml [4]. To bohužel není u většiny nemocných léčených standardně intravenózním podáváním dosaženo a je to také jeden z hlavních důvodů omezené efektivity této léčby. Primární selhání terapie, tj. nedosažení významné klinické odpovědi nebo remise, je po indukční fázi léčby zaznamenáváno u > 30 % nemocných s ulcerózní kolitidou nebo Crohnovou nemocí. Druhotná ztráta odpovědi se vysvětluje akcelerovanou clearancí léčiva, které je komplexně odbouráváno a z větší části degradováno v retikuloendotelovém systému pacienta. Komplexní, a především velmi individuální clearance terapeutických monoklonálních protilátek se navíc v čase mění, a to u každého konkrétního pacienta. Nedostatek léčiva v těle je pak hlavní příčinou ztráty odpovědi na podávanou terapii. Vedle zvýšené clearance se na akcelerovaném metabolizmu anti-TNF léčiv podílí také imunitní faktory s tvorbou protilátek (ADA – anti-drugs antibodies), které inaktivují protizánětlivý biologický efekt podávané terapie. Kolísání hladiny infliximabu při intravenózním podávání je příčinou silné imunogenicity infliximabu, nikoli komponenta myších sekvencí aminokyselin v chimérické makromolekule, jak jsme se dříve domnívali. Významné snížení tvorby protilátek proti infliximabu CT-P13 podávaného subkutánně, a to až na úroveň, kterou vykazují nové inovativní molekuly, jako jsou vadolizumab a ustekinumab, je toho dokladem. V této pilotní studii se ukázal také logicky důsledek lepšího farmakodynamického efektu subkutánního podávání infliximabu ze strany pacientů, kteří vykazovali zvýšení hodnoty kvality života, indexem HRoQL. Je zřejmé, že trend podávání terapeutických monoklonálních protilátek je jednoznačně namířen na subkutánní aplikaci, a to s ohledem na vyšší komfort nemocných. Zvláště v době pandemie SARS-Cov-2 je možnost aplikace léčiva v domácích podmínkách a minimalizace nezbytných návštěv u lékaře velmi zásadní i pro pacienta. Takovou léčbu je možné využít u stabilizovaných nemocných s IBD pomocí dálkového monitorování. V seznamu hrazených zdravotních výkonů pro rok 2022 je dostupný specifický kód pro dálkové sledování IBD pacientů (kód 15150), který může poskytovatel nasmlouvat s plátcem zdravotní péče. Toto sledování zahrnuje validované dotazníky a náklady na provedení CalproSmart testu.
Jak v reálné praxi nový lék, který je pro svůj vylepšený farmakokinetický profil také někdy označován termínem bio-better, podávat? Po úvodních infuzích v týdnu 0 a 2 se přechází na aplikaci subkutánní ve standardní dávce 120 mg 1× za 2 týdny. V případě nutnosti intenzifikace je nutné, podobně jako v případě subkutánního vedolizumabu, přejít na podávání intravenózní. Není potřeba zahajovat současně imunosupresivní léčbu azathioprinem nebo metotrexátem, čímž se významně zvyšuje bezpečnost léčby preparátem Remsima SC 120 mg.
ORCID autora
M. Lukáš ORCID 0000-0002-1463-3840
prof. MUDr. Milan Lukáš, CSc., AGAF
Klinické a výzkumné centrum pro střevní záněty
Klinické centrum ISCARE a. s. a 1. LF UK v Praze
Českomoravská 19
190 00 Praha 9
milan.lukas@email.cz
Tento článek vznikl s podporou společnosti Celltrion Healthcare CZ.
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Remsima; summary of product characteristics. 2021 [online]. Available from: https: //www.ema.europa.eu/en/documents/product-information/remsima-epar-product-information_en.pdf.
2. Schreiber S, D’Haens G, Cummings F et al. Switching from intravenous to subcutaneous infliximab in patients with active inflammatory bowel disease. Post hoc analysis of pre-post switch outcomes from multicentre, randomized, controlled pivotal trial. UEGW 2021, P0472.
3. Lukáš M. První generace biologických léčiv anti-TNF alfa monoklonální protilátky. In: Pokroky v diagnostice a léčbě idiopatických střevních zánětů. Praha: Galén 2019.
4. Kennedy NA, Heap GA, Green HD et al. Predictors of anti-TNF therapy failure in anti-TNF naive patients with active luminal Crohn’s disease. A prospective multicentre cohort study. Lancet Gastroenterol Hepatol 2019; 4(5): 341–353. doi: 10.1016/S2468-1253(19)30012-3.