Ledipasvir/sofosbuvir – rychlý vývoj poznatků vede ke zkrácení léčby u cirhotických pacientů s chronickou hepatitidou C
Petr Husa1
+ Pracoviště
Souhrn
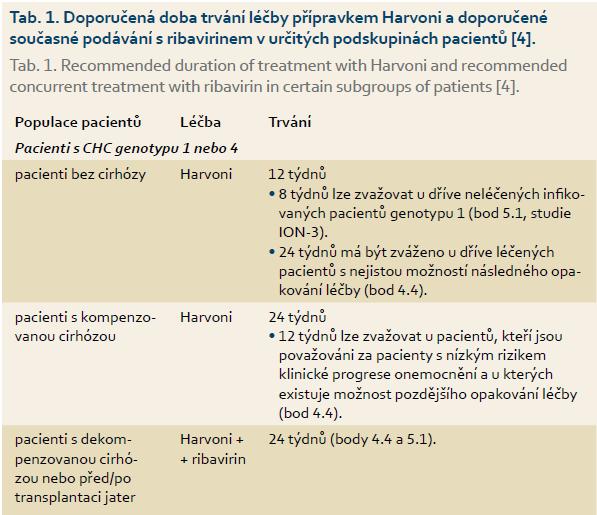
Ledipasvir a sofosbuvir ve fixní jednotabletové kombinaci má široké pole uplatnění v léčbě pacientů infikovaných genotypy 1, 3 a 4 viru hepatitidy C. Podle platných doporučení Evropské asociace pro studium jater je u cirhotiků infikovaných genotypy 1 nebo 4 viru hepatitidy C doba léčby kombinací ledipasviru/sofosbuviru a ribavirinu 12 týdnů. Toto doporučení se týká pacientů s jaterní cirhózou kompenzovanou i dekompenzovanou, před transplantací jater i po ní. Prodloužení délky kombinované léčby na 24 týdnů se týká pouze cirhotiků s negativními prediktivními faktory pro dosažení setrvalé virologické odpovědi, zejména s výraznou trombocytopenií nebo pokud je ribavirin kontraindikován či špatně tolerován. Poslední revize Souhrnu údajů o přípravku Harvoni z června 2015 doporučuje 24 týdnů léčby – u kompenzované cirhózy se má podávat samotný ledipasvir/sofosbuvir, u dekompenzované cirhózy, před transplantací jater a po ní ledipasvir/sofosbuvir s ribavirinem. Analýza uvedeného rozporu je obsahem tohoto sdělení.
Klíčová slova
HCV, chronická hepatitida C, ledipasvir, ribavirin, sofosbuvir, virus hepatitidy CÚvod
Léčba chronické hepatitidy C prodělává v posledních pěti letech zcela mimořádné změny. Do praxe se postupně zavádějí přímo působící antivirotika (DAA – direct-acting antivirals), která se podávají buď v kombinaci s pegylovaným interferonem a ribavirinem, nebo v tzv. interferon-free režimech, nebo dokonce v ribavirin-free režimech. Výrazné změny v možnostech léčby chronické hepatitidy C vedly k rychlým inovacím doporučených postupů. Evropská asociace pro studium jater (EASL – European Association for the Study of the Liver) vydala doporučení léčby hepatitidy C v dubnu 2014 [1] a během jednoho roku došlo k takovému vývoji léčebných možností, že v rámci 50. výročního zasedání EASL ve Vídni v dubnu 2015 byla představena doporučení nová [2]. Americká asociace pro studium jater (AASLD – American Association for the Study of Liver Diseases) dokonce přestala svá doporučení vydávat v tištěné formě a zpřístupnila je pouze online na webových stránkách, kde jsou plynule doplňována o výsledky nových klinických hodnocení. Při každém stažení tohoto doporučeného postupu se k textu automaticky přiřadí datum, ve kterém daná verze platila a byla uživatelem získána [3]. Tento rychlý příliv informací vede k tomu, že poznatky obsažené v Souhrnech údajů o přípravku (SPC) se v řadě aspektů liší od doporučených postupů renomovaných hepatologických společností, které reagují na výsledky klinických studií pružněji než SPC. Toto platí i pro fixní kombinaci ledipasviru (LDV) a sofosbuviru (SOF). Disproporce se v současnosti týkají léčby pacientů s jaterní cirhózou, a to kompenzovanou i dekompenzovanou, a léčby pacientů před transplantací jater a po ní. Ve všech uvedených případech se jedná o pacienty infikované genotypem 1 nebo 4 viru hepatitidy C (HCV).
Sofosbuvir a ledipasvir
SOF je nukleotidový inhibitor NS5B polymerázy HCV, který in vitro vykazuje aktivitu vůči všem genotypům HCV. LDV působí jako inhibitor komplexu NS5A. Blokuje dvě fáze virového replikačního cyklu, a sice syntézu RNA, ale také kompletaci virionu a pravděpodobně i proces jeho uvolnění z hepatocytu. LDV a SOF má ve fixní jednotabletové kombinaci široké pole uplatnění v léčbě pacientů infikovaných genotypy HCV 1, 3 a 4. Kombinovaná tableta obsahuje 400 mg SOF a 90 mg LDV.
Léčba kompenzované jaterní cirhózy
Podle poslední revize textu SPC Harvoni z června 2015 je základní délka léčby pacientů infikovaných genotypy HCV 1 nebo 4, s kompenzovanou cirhózou (Child-Pugh A), podávání LDV/SOF po dobu 24 týdnů, a to bez ribavirinu. O 12 týdnech léčby lze uvažovat u pacientů, kteří jsou považováni za nemocné s nízkým rizikem klinické progrese onemocnění a u kterých existuje možnost pozdějšího opakování léčby (tab. 1) [4].
Kritériem úspěšnosti eradikace HCV je obecně při léčbě přímo působícími antivirotiky nedetekovatelná HCV RNA (≤ 15 IU/ml) 12 týdnů po ukončení léčby – setrvalá virologická odpověď (SVR – sustained virologic response) 12. Doporučený postup EASL z dubna 2015 cituje v části věnované léčbě fixní kombinací SOF a LDV výsledky integrované analýzy 513 pacientů infikovaných genotypem HCV 1 s kompenzovanou jaterní cirhózou léčených v různých studiích fází II a III s ribavirinem/bez ribavirinu. Setrvalé virologické odpovědi 12 bylo dosaženo po 12 týdnech léčby u 305 z 322 léčených osob (95 %), po 24 týdnech léčby byl úspěch zaznamenán u 188 ze 191 pacientů (98 %). Na úspěšnost léčby dosud neléčených pacientů (naivních) neměla vliv ani délka léčby ani přidání či nepřidání ribavirinu – SVR 12 mezi 96 a 100 %. Naopak u pacientů již v minulosti antivirově léčených byly patrné rozdíly v úspěšnosti léčby v závislosti na její délce a podání ribavirinu – SVR 12 dosaženo po 12 týdnech terapie LDV/SOF u 90 % léčených, po 12 týdnech kombinace LDV/SOF a ribavirin u 96 %, po 24 týdnech léčby LDV/SOF u 98 % a po 24 týdnech kombinace LDV/SOF s ribavirinem u všech léčených. Počet destiček < 75 × 109/l byl spojen s nižší pravděpodobností dosažení SVR 12 u již léčených pacientů [5].
Ve studii SIRIUS bylo dosaženo SVR 12 u 74 ze 77 pacientů (96 %) léčených 12 týdnů kombinací LDV/SOF a ribavirinu a u 75 ze 77 osob (97 %) léčených 24 týdnů pouze LDV/SOF. Jednalo se v obou případech o pacienty s kompenzovanou jaterní cirhózou, u kterých selhala předchozí léčba pegylovaným interferonem, ribavirinem a proteázovým inhibitorem 1. generace – boceprevirem nebo telaprevirem [6].
Na základě výsledků studie SIRIUS a výše uvedené integrované analýzy více než 500 pacientů s kompenzovanou jaterní cirhózou mají být podle doporučení EASL z dubna 2015 pacienti infikovaní genotypy HCV 1 nebo 4 léčeni následovně:
Pacienti s kompenzovanou cirhózou, naivní nebo v minulosti neúspěšně léčení mají dostat kombinaci LDV/SOF a ribavirinu po dobu 12 týdnů.
Pacienti s kompenzovanou cirhózou, s kontraindikacemi podávání ribavirinu nebo s jeho špatnou tolerancí mají být léčeni pouze LDV/SOF po dobu 24 týdnů.
Pacienti s kompenzovanou cirhózou a negativními prediktivními faktory dosažení SVR (počet destiček < 75 × 109/l) jsou indikováni pro prodlouženou léčbu (24 týdnů) kombinací LDV/SOF a ribavirinu [2].
Tedy základním způsobem léčby je u pacientů s kompenzovanou jaterní cirhózou infikovaných genotypy HCV 1 nebo 4 po dobu 12 týdnů kombinace LDV/SOF a ribavirinu. Tato kombinovaná léčba se prodlužuje na 24 týdnů v případě přítomnosti negativních prediktivních faktorů pro dosažení SVR 12, zejména při výrazné trombocytopenii. Podávání LDV/SOF po dobu 24 týdnů, které je uvedeno v SPC, je doporučeno jen pro pacienty s kontraindikacemi podávání ribavirinu nebo s jeho špatnou snášenlivostí.
Léčba dekompenzované jaterní cirhózy nebo pacientů před transplantací jater a po ní
Pacienti infikovaní genotypy HCV 1 nebo 4 s dekompenzovanou jaterní cirhózou nebo před transplantací jater či po ní mají být léčeni kombinací LDV/SOF a ribavirinu po dobu 24 týdnů (SPC Harvoni z června 2015).
Doporučený postup EASL 2015 zmiňuje v této souvislosti předběžné výsledky prospektivní americké multicentrické studie, ve které se hodnotila účinnost kombinace LDV/SOF a ribavirinu podávaná 12 nebo 24 týdnů pacientům s jaterní cirhózou kompenzovanou (Child-Pugh A) nebo dekompenzovanou (Child-Pugh B nebo C, do 12 bodů). U pacientů ve stadiu Child-Pugh B a C bylo dosaženo SVR 12 u 50 z 57 pacientů (88 %), resp. 37 z 42 pacientů (88 %). V obou případech rovněž bez závislosti na délce léčby. V týdnu 4 po skončení léčby došlo ke snížení hodnoty skóre MELD, kterým se hodnotí naléhavost provedení transplantace jater, o 1–8 bodů u 64 % pacientů ve stadiu Child-Pugh B a u 70 % nemocných ve stadiu Child- -Pugh C. Zhruba u 2/3 léčených se zlepšilo skóre Child-Pugh o 1–3 body. Bezpečnostní profil LDV/SOF byl dobrý a většina hlášených závažných nežádoucích účinků nebyla v příčinné souvislosti s touto léčbou [2,7]. Studie nebyla specificky designována pro pacienty čekající na transplantaci jater, ale její výsledky podporují použití LDV/SOF a ribavirinu u pacientů s kompenzovanou a dekompenzovanou jaterní cirhózou na čekací listině před transplantací jater.
Předběžná data z dosud probíhající americké multicentrické studie neprokázala významný rozdíl v účinnosti 12 nebo 24 týdnů léčby kombinací LDV/SOF a ribavirinu u nemocných po transplantaci jater. Do studie byli zahrnuti pacienti infikovaní genotypy HCV 1 nebo 4 dosud neléčení nebo již dříve léčení po transplantaci jater se všemi vývojovými stupni jaterní fibrózy dle klasifikace METAVIR (F0–F4). Setrvalé virologické odpovědi 12 bylo dosaženo u 108 ze 111 (97 %) pacientů bez cirhózy (F0–F3), 49 z 51 (96 %) nemocných s cirhózou ve stadiu Child-Pugh A, 37 ze 44 (84 %) osob s cirhózou ve stadiu Child-Pugh B a zatím 5 z 8 (62 %) ve stadiu Child-Pugh C. Bezpečností profil byl u pacientů po transplantaci jater excelentní a u většiny pacientů s jaterní cirhózou ve stadiu Child-Pugh A nebo B došlo ke zlepšení MELD skóre (hodnoceno čtyři týdny po skončení léčby) [8]. K analogickým výsledkům dospěla i studie SOLAR-2 prezentovaná na EASL 2015, ve které převažovali evropští pacienti. Ani v této studii nebyl prokázán rozdíl v dosažení SVR 12 při léčbě LDV/SOF s ribavirinem trvající 12 nebo 24 týdnů. Dosažení virologické odpovědi bylo provázeno zlepšením MELD a Child-Pugh skóre [9].
Doporučení EASL z dubna 2015 je pro pacienty infikované genotypy HCV 1 a 4 s dekompenzovanou jaterní cirhózou čekající na transplantaci jater a pro nemocné s chronickou infekcí HCV po transplantaci jater následující:
Pacienti s dekompenzovanou jaterní cirhózou (Child-Pugh B nebo C) čekající na transplantaci jater mohou být léčeni kombinací LDV/SOF a ribavirinu po dobu 12 týdnů.
Pacienti po transplantaci jater, bez cirhózy, s jaterní cirhózou kompenzovanou (Child-Pugh A) nebo dekompenzovanou (Child-Pugh B nebo C) mohou být léčeni kombinací LDV/SOF a ribavirinu po dobu 12 týdnů. Při této léčbě není nutná úprava dávky takrolimu nebo cyklosporinu.
I u těchto pacientů lze tedy nalézt rozpor mezi doporučenou dobou délky kombinací LDV/SOV a ribavirinu uvedenou v SPC (24 týdnů) a v posledních doporučeních EASL z roku 2015 (12 týdnů).
Závěr
Podle platných doporučení EASL 2015 je u cirhotiků infikovaných genotypy HCV 1 nebo 4 doba léčby kombinací LDV/SOF a ribavirinu 12 týdnů. Toto doporučení se týká pacientů s jaterní cirhózou kompenzovanou i dekompenzovanou, před transplantací jater i po ní. Prodloužení délky kombinované léčby na 24 týdnů se týká pouze cirhotiků s negativními prediktivními faktory pro dosažení setrvalé virologické odpovědi, zejména s výraznou trombocytopenií nebo pokud je ribavirin kontraindikován či špatně tolerován. Poslední revize textu SPC Harvoni z června 2015 doporučuje 24 týdnů léčby – u kompenzované cirhózy se má podávat samotná fixní kombinace LDV/SOF, u dekompenzované cirhózy, před transplantací jater a po ní LDV/SOF s ribavirinem. Vzhledem k vyšším ekonomickým nákladům na léčbu LDV/SOF představuje zkrácení léčby na 12 týdnů oproti 24 týdnům výraznou úsporu.
Publikace je podpořena firmou Gilead Sciences, s. r. o.
Autor deklaruje, že v souvislosti s předmětem studie nemá žádné komerční zájmy.
The author declares he has no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Doručeno/Submitted: 14. 8. 2015
Přijato/Accepted: 7. 9. 2015
prof. MUDr. Petr Husa, CSc.
Klinika infekčních chorob LF MU a FN Brno
Jihlavská 20
625 00 Brno
phusa@fnbrno.cz
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. European Association for Study of Liver. EASL recommendations on treatment of hepatitis C 2014. J Hepatol 2014; 61 (2): 373–395. doi: 10.1016/j.jhep.2014.05.001.
2. European Association for Study of Liver. EASL recommendations on treatment of hepatitis C 2015. J Hepatol 2015; 63 (1): 199–236. doi: 10.1016/j.jhep.2015.03.025.
3. American Association for the Study of Liver Disease. HCV Guidance: Recommendations for testing, managing, and treating hepatitis C. Available from: www.hcvguidelines.org.
4. Souhrnu údajů o přípravku Harvoni [on- line]. Dostupné z: http: //www.ema.europa.eu/docs/cs_CZ/document_library/EPAR_ –_Product_Information/human/003850/ WC500177995.pdf.
5. Bourlière M, Sulkowski MS, Omata M et al. An integrated safety and efficacy analysis of >500 patients with compensated cirrhosis treated with ledipasvir/sofosbuvir with or without ribavirin. Hepatology 2014; 60: 239A.
6. Bourlière M, Bronowicki JP, de Ledinghen V et al. Ledipasvir-sofosbuvir with or without ribavirin to treat patients with genotype 1 infection and cirrhosis non-responsive to previous protease-inhibitor therapy: a randomised, double-blind, phase 2 trial (SIRIUS). Lancet Infect Dis 2015; 15 (4): 397–404. doi: 10.1016/S1473-3099 (15) 70050-2.
7. Flamm SL, Everson GT, Charlton M et al. Ledipasvir/sofosbuvir with ribavirin for the treatment of HCV in patients with decompensated cirrhosis: preliminary results of a prospective, multicenrter study. 65th Annual Meeting of the American Association for the Study of Liver Diseases (AASLD). Hepatology 2014; 60: 320A.
8. Reddy RK, Everson GT, Flamm SL et al. Ledipasvir/sofosbuvir with ribavirin for the treatment of HCV in patients with post-transplant recurrence: preliminary results of a prospective, multicenter study. Hepatology 2014; 60: 200A–201A.
9. Gane E, Manns MP, Forns X et al. 365 Ledipasvir/sofosbuvir with ribavirin is safe and efficacious in decompensated and post-liver transplantation patients with HCV infection: preliminary results of the prospective SOLAR2 trial. Gastroenterology 2015; 148 (4): S-978. doi: 10.1016/S0016-5085 (15) 33342-4.