Zvýšení resekability jaterních metastáz kolorektálního karcinomu etapovými výkony
Vladislav Třeška Orcid.org 1, Tomáš Skalický Orcid.org , Václav Liška Orcid.org , Stanislav Kormunda Orcid.org , Alan Sutnar Orcid.org , Jiří Ferda Orcid.org , Hynek Mírka Orcid.org
+ Pracoviště
Souhrn
Cíl studie: Zhodnocení etapových postupů pro zvýšení operability jaterních metastáz kolorektálního karcinomu (JMKRK).
Materiál a metodika: Autoři operovali 267 nemocných s JMKRK od 1/1/2000 do 31/12/2006. U 28 nemocných provedli etapový výkon, spočívající v embolizaci větve portální žíly (PVE) a v resekci jater (n = 16), v chemoterapeutickém "downstagingu" a resekci, nebo radiofrekvenční ablaci (RFA) metastáz (n = 6), v RFA metastáz, PVE a resekci jater (n = 4), v kombinaci resekce s RFA (n = 2).
Výsledky: Přežití nemocných operovaných jedno-dobou resekci bylo 87,4; 46,1 a 31,4% po 1., 3. a 5. roce. Po 1. a 3. roce přežívalo po etapovém výkonu 62,5 a 20,8 % nemocných (p < 0,15). Přežití nemocných po RFA bylo 90,3 a 13,4 % po 1. a 3. roce. Po 1. a 2. roce přežilo po etapových výkonech, kde součástí byla RFA 66,7 a 44 % nemocných (p < 0,19).
Bez recidivy nádoru v játrech po jednodobé resekci bylo 72,1; 30,1 a 16,2% nemocných po 1., 3. a 5. roce, zatímco po etapovém výkonu 50,8 a 12,7% nemocných po 1. a 2. roce (p < 0,01). Po jednodobé RFA bylo po 1. a 2. roce 38,1 a 10,3 %, po etapovém výkonu po 1. roce jen 12,5 % nemocných bez recidivy (p < 0,0001).
Závěr: Etapové výkony rozšiřují operabilitu JMKRK. Přežívání nemocných je srovnatelné s primárními výkony. Přednost mají radikální etapové výkony před výkony, jejichž součástí je RFA.
Klíčová slova: embolizace portální žíly - etapové výkony - jaterní metastázy - kolorektální karcinom - radiofrekvenční ablace.
ÚVOD
Resekabilita jaterních metastáz kolorektálního (JMKRK) je celosvětově stále nízká. V čase diagnostiky jaterních metastáz je jen 15-20 % postižených nemocných radikálně operovatelných. Nemocní radikálně operovaní pro JMKRK mají jednoznačně největší šanci na dlouhodobé přežití v porovnání s nemocnými, u kterých je léčebnou volbou chemoterapie, nebo jen symptomatická léčba. Medián přežití u nemocných po radikální resekci jater je 30-40 měsíců, zatímco u nemocných léčených pouze chemoterapií jen 12-20 měsíců. Nemocní léčeni jen symptomaticky se většinou nedožijí jednoho roku od stanovení diagnózy JMKRK.
Nízká resekabilita JMKRK obecně nutí ke snaze o její zvýšení pomocí technicky sofistikovaných metod s cílem maximálního prospěchu pro nemocného z hlediska prodloužení jeho kvalitního života a minimalizace recidiv nádorového procesu v játrech. Takovou možnost v současné době dávají etapové postupy využívající k eradikaci nádorového procesu v játrech kombinaci radiointervenčních, onkologických a chirurgických metod.
MATERIÁL A METODIKA
Na chirurgické klinice FN a LFUK v Plzni jsme od 1. ledna 2000 do 1. května 2007 operovali celkem 267 nemocných průměrného věku 60,7 let (20-82 let) pro JMKRK. U těchto nemocných jsme provedli celkem 28 etapových výkonů. Jednalo se o 19 mužů a 9 žen průměrného věku 63,2 roku (49-71 let).
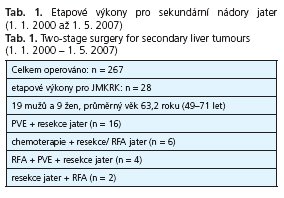
Etapové výkony u nemocných s JMKRK spočívaly v embolizaci větve portální žíly (PVE) na straně nádoru a po hypertrofii druhostranného laloku v resekci jater na straně nádoru (n =16). Další etapový postup spočíval u 4 nemocných s bilaterálním postižením JMKRK v radiofrekvenční ablaci (RFA) ložisek nádoru v jednom laloku, PVE druhého laloku a po hypertrofii laloku po RFA v resekci jater. Další etapovou metodou byla u 2 nemocných opět s bilaterálním postižením kombinace resekční léčby s RFA v jednotlivých sezeních nutných k regeneraci a hypertrofii jaterního parenchymu před dalším výkonem. U 6 nemocných jsme nejprve zvolili metodu chemoterapeutického „downstagingu" následovaného resekci a/nebo RFA (tab. 1).
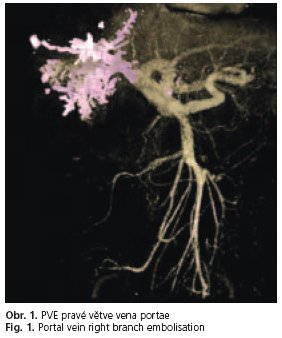
PVE jsme u většiny nemocných provedli transparietálně pomocí kovových spirál, lipiodolu, tkáňového lepidla nebo fibrinové pěny (obr. 1). Časový interval od provedení PVE a dalšího výkonu se pohyboval mezi 4-6 týdny v závislosti na rozvoji hypertrofie druhostranného jaterního laloku.
Před každou resekční léčbou v rámci etapového postupu jsme vyšetřili funkci jaterního parenchymu pomocí testu retence indocyaninové zeleně v plazmě po 15 minutách od jejího bolusového intravenózního podání (ICGR-15). Nemocný byl dále zhodnocen klinicky dle jeho celkového stavu, kardiopulmonální kompenzace a stavu jaterních funkcí na základě Child-Pugh klasifikace. U nemocných jsme v rámci etapového postupu provedli minimálně dva a maximálně čtyři výkony.
Nemocní byli v průběhu etapového postupu sledováni jak chirurgem, tak onkologem a po konečném výkonu na játrech s kompletní eradikací metastatického procesu byli dispenzarizováni v jaterní poradně onkologického centra FN v Plzni. Výsledky léčby jsme hodnotili pomocí statistické analýzy s užitím software CRAN 2.4.0. Pro měřené parametry v celém souboru a v jednotlivých skupinách a podskupinách byly počítány základní statistické údaje jako průměr, směrodatná odchylka, rozptyl, medián, mezikvartilové rozpětí, minimum, maximum a vybrané kvantily. U kategorických proměnných byly počítány jejich frekvence. Interval od poslední operace do recidivy nádoru („disease free interval" - DFI) a přežití nemocných („overall survival" - OS) jsme hodnotili pomocí Kaplan-Maierové metody.
VÝSLEDKY
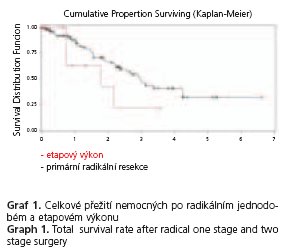
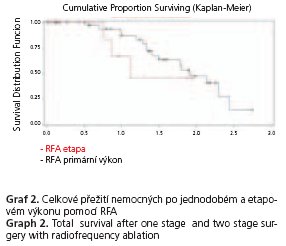
OS nemocných operovaných radikální jednorázovou resekcí pro JMKRK bylo 87,4; 46,1 a 31,4 % po 1., 3. a 5. roce. Po 1. a 3. roce bylo přežití nemocných po etapovém výkonu 62,5 a 20,8 % (p < 0,15) (graf 1). OS nemocných, u kterých byla provedena RFA jako jediný výkon, bylo 90,3 a 13,4 % po 1. a 3. roce. Po 1. a 2. roce bylo OS u etapových výkonů, kde součástí byla RFA 66,7 a 44 % (p < 0,19) (graf 2).
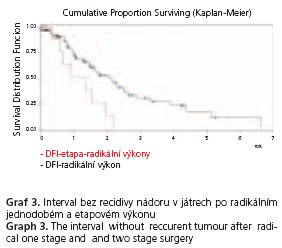
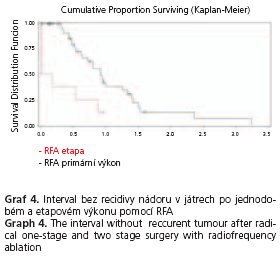
DFI nemocných po radikálním jednorázovém výkonu bylo 72,1; 30,1 a 16,2 % po 1., 3. a 5. roce. DFI po radikálním etapovém výkonu bylo 50,8 a 12,7 % po 1. a 2. roce (p < 0,01) (graf 3). DFI po RFA jako jediném výkonu bylo po 1. a 2. roce 38,1 a 10,3 %, zatímco po etapovém výkonu po 1. roce 12,5 % (ostatní roky vzhledem k malému počtu zařazených nemocných nelze hodnotit) (p < 0,0001) (graf 4).
DISKUZE
Česká republika bohužel zaujímá ve světě čelní místo ve výskytu kolorektálního karcinomu (KRK), když ročně u nás nově onemocní touto chorobou kolem 7000 osob a více než 4000 jich ročně umírá. U 50-60 % nemocných s KRK se v různém časovém intervalu od primární operace tlustého střeva nebo konečníku vyvinou JMKRK Metodou léčebné volby je chirurgická resekce, jejíž dlouhodobé výsledky jsou v porovnání s čistě onkologickou nebo jen symptomatickou léčbou jednoznačně nejlepší(1,2).
Bohužel v době diagnózy JMKRK je jen 15-20 % nemocných operovatelných bud radikální resekcí jater, nebo miniinvazivními technikami, které volíme jen tam, kde nelze využít radikální resekční léčby. K těmto technikám patří RFA, kryoablace, laserová nebo mikrovlnná koagulace. Jejich dlouhodobý efekt z hlediska recidivy maligního onemocnění - DFI je výrazněji horší v porovnání s chirurgickou resekcí.
Vzhledem k nízké resekabilitě jaterních metastáz se v poslední době hledají možnosti, jak tuto resekabilitu zvýšit a významnou měrou prodloužit kvalitní život nemocných. Takovou možností se jeví tzv. etapové výkony na játrech(3-5). Jedná se o výkony, které nelze provést v jedné době, jsou rozloženy do určitého časového intervalu a slouží k úplné eradikaci metastáz v játrech. Podmínkou pro jejich provedení je vedle lokalizace a velikosti metastáz v játrech především funkce jaterního parenchymu a celkově příznivý stav nemocného především z hlediska jeho opakované operační zátěže. Kontraindikací je mimojaterní lokalizace nádoru, kterou nelze chirurgicky radikálně odstranit. Vždy při plánování etapového výkonu je třeba mít na paměti dlouhodobý profit nemocného, který je kompenzací jeho operační zátěže při opakovaných výkonech na játrech.
Mezi faktory, které brání radikální operaci JMKRK, patří především nedostatek zdravé jaterní tkáně po resekci nádoru, která umožňuje nemocnému krytí metabolických potřeb v pooperačním období. Je známo, že tam, kde jaterní tkáň je zdravá, bez funkčního postižení, je možné resekovat až 75 % jaterního parenchymu. Zbylých 25 % pak v pooperačním průběhu nahradí jaterní funkce. Do původní velikosti regenerují játra za cca 4-6 týdnů. Samozřejmě u jater postižených steatózou, fibrózou a cirhózou, je nutné ponechat podstatně více jaterní tkáně (70-80 %), která je schopná pokrýt metabolické požadavky organizmu po resekci(6-8). Velmi důležité je posouzení funkce jaterního parenchymu zejména před rozšířeným výkonem na játrech u jinak zdravých jater, nebo u všech výkonů na játrech postižených chronickým porcesem (steatofibróza, cirhóza). K hodnocení používáme klasickou Child-Pughovu klasifikaci A, B, C. Absolutní kontraindikací jaterní resekce je klasifikace C. Klasifikace B pak limituje jaterní resekci v rozsahu maximálně 2 segmentů. U klasifikace A ověřujeme ještě (zejména u rozšířených jaterních resekcí) metabolickou funkci jater pomocí ICGR-15 testu. Tak například pravostranná hepatektomie je dobře tolerována u ICGR-15 < 10 %. Pokud je ICGR-15 v rozmezí 10-19 %, můžeme provést resekci 1/3 jater (levostranná hepatektomie). U ICGR-15 mezi 20-29 % je možné odstranit 1/4 jater (jeden - dva segmenty) (9-11).
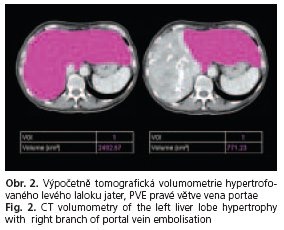
Možným řešením výše uvedeného problému je zvýšení objemu jaterní tkáně předoperační PVE pomocí kovových spirál, lipiodolu, tkáňovým lepidlem nebo fibrinovou pěnou. PVE způsobuje ischemizaci vyživované oblasti jater portální krví a kompenzatorní zvýšení toku portální krve do druhostranného řečiště s následnou parakrinní a endokrinní reakcí - zvýšením koncentrace růstových faktorů, které vedou k postupné druhostranné hypertrofii jaterní tkáně s volným portálním řečištěm. Z řady prací je však známé, že tyto růstové faktory stimulují růst nádorových buněk, a proto by tzv. zdravá jaterní tkáň neměla být postižena nádorovým procesem v době kontralaterální PVE. Samozřejmě rizikem je eventuální přítomnost mikrometastáz, které nejsou detekovatelné žádnou z dostupných radiodiagnostických metod (ultrasonografie, výpočetní tomografie, magnetická rezonance či pozitronová emisní tomografie). K hypertrofii jaterní tkáně dochází zpravidla v intervalu 4-6 týdnů po PVE(12). Zvětšení objemu jaterní tkáně pak hodnotíme pomocí výpočetně tomografické volumometrie (obr. 2). Obecně se udává, že kontralaterální jaterní tkáň zvyšuje po PVE průměrně svůj objem o 10 %(13). U metastáz postihujících oba laloky jater je metodou volby jejich resekce nebo RFA, mikrovlnná ablace, kryoablace na kontralatelární straně jater ještě před PVE a poté následná hepatektomie (v odstupu 4-6 týdnů od ablace a PVE) embolizovaného laloku jater s rozsáhlým nádorovým postižením(14). Možným, i když ne zcela ověřeným postupem u bilobárního metastatického postižení jater je PVE jedné větve portální žíly s hypertrofii druhé strany jater, ve které jsou rovněž přítomné metastázy Zde je však z hlediska nebezpečí rychlého růstu a šíření metastatického procesu v hypertrofované oblasti nutné provést hepatektomii do 4 týdnů od PVE.
Další variantou řešení je neoadjuvantní systémová nebo lokoregionální chemoterapie před vlastní resekcí nádoru jater, jejímž cílem je redukce objemu nádorové masy (tzv. „down-staging") a z technického hlediska umožnění resekability původně inoperabilního nádoru jater. Bismu»h(15) uvedl, že 15 % nemocných s primárně neresekabilními metastázami jater bylo možné po neoadjuvantní chemoterapii radikálně operovat s pětiletým přežitím dosahujícího 40 %. Problémem neoadjuvantní chemoterapie však zůstává, že způsobuje steatózu jater, snižuje regeneraci jaterní tkáně, a tak zvyšuje pooperační morbiditu nemocných.
První linií neoadjuvantní chemoterapie je kombinace 5-fiuorouracilu s jinými chemoterapeutiky (irinotecan, oxaliplatina, leucovorin), tzv. režimy FOLFIRI, FOLFOX. Léčebná odpověď se u těchto chemoterapeutických režimů pohybuje kolem 55 %(16, 17) u nemocných, kteří reagují redukcí nádorové masy na neoadjuvantní chemoterapii, je nutné provést radikální operační výkon včas bez zbytečné prodlevy. Problémem pro operujícího chirurga je větší křehkost a krvácivost jaterní tkáně po chemoterapii a nižší regenerační rezerva jater(18).
K nadějným, i když ekonomicky velmi nákladným preparátům, z hlediska „downstagingu" patří tzv. biologické látky(19). Jedná se o monoklonální protilátku proti „vascular endothelial growth faktoru" - bevacizumab (Avastin) a protilátku proti epidermálnímu růstovému faktoru - cetuximab (Erbitux). Tyto biologické preparáty obecně prodlužují medián přežití u pokročilých KRK o více než 20 měsíců a lze proto doufat, že i v rámci „downstagingu" JMKRK budou mít kvalitní výsledky.
Neoadjuvantní chemoterapii lze kombinovat rovněž s PVE, nebo ablačními metodami jako přípravnou fázi pro vlastní resekci jater u nemocných s mnohočetným postižením jaterní tkáně nádorovými ložisky. I zde je však nebezpeční vyšší pooperační morbidity z hlediska vývoje steatofibrózy jaterní tkáně po chemoterapii.
Další léčebnou možností u bilobárního postižení jater metastázami je postupná resekce jaterního parenchymu postiženého nádorovým procesem. Obyčejně jsou nutné dva resekční výkony na játrech, mezi kterými je zpravidla ótýdenní interval potřebný k regeneraci zdravé jaterní tkáně(20,21). Výkony lze kombinovat i s PVE nebo RFA. Opakované resekční výkony nejsou zatíženy významně vyšší morbiditou a dlouhodobé přežívání nemocných s pěti a více bilobárními metastázami je podobné jako u nemocných, u kterých byly metastázy lokalizovány v jednom laloku, nebo byly v obou lalocích v počtu menším čtyřech(22). Minagawa(23) však zjistil větší výskyt nádorových recidiv v játrech po etapovém řešení vícečetného postižení jater. Přesto bylo zřejmé, že dlouhodobé výsledky tohoto etapového postupu byly výrazně lepší (pět let přežilo 40-50 % nemocných) než tam, kde byli nemocní léčeni jen chemoterapií, kde dvouleté přežití nemocných se pohybovalo kolem 15 %.
Naše výsledky podpořily význam etapových výkonů vzhledem k přežívání nemocných. Pokud tyto výkony jsou z chirurgického hlediska radikální, pak není rozdílu v délce přežívání mezi jednodobými a etapovými výkony. Obecně nižší přežití mají nemocní po RFA (a» jako jednodobý nebo etapový výkon), kterou je nutné považovat za paliativní výkon. Otázkou zůstává poměrně vysoký počet recidiv JMKRK v játrech jak po radikálních etapových, tak etapových výkonech, jejichž součástí byla RFA. Oba typy etapových výkonů se v tomto směru statisticky významně odlišovaly od skupin nemocných, u kterých byl proveden jen jednodobý výkon. Toto zjištění vyžaduje ještě podrobnější analýzu a především zhodnocení větší skupiny nemocných.
ZÁVĚR
Etapové výkony na játrech využívají multimodálních principů léčby (radiointervenční, onkologické, chirurgické) s cílem významnou měrou rozšířit operabilitu jaterních metastáz. Naše i literární výsledky dokazují oprávněnost těchto postupů z hlediska morbidity a mortality nemocných, u nichž byla ještě v nedávné minulosti léčbou volby onkologická, nebo symptomatická léčba nabízející nemocným jen velmi krátkou životní expektaci.
Podpořeno grantem IGA MZ NG 8301-3/2005.
LITERATURA
- 1. Skalický T, Třeška V, Šnajdauf J. Chirurgie jater, 1. vydání. Praha: Maxdorf - Jessenius 2004.
- 2. Fusai G, Davidson BR. Management of colorectal liver metastases. Colorectal Disease 2003; 5: 2-23.
- 3. Jaeck D, Bachellier P, Nakano H, et al. One or two-stage hepatectomy combined with portal vein embo-lization for initially nonresectable colorectal liver metastases. AJS 2003; 185: 221-229.
- 4. Lygidakis NJ, Singh G, Bardaxoglou, E, et al. Two-stage liver surgery for advanced liver metastasis synchronous with colorectal tumor. Hepato-Gastroente-rology2004; 51: 413-417.
- 5. Khatri VP, Petrelli NJ, Belghiti J. Extending the frontiers of surgical therapy for hepatic colorectal metastases: Is there a limit? J Clin Oncol 2005; 23: 8490-8499.
- 6. Třeška V. Technika jaterních resekcí. Rozhl Chir 2003; 82: 397-402.
- 7. Vyhnánek F, Denemark L, Ducháč V, Skrabalová D. Kde je indikována resekce jater u metastáz. Rozhl chir 2003; 82: 570-576.
- 8. Ryska M. Metastázy kolorektálního karcinomu v játrech a možnosti multimodální terapie. Bull HPB 2001;9:29-33.
- 9. Bennet J, Blumgart LH. Assessment of hepatic reserve prior to hepatic resection. J Hepatobiliary Pancreat Surg2005;12: 10-15.
- 10. Lee SG, Hwang S. How I do it: assessment of hepatic functional reserve for indication of hepatic resection. J Hepatobiliary Pancreat Surg 2005; 12: 38-43.
- 11. Gazzaniga ChM, Cappato S, Belli FE, et al. Assessment of hepatic reserve for the indication of hepatic resection: how I do it. Hepatobiliary Pancreat Surg 2005; 12: 27-30.
- 12. Seymour K, Charnley RM, Rose JDG, et al. Preoperative portal vein embolisation for primary and metastatic liver tumours: volume effects, efficacy, complications and short-term outcome. HPB 2002; 4: 21-28.
- 13. Kusaka K, Imamura H, Tomiya, T, Makuuchi M. Factors affecting liver regeneration after right portal vein embolization. Hepato-Gastroenterology 2004; 51: 532-535.
- 14. Liška V, Třeška V, Mírka H, et al. Embolizace portální žíly - zvýšení resekability jater pro maligní onemocnění. Rozhl chir 2007; 86: 97-103.
- 15. Bismuth H, Adam R, Levi F. Resection of nonresectable liver metastases from colorectal cancer after neoadjuvant chemotherapy. Ann Surg 1996; 224: 509-520.
- 16. Adam R, Delvart V, Pascal G, et al. Rescue surgery for unresectable colorectal liver metastases downstaged by chemotherapy. Annals of Surgery 2004; 4: 644-658.
- 17. Vibert E, Canedo L, Adam R. Strategies to treat primary unresectable colorectal liver metastases. Seminars in Oncology 2005; 32: 33-39.
- 18. Třeška V, Skalický T, Sutnar A, et al. Nové trendy v chirurgii jater - kombinované, etapové výkony. Interní medicína pro praxi 2004; 1: 49-51.
- 19. Goldberg RM. Advances in the treatment of metastatic colorectal cancer. The Oncologist 2005; 10: 40-48.
- 20. Adam R, Laurent A, Azoulay D. Two-stage hepatectomy: a planned strategy to treat irresectable liver tumors. Ann Surg 2000; 232: 777-785.
- 21. Shimada H, Tanaka K, Masui H, et al. Results of surgical treatment for multiple bilobar hepatic metastases from colorectal cancer. Langenbeck's Archives Surgery 2004; 4: 86-94.
- 22. Minagawa M, Makuuchi M, Torzilli G, et al. Extension of the frontiers of surgical indications in the treatment of liver metastases from colorectal cancer. Long-term results. Ann Surg 2002; 231: 487-499.
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené