Zařazení režimu FOLFIRINOX do algoritmu léčby metastazujícího karcinomu slinivky břišní – první zkušenosti
Luboš Petruželka Orcid.org 1, Michal Vočka Orcid.org 1
+ Pracoviště
Souhrn
Pancreatic cancer represents ~ 2% of all cancers (6% of all deaths from cancer). The most common histological type (> 90%) are ductal adenocarcinomas. This type of cancer has a strong tendency for local invasion and distant metastases. Therapeutic results in all stages of the disease are worse than in all other solid tumors. Methods: The study involved a total of 23 patients with locally advanced and metastatic pancreatic cancer at the Oncology Clinic of the 1st Faculty of Medicine and General Teaching Hospital in Prague between January 2013 and July 2014. All patients underwent treatment with FOLFIRINOX regimen every two weeks (oxaliplatin 85 mg/m2, irinotecan180 mg/m2, leucovorine 400 mg/m2, bolus of 5-fluorouracile 400 mg/m2 and continual infusion of 5-fluorouracile 2,400 mg/m2 for 46 hours) with a good performance status (PS 0–1) in the first or second line therapy. The antitumor efficacy (number of objective responses, time to progression and overall survival) and adverse events were monitored. Results: The median time to progression was 7.5 months, with one complete remission and six partial remissions according to RECIST. The median number of administered cycles was 10 (from 1 to 17). Irinotecan was reduced in six patients because of toxicity (irinotecan administration had to be discontinued permanently in three patients), oxaliplatin was reduced in five patients (it had to be discontinued permanently in three patients). The median overall survival reached 15.1 months from the diagnosis of inoperable locally advanced or generalized tumor. Conclusion: In patients with advanced pancreatic cancer with a good performance status (0–1) FOLFIRINOX may significantly increase the time to progression and overall survival with a good quality of life.
Klíčová slova
FOLFIRINOX, karcinom slinivky břišní, toxicita, účinnostKarcinomy slinivky břišní tvoří ~2 % všech zhoubných nádorů (6 % všech úmrtí na zhoubný novotvar). Incidence a mortalita jsou stabilizované s mírným nárůstem bez jakéhokoli náznaku zlepšení ve srovnání s ostatními solidními nádory v ČR [1]. Nejčastějším histologickým typem (> 90 %) jsou duktální adenokarcinomy [2]. Jedná se o nádorové onemocnění se silnou tendencí k lokální invazi a vzdálenému metastazování. Při porovnání s ostatními solidními nádory jsou léčebné výsledky ve všech stadiích onemocnění nejhorší. Pětiletá doba přežití nemocných s karcinomem slinivky břišní je < 5 % [3,4]. Doba přežití byla stejná u mužů i žen [5]. Doba přežití u neléčeného metastazujícího onemocnění je ~2–3 měsíce [6].
Po dlouhých letech stagnace s monoterapií gemcitabinem [6,7] jako nejlepší možností systémové léčby přinesly výsledky dvou zásadních klinických studií kombinované chemoterapie (FOLFIRINOX: oxaliplatina, irinotekan, leukovorin, 5-fluorouracil/nab-paklitaxel plus gemcitabin) změnu klinických algoritmů jak lokalizovaného, tak metastazujícího onemocnění [8–10]. V klinické studii PRODIGE 4/ACCORD 11 byl medián celkové doby přežití při kombinaci FOLFORINOX 11,1 měsíců ve srovnání s 6,8 měsíci při monoterapii gemcitabinem [9]. V klinické studii IMPACT byl medián doby přežití 8,6 měsíců ve srovnání s 6,7 měsíci při monoterapii gemcitabinem [10].
Klinický trial PRODIGE 4/ACCORD 11 byl první klinickou studií, která změnila vnímání účinnosti chemoterapie v léčbě metastazujícího onemocnění. Použití režimu FOLFIRINOX signifikantně prodlužuje medián celkové doby přežití (11,1 měsíců vs 6,8 měsíců; míra rizika 0,57; p < 0,0001) a signifikantně prodlužuje čas do progrese (6,4 měsíců vs 3,3 měsíců; míra rizika 0,47; p < 0,0001). Léčebným rizikem je profil nežádoucích účinků (neutropenie stupeň 3/4 46 %, febrilní neutropenie 5 %). Hlavní obavou pro klinickou aplikaci FOLFIRINOXu je profil nežádoucích účinků. V tab. 1 je uvedeno původní dávkování v uvedené studii.
V klinické praxi jsou v řadě indikací uplatňovány dávkové modifikace oxaliplatiny, irinotekanu a bolusové dávky 5-fluorouracilu. Vliv dávkové modifikace na léčebnou účinnost není znám a je předmětem klinických analýz. Ukazuje se, že mírná modifikace dávkování nemusí být na úkor účinnosti při snížení toxicity režimu. V klinické studii fáze II s modifikací FOLFIRINOXu je použitá dávka irinotekanu 135 mg/m2 a bolusová dávka 5-fluorouracilu 300 mg/m2 s primární profylaxí pegfilgrastimem [9].
Pacienti a metody
Pacienti
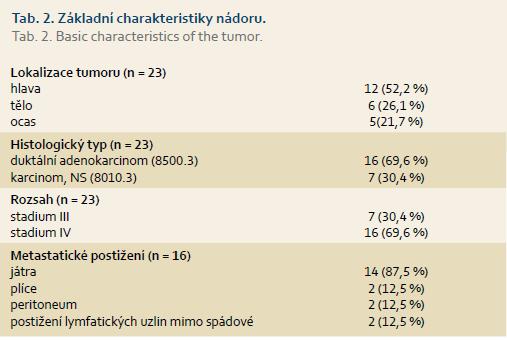
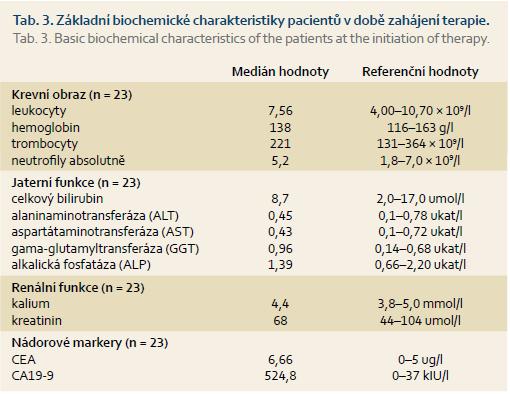
V období mezi lednem 2013 a červencem 2014 bylo na Onkologické klinice 1. LF UK a ÚVN – VFN v Praze léčeno režimem FOLFIRINOX pro karcinom slinivky břišní 23 nemocných (16 mužů a 7 žen) s mediánem věku 59,7 let (43,2–68,9). Diagnóza byla stanovena na základě histologického vyšetření (ve 13 případech, z toho materiál získán v šesti případech během explorativní laparotomie a v sedmi případech jehlovou jaterní biopsií pod CT kontrolou) nebo cytologického vyšetření (v deseti případech, materiál získán jehlovou aspirační biopsií během endosonografického vyšetření). Základní charakteristiky nádoru jsou uvedeny v tab. 2. Všichni pacienti byli v dobrém výkonnostním stavu (13 pacientů v PS 0 a 10 pacientů v PS 0). U čtyř nemocných předcházelo zahájení terapie zavedení stentu do žlučových cest. U všech byla provedena základní laboratorní vyšetření (krevní obraz, jaterní a renální parametry a nádorové markery, tab. 3).
Podávaný režim
Režim FOLFIRINOX byl podáván ve schématu dle studie PRODIGE 4/ACCORD 11 (tab. 1) s 25% redukcí oxaliplatiny, irinotekanu a bolusu 5-fluorouracilu. Dvacet pacientů dostalo tento režim v 1. linii paliativní terapie a tři pacienti dostali tento režim ve 2. linii po selhání monoterapie gemcitabinem. U všech nemocných byly během léčby pravidelně kontrolovány laboratorní hodnoty (krevní obraz, biochemický profil včetně nádorových markerů) s pravidelnými zobrazovacími vyšetřeními stran vývoje nemoci. Léčebné odpovědi byly hodnoceny podle RECIST 1.1 kritérií.
Statistika
Statistická analýza byla provedena s užitím software SAS (SAS Institute Inc., Cary, NC, USA) a grafy byly vytvořeny za pomoci GraphPad Prism 5.0 (GraphPad Software, CA). Pro měřené parametry v celém souboru byly počítány základní statistické údaje jako průměr, směrodatná odchylka, medián, minimum, maximum. Čas do progrese a doba celkového přežití byly též zpracovány graficky do tzv. KaplanMeyerových křivek.
Výsledky
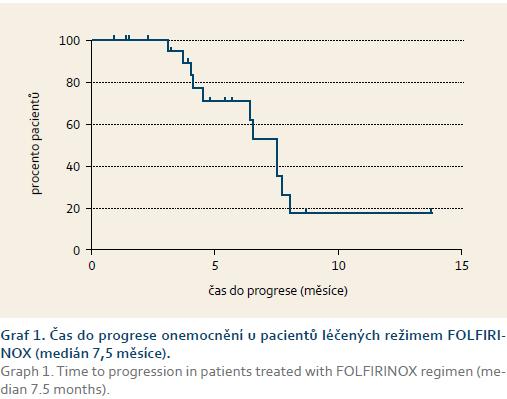
Terapii kombinací FOLFIRINOX absolvovalo 23 pacientů s mediánem počtu cyklů 10 (1–17). Bylo dosaženo mediánu času do progrese 7,5 měsíce (graf 1). Nejlepší dosaženou odpovědí byla u jednoho pacienta kompletní remise (úplné vymizení všech sledovaných lézí), u šesti pacientů parciální remise (zmenšení součtu nejdelších rozměrů známých nádorových ložisek o > 30 %), u tří pacientů stabilizace (zvětšení velikosti součtu nejdelšího rozměru známých nádorových ložisek o < 20 % nebo zmenšení tohoto rozměru o méně než 30 %), u pěti pacientů progrese onemocnění (zvětšení velikosti součtu nejdelšího rozměru známých nádorových ložisek o > 20 % nebo výskyt nového ložiska). U sedmi pacientů nelze odpověď hodnotit, protože ještě nebylo provedeno první kontrolní CT vyšetření (standardně prováděno po třech měsících terapie). U jednoho pacienta byla terapie po prvním cyklu ukončena, protože došlo k rychlému rozpadu tumoru pravděpodobně v důsledku vysoce účinné terapie s následnou hnisavou peritonitidou a rozvojem septického stavu. Pacient byl opakovaně operován a strávil přibližně jeden měsíc na jednotce intenzivní péče. Po stabilizaci stavu pokračoval gemcitabinem v monoterapii (t. č. je na 2. linii terapie). V současné době je 11 pacientů stále na léčbě FOLFIRINOX, jeden pacient podstoupil resekci pankreatu s nálezem kompletní patologické remise (tedy bez nálezu maligních buněk v resekátu pankreatu při vyšetření patologem) s následnou adjuvantní terapií gemcitabinem a jeden pacient cholangoitidy s výměnou a proplachy absolvuje konkomitantní radiochemo terapii (následně je u něj plánován resekční výkon). U deseti pacientů byla zaznamenána progrese dle RECIST 1.1 kritérií.
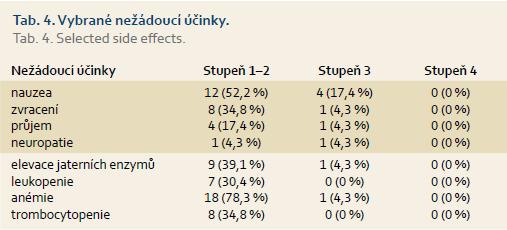
U pacientů byly zaznamenány očekávané nežádoucí účinky (tab. 4) s výjimkou jednoho případu hnisavé peritonitidy s rozvojem septického stavu po 1. cyklu chemoterapie FOLFIRINOX.Během terapie došlo k průměrnému váhovému úbytku –0,17 kg (–4 kg až +2 kg). U šesti pacientů byl pro nežádoucí účinky redukován irinotekan (u čtyř pacientů pro průjmy stupně 3,u jednoho pro nauzeu stupně 3 a zvracení stupně 2 i přes antiemetickou premedikaci,u jednoho pro opakované cholangoitidy s výměnou a proplachy stentu). U dvou pacientů byl irinotekan úplně vysazen pro průjmy (od 7. cyklu) a u jednoho pro opakované cholangitidy s elevací jaterních enzymů (od 4. cyklu). U pěti pacientů byla redukována dávka oxaliplatiny (u dvou pacientů pro neuropatie stupně 2, u dvou pacientů pro nauzeu a zvracení, u jednoho pro opakované cholangoitidy).U jednoho pacienta byla oxaliplatina pro neurotoxicitu úplně vysazena (od 15. cyklu), dále u jednoho pacienta pro alergickou reakci (od 7. cyklu) a u jednoho pro progredující nauzeu a zvracení (od 7. cyklu).
V dalších liniích (11 pacientů) byl u pěti pacientů podáván gemcitabin v monoterapii (u dvou v další linii kapecitabin) u dvou pacientů kapecitabin,u jednoho pacienta kombinace gemcitabin s nab-paklitaxelem, u jednoho nab-paklitaxel v monoterapii, u jednoho pacienta byl podáván FOLFOX 4 a jeden pacient byl léčen pouze symptomaticky.
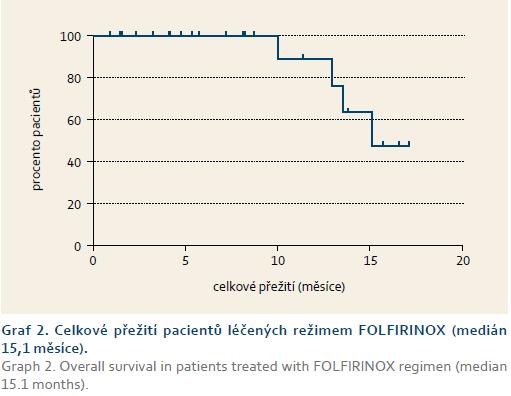
Bylo dosaženo mediánu celkového přežití 15,1 měsíce od diagnózy inoperabilního lokálně pokročilého nebo generalizovaného tumoru.
Diskuze
Užití režimu FOLFIRINOX v paliativní terapii lokálně pokročilého nebo generalizovaného karcinomu pankreatu
u pacientů v dobrém výkonnostním stavu vedlo ke statisticky významnému prodloužení času do progrese i celkového přežívání pacientů za cenu vyšší toxicity spojené s podáváním kombinované chemoterapie [8,9]. Nejčastějšími nežádoucími účinky stupně 3–4 provázejícími podávání tohoto režimu byla neutropenie (45,7 %, z toho 5,4 % febrilních neutropenií), únava (23,2 %), zvracení (14,5 %), průjem (11,4 %) a neuropatie (9,0 %) [9]. V rámci této pilotní analýzy bylo sledováno 23 pacientů, kteří byli režimem FOLFIRINOX léčeni na Onkologické klinice 1. LF UK a ÚVN – VFN Praha. U těchto pacientů bylo dosaženo mediánu času do progrese 7,5 měsíce s dosažením jedné kompletní remise a šesti parciálních regresí dle RECIST. Krom potvrzení významného prodloužení času do progrese a zvýšení procenta objektivních odpovědí (odpovídající datům z recentních multicentrických studií), a to i přes vstupní redukci dávek jednotlivých chemoterapeutik na 75 %, režim prokázal značný potenciál konverze primárně inoperabilního lokálně pokročilého karcinomu na operabilní s dosažením dlouhodobé remise.
Z hlediska nežádoucích účinků byly zaznamenány očekávané nežádoucí účinky stupně 3–4 odpovídající datům z dostupné literatury (zvracení, průjmy, neuropatie). V rozporu s literaturou nebyla v tomto souboru zaznamenána žádná neutropenie stupně 3–4 nebo febrilní neutropenie pravděpodobně v důsledku vstupní redukce dávky chemoterapie o 25 %. U jednoho pacienta musela být terapie přerušena po 1. cyklu z důvodu rozvoje hnisavé peritonitidy se septickým stavem. Dle operačního protokolu došlo k perforaci tenkého střeva v místě prorůstání karcinomu pravděpodobně v důsledku odpovědi nádoru na podávanou léčbu s následným rozpadem rumorózní masy.
Mediánu doby celkového přežití se dosáhlo 15,1 měsíce od diagnózy inoperabilního lokálně pokročilého nebo generalizovaného tumoru. Tato data jsou však velmi limitována malým počtem pacientů a krátkým časem sledování.
Závěr
U pacientů ve velmi dobrém výkonnostním stavu (0–1) s pokročilým karcinomem pankreatu může vést užití režimu FOLFIRINOX v redukci na 75 % ke značnému prodloužení času do progrese, zvýšení procenta objektivních odpovědí a také celkového přežívání při zachování dobré kvality života nemocných.
Práce vznikla v rámci projektu PRVOUK-P-27/LF1/1 a TIP FR-TI3/666.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Doručeno/Submitted: 29. 8. 2014
Přijato/Accepted: 6. 10. 2014
MUDr. Michal Vočka
Onkologická klinika 1. LF UK a ÚVN – VFN Praha
U Nemocnice 499/2, 128 00 Praha 2
michal.vocka@vfn.cz

Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
Literatura
1. Informační systém pro analytické zpracování dat Národního onkologického registru. Dostupné z: www.svod.cz.
2. Cowgill SM, Muscarella P. The genetics of pancreatic cancer. Am J Surg 2003; 186(3): 279–286.
3. Hidalgo M. Pancreatic cancer. N Engl J Med 2010; 362(17): 1605–1617. doi: 10.1056/ NEJMra0901557.
4. Verdecchia A, Francisci S, Brenner H et al. Recent cancer survival in Europe: a 2000–02 period analysis of EUROCARE-4 data. Lancet Oncol 2007; 8(9): 784–796.
5. Roazzi P, Capocaccia R, Santaquilani M et al. Electronic availability of EUROCARE-3 data: a tool for further analysis. Ann Oncol 2003; 14 (Suppl 5): 150–155.
6. Glimelius B, Hoffman K, Sjödén PO et al. Chemotherapy improves survival and quality of life in advanced pancreatic and biliary cancer. Ann Oncol 1996; 7(6): 593–600.
7. Burris HA 3rd, Moore MJ, Andersen J et al. Improvements in survival and clinical benefit with gemcitabine as first-line therapy for patients with advanced pancreas cancer: a randomized trial. J Clin Oncol 1997; 15(6): 2403–2413.
8. Conroy T, Desseigne F, Ychou M et al. FOLFIRINOX versus gemcitabine for metastatic pancreatic cancer. N Engl J Med 2011; 364(19): 1817–1825. doi: 10.1056/ NEJMoa1011923.
9. Von Hoff DD, Ervin T, Arena FP et al. Increased survival in pancreatic cancer with nabpaclitaxel plus gemcitabine. N Engl J Med 2013; 369(18): 1691–1703. doi: 10.1056/ NEJMoa1304369.
10. Gunturu KS, Yao X, Cong X et al. FOLFIRINOX for locally advanced and metastatic pancreatic cancer: single institution retrospective review of efficacy and toxicity. Med Oncol 2013; 30(1): 361. doi: 10.1007/ s12032-012-0361-2.