Syndrom arteria mesenterica superior v souvislosti s Crohnovou chorobou – kazuistika
Ivana Červinková1, Denisa Pavlovská1, Marcela Charvátová1, Jarmila Skotáková1
+ Pracoviště
Souhrn
Syndrom arteria mesenterica superior (SMAS) je vzácný stav charakterizovaný mechanickou kompresí třetí části duodena mezi břišní aortou a horní mezenterickou tepnou. Souvislost Crohnovy choroby se SMAS je v literatuře popisována raritně, ačkoliv pacienti s Crohnovou chorobou mají mnoho predispozic k jeho vzniku. Popisujeme případ 17leté pacientky s několik let diagnostikovanou Crohnovou chorobou, s 5 měsíců trvajícími příznaky břišního diskomfortu a s výraznou ztrátou hmotnosti. Klíčovou metodou pro stanovení dia gnózy SMAS byla magnetická rezonance (MR). Dále bylo retrospektivně zhodnoceno i starší kontrastní vyšetření výpočetní tomografií (CT) s posouzením velikosti aortomezenterického úhlu a vzdálenosti, jejichž snížení je dia gnostickým kritériem pro SMAS. Naším cílem je upozornit na důležitost měření těchto hodnot u pacientů s Crohnovou chorobou pro včasné odhalení rizika SMAS.
Klíčová slova
syndrom arteria mesenterica superior, Crohnova choroba, magnetická rezonanceÚvod
Syndrom arteria mesenterica superior (SMAS), známý jako Wilkie syndrom, je vzácným stavem. Onemocnění popsal poprvé v roce 1842 Carl von Rokitansky, v roce 1927 zveřejnil Wilkie studii založenou na 75 případech. Incidence je udávána 0,013–0,3 %, maximum výskytu u žen ve věku 10–39 let [1].
Arteria mesenterica superior je tepna vycházející z aorty v úrovni prvního bederního obratle. Zde je uzavřena v mezenterickém tuku a lymfatické tkáni, které chrání duodenum před kompresí. Pokud dojde ke zmenšení tohoto polštáře, zúží se úhel mezi abdominální aortou (AA) a horní mezenterickou tepnou (SMA) z obvyklých 38–56° na 6–25°, a dochází tak ke kompresi duodena s příznaky střevní obstrukce. Aortomezenterická vzdálenost přitom činí 2–8 mm, na rozdíl od typických 10–20 mm [2,3].
U nemocných se objevuje nauzea, zvracení, postprandiální bolest břicha, anorexie a ztráta hmotnosti [3]. Příčinou bývají stavy po operacích spojené s úbytkem a narušením mezenteriálního tuku nebo rychlá a velká ztráta hmotnosti z různých příčin. Obojí můžeme vidět u pacientů s Crohnovou chorobou [4].
Popis případu
Popisujeme případ nyní 17leté mladé ženy s diagnostikovanou Crohnovou chorobou s postižením terminálního ilea, tračníku, žaludku a duodena. Již před diagnostikováním Crohnovy choroby byla sledována pro opakované sinusitidy, afty a stomatitidy, dále pro atopický ekzém a také pro intoleranci laktózy. V roce 2010 došlo ke změně frekvence a konzistence stolic, jednalo se o 3–6 hnědožlutých, kašovitých stolic denně, i v noci, nucení na stolici bylo ihned při jídle, chuť k jídlu byla snížená, byl patrný také hmotnostní úbytek. V roce 2011, v jejích 9 letech, byla následně stanovena diagnóza Crohnovy choroby. V roce 2017 došlo při konvenční terapii k výraznému zhoršení nemoci s následnou ileocékální resekcí a reresekcí s ileo-ascendentoanastomózou, adheziolýzou a evakuací abscesu pod ventrální břišní stěnou. V roce 2018 byla zahájena biologická léčba (Remicade).
Posledních 5 měsíců si pacientka stěžovala na chronický pocit plnosti žaludku, nechuť k jídlu, nevolnost a značný hmotnostní úbytek. K akutnímu zhoršení těchto potíží došlo v návaznosti na podanou biologickou léčbu, což mohlo mít, jak se později ukázalo, také souvislost s probíhajícím lehčím viroinfektem. Laboratorní odběry byly bez významných změn, bez anemie, leukocytózy, C reaktivní protein (CRP) nízký. Úbytek hmotnosti byl 6 kg a pacientka měla 39,6 kg při výšce 167,4 cm, body mass index (BMI) 14,1.
V širší diferenciálně diagnostické rozvaze byl zhotoven prostý snímek hrudníku, který byl bez patologického nálezu. Na ultrazvuku byl nález normálně průchodné ileo-ascendentoanastomózy s minimální akcentací a hraniční šíří stěny v oblasti anastomózy. Dále byla patrna hypersekrece, hyper- a dysmotilita kliček ilea, které byly kalibru až 25 mm. V porovnání s předchozími ultrazvukovými nálezy se jednalo o dlouhodobě popisované změny po opakovaných operacích, bez nových změn, které by vysvětlovaly aktuální potíže pacientky.
Následně byla provedena MR – enterografie (MRE) s aplikací 600 ml roztoku 2,5% mannitolu perorálně a s intravenózní aplikací 4 ml přípravku Gadovist. Vzhledem ke špatné náplni kliček je juna a ilea bylo vyšetření doplněno polohováním pacientky na břicho, ale střevní kličky nadále zůstávaly téměř bez obsahu. V MR nálezu dominoval obraz distenze žaludku a D1 a D2 duodena, D3 bylo nenaplněno – komprimováno. Byla zmenšena vzdálenost mezi SMA a AA na 7 mm, aortomezenterický úhel byl zmenšen na 14°. Obraz odpovídal diagnóze Wilkie syndromu (obr. 1).
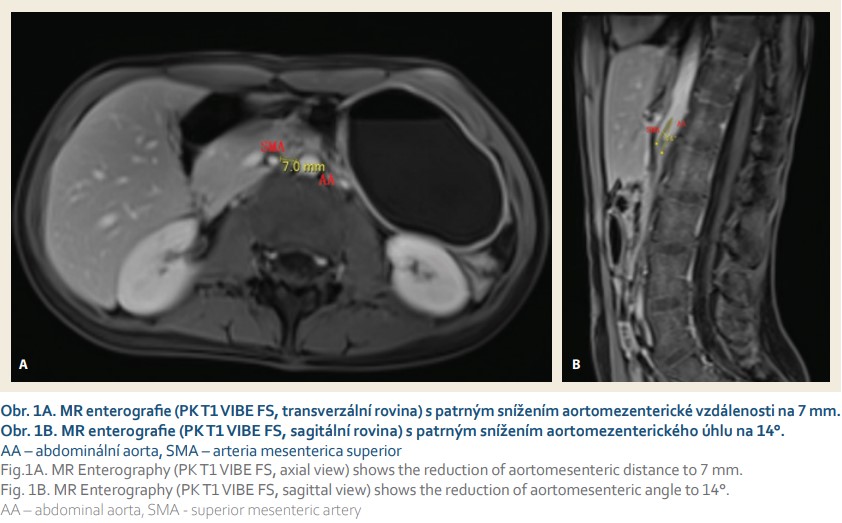
Byla také doplněna gastroskopie, kde byl popisován pseudopolypoidní vzhled sliznice kardie, diskolorace antra a prepylorické krajiny, duodenum bylo při makroskopickém vyšetření v normě. Histologicky byla prokázána mírná reaktivní gastropatie polékového typu.
Při léčbě tohoto stavu byla zpočátku částečně parenterální nutrice, posléze pro obtížné dosažení ideálního kalorického příjmu však byla pacientka převedena na úplnou exkluzivní enterální výživu (Modulen). Bylo zvažováno zavedení nazojejunální sondy, ale na přání pacientky a rodiny byl zvolen maximálně konzervativní postup s postupným mírným hmotnostním přírůstkem, kdy mohla být pacientka propuštěna do domácí péče.
Pro zajímavost jsme se zpětně podívali na kontrastní CT vyšetření, které bylo provedeno při exacerbaci Crohnovy choroby v roce 2017. Již na tomto vyšetření bylo patrné zmenšení vzdálenost mezi SMA a AA na 8 mm, aortomezenterický úhel byl zmenšen na 17°, ale tyto skutečnosti v popisu vyšetření uvedeny nebyly (obr. 2).
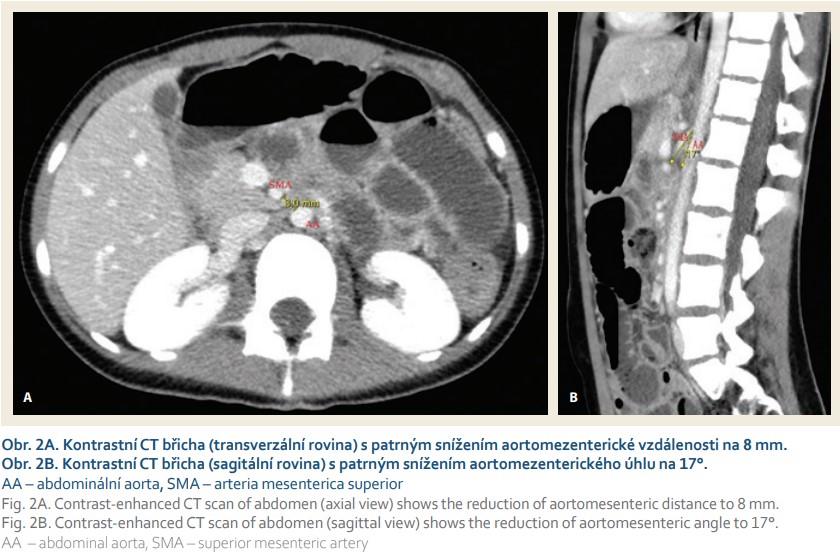
Diskuze
Diagnóza SMAS je založena na kombinaci klinických příznaků a radiologického průkazu obstrukce. Prostý rentgenový snímek ukazuje dilatované, tekutinou a plynem naplněné duodenum a žaludek. Vyšetření s baryovou kontrastní látkou prokazuje dilataci první a druhé části duodena, vnější kompresi jeho třetí části a kolabované tenké střevo distálně od zúžení. Jako referenční standard při diagnostice SMAS byla navržena v minulosti angiografie, která je nyní rovnocenně nahrazena neinvazivním vyšetřením pomocí kontrastního CT či MR, na nichž je možné přesně změřit aortomezenterickou vzdálenost a úhel. Dále lze v diagnostice využít i ultrazvukové dopplerovské vyšetření a také vyšetření endoskopické [1,3].
Autoři Cicero et al (2018) zveřejnili využití nové „hybridní“ MRE metody u pacientů s klinickým podezřením na strikturu duodena nebo jejuna, která zvyšuje výtěžnost vyšetření. V první fázi se jedná o MR fluoroskopii, kdy pacient v poloze na břiše popíjí orální kontrastní látku v průběhu MR fluoroskopických sekvencí. V druhé době navazují standardní MRE sekvence. Na MR fluoroskopii vidíme obraz shodný s konvenční fluoroskopií, navíc na MRE můžeme vidět zmenšení aortomezenterické vzdálenosti a úhlu, což je hlavním znakem SMAS. Zobrazovací modalita bez záření – MRE, již zahrnutá ve standardním diagnostickém algoritmu zánětlivého onemocnění střev, by tedy mohla být nápomocná při včasném rozpoznávání SMAS. Tuto metodu autoři popisují v souvislosti se dvěma kazuistikami mladých žen (23 a 27 let) s diagnostikovanou Crohnovou chorobou a s několik měsíců trvajícím břišním diskomfortem a s hmotnostním úbytkem, kde byl takto prokázán SMAS [4].
V literatuře se nám podařilo dohledat další dva popsané případy SMAS u pacientů s Crohnovou chorobou. Lourenço et al (2017) popisují přidružený Wilkie syndrom u 36leté ženy s diagnostikovanou Crohnovou chorobou gastroduodena po období těžké ztráty hmotnosti [5]. Další kazuistika mladého muže s Wilkie syndromem ve spojení s Crohnovou chorobou byla referována Salamem [6].
Pacienti s Crohnovou chorobou mají vícero predispozic pro vznik SMAS, přesto je tato souvislost v literatuře popisována jen raritně. Sami jsme se při retrospektivním hodnocení CT naší pacientky přesvědčili, že měření aortomezenterické vzdálenosti a úhlu se rutinně neprovádí, což zřejmě podhodnocuje výskyt SMAS. Naše pacientka měla tyto hodnoty snížené, ale byla bez příznaků svědčících pro SMAS, což je u pacientů s nízkým BMI, zvláště u dětí, známé [7]. V souvislosti s vyšetřováním pacientů s diagnostikovanou Crohnovou chorobou na MR a CT je tedy vhodné všímat si hodnot aortomezenterické vzdálenosti a úhlu, pokud jsou měřitelné. V případě snížených hodnot, při objevení se příznaků typických pro SMAS tak může být přikročeno k léčbě dříve, než nastanou komplikace, které mohou vést až k úmrtí. To je zvláště důležité v souvislosti se zvyšujícím se počtem dětských pacientů s Crohnovou chorobou, které na našem pracovišti vyšetřujeme. V první fázi bývá totiž léčba konzervativní. Je doporučeno jíst po malých porcích, polohovací manévry během jídla, léky zvyšující motilitu, úprava nutrice a odstranění či zmírnění vyvolávajícího faktoru. Hmotnostního přírůstku lze docílit výživou periferním či centrálním žilním katétrem nebo enterální jejunální sondou. Tak dochází k hyperalimentaci a opětovnému hromadění tuku v aortomezenterickém úhlu. Pokud konzervativní léčba selže, pak je metodou volby duodenojejunoanastomóza [3,8].
Závěr
Závěrem lze říct, že kazuistiky popisující souvislost Crohnovy choroby se SMAS jsou ojedinělé, i když se u pacientů s Crohnovou chorobou mnohdy vyskytuje vícero predispozičních faktorů najednou, které mohou vést k tomuto syndromu. Je nutno na to pomýšlet a při hodnocení CT nebo MR vyšetření se na tuto oblast speciálně zaměřit. Naše zkušenost dokládá, že při rutinním hodnocení vyšetření může být tento syndrom přehlédnut.
Doručeno/Submitted: 13. 5. 2020
Přijato/Accepted: 15. 5. 2020
MUDr. Ivana Červinková
Klinika dětské radiologie
LF MU a FN Brno
Černopolní 9
662 63, Brno
icervinkova@seznam.cz
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Mandarry MT, Zhao L, Zhang C et al. A comprehensive review of superior mesenteric artery syndrome. Eur Surg 2010; 42 (5): 229–236. doi: 10.1007/s10353-010-0561-y.
2. So CY, Chan KY, Au HY et al. Superior mesenteric artery (SMA) syndrome: an unusual cause of intestinal obstruction in palliative care. Ann Palliat Med 2016; 6 (1): 91–93. doi: 10.21037/apm.2016.07.03.
3. Válková L. Syndrom arteria mesenterica superior – syndrom Wilkie. Interní Med 2011; 13 (9): 353–354.
4. Cicero G, D’Angelo T, Bottari A et al. Superior Mesenteric Artery Syndrome in Patients with Crohn’s Disease: a Description of 2 Cases Studied with a Novel Magnetic Resonance Enterography (MRE) Procedure. Am J Case Report 2018; 19: 431–437. doi: 10.12659/ajcr.908 273.
5. Lourenço LC, Martins A, Oliveira AM et al. Wilkie Syndrome behind Crohn Disease? Superior Mesenteric Artery Syndrome Mimicking and Complicating Crohn Disease of the Upper Gastrointestinal Tract. GE Port J Gastroenterol 2017; 24 (1): 50–52. doi: 10.1159/000450 873.
6. Salam HA. Superior mesenteric artery syndrome. [online]. Available from: http: //www.radiopaedia.org/cases/superior-mesenteric-artery-syndrome-2.
7. Arthurs OJ, Mehta U, Set PA. Nutcracker and SMA syndromes: What is the normal SMA angle in children? Eur J Radiol 2012; 81 (8): e854–e861. doi: 10.1016/j.ejrad.2012.04.010.
8. Welsch T, Büchler MW, Kienle P. Recalling superior mesenteric artery syndrome. Dig Surg 2007; 24 (3): 149–156. doi: 10.1159/000102 097.