Stent jako řešení perforace „černého jícnu“
Miloš Rys1, Tomáš Fejfar Orcid.org 2, Rudolf Repák Orcid.org 2, Štěpán Šembera Orcid.org 2, Marcela Kopáčová Orcid.org 2, Ilja Tachecí2
+ Pracoviště
Souhrn
„Černý jícen“, známý též jako akutní nekróza jícnu (AEN – acute esophageal necrosis), je relativně vzácné onemocnění charakterizované černým zabarvením sliznice jícnu. Postižení může být lokalizováno pouze distálně, možné je ale také postižení celého jícnu. Nejčastějším klinickým projevem je hemateméza, v rizikových skupinách nemocných je spojen se zvýšenou letalitou. Včasná diagnostika AEN je spojena s provedením gastroskopie, zahájení adekvátní léčby je základem příznivé prognózy pacienta. Mezi nejzávažnější komplikace AEN patří perforace jícnu s rizikem dalších komplikací, jako je mediastinitida a sepse. Vzhledem k charakteru onemocnění, postižení jícnu a potenciálně i mediastina je nutné k pacientovi přistupovat multioborově. Níže předkládáme kazuistiku 68letého pacienta s diagnózou AEN komplikované perforací potvrzenou pomocí CT a časné endoskopie. Jako primární řešení perforace jícnu byl zvolen endoskopický přístup se zavedením plně potahovaného metalického stentu. U pacienta přesto došlo k rozvoji dalších komplikací perforace: mediastinitida, empyém s nutností zavedení hrudní drenáže. Kromě intervenčních metod byl pacient léčen širokospektrými antibiotiky a kombinací parenterální a enterální výživy. Po 3 měsících léčby a zvládnutí komplikací byl pacient v dobrém klinickém stavu propuštěn do ambulantní péče.
Klíčová slova
akutní nekróza jícnu, perforace jícnu, mediastinitida, Danišův stent, metalický stent
Úvod
„Černý jícen“, známý také jako akutní nekróza jícnu, je vzácné onemocnění, které bylo poprvé popsáno Goldenbergem et al v roce 1990 [1]. Prevalence AEN je uváděna mezi 0,001 a 0,28 % z provedených endoskopických a pitevních vyšetření [2,3]. Incidence AEN je 4krát vyšší u mužů ve srovnání se ženami a průměrný věk je v době diagnózy 68 let [4,5]. Onemocnění je diagnostikováno při gastroskopii (EGD), projevuje se difuzním černým zbarvením sliznice v celé cirkumferenci, většinou pouze distálního jícnu. Nekrotická sliznice je s hemoragickou, křehkou spodinou a je ostře ohraničena od normálního cylindrického epitelu v oblasti gastroezofageální junkce. Později je jícen pokryt bělavým exsudátem kryjícím granulační tkáň [4,6]. Nekróza vznikající nejspíše na podkladě ischemie může postihovat i submukózu a svalovinu jícnu. Pacienti většinou přicházejí pro známky krvácení do horní části trávicího traktu, jako jsou hemateméza či meléna. Mezi další typické symptomy patří bolest v epigastriu, nauzea, zvracení, dysfagie, bolesti na hrudi a synkopa. Klinické vyšetření je většinou nespecifické a odvíjí se od aktuálního stavu pacienta. Může být přítomna tachykardie, hypotenze, šok, horečka, kachexie, hypoxie a citlivost v oblasti břicha [4]. Laboratorní nálezy spíše odpovídají základnímu onemocnění. Často bývá zachycena laktátová acidóza, hypoalbuminemie, anemie, renální insuficience a hyperglykemie.
Etiopatogeneze AEN je multifaktoriální a není jednoznačně vysvětlena. Může být ovlivňována více faktory jako poškozením jícnu refluxátem (např. při obstrukci výtokového traktu žaludku), narušením cévního zásobení jícnu vedoucím následně k jeho hypoperfuzi a ischemii. Dále poškozením ochranné bariéry způsobeným oslabením imunitního systému nebo oběhovou nestabilitou např. u septického stavu [7,8]. Riziko vzniku AEN je vyšší u mužů, u nemocných s vyšším věkem, s paraezofageální kýlou, traumatem a komorbiditami jako diabetes mellitus, diabetická ketoacidóza, chronické onemocnění jater, arteriální hypertenze, ateroskleróza, malnutrice, abúzus alkoholu a onkologické onemocnění [9].
Kazuistika
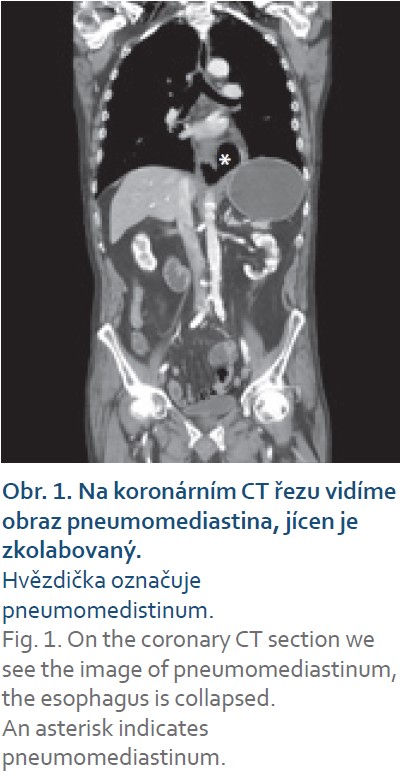
Osmašedesátiletý muž, hypertonik, léčený pětikombinací antihypertenziv, po recentní resekci karcinomu jazyka a spodiny ústní se dostavil v listopadu 2020 pro nauzeu, úporné zvracení a bolesti břicha na urgentní příjem. Pacient byl afebrilní, bez klinických známek krvácení do trávicí trubice, kardiopulmonálně kompenzován. Akutně byl proveden UZ břicha s nálezem distenze žaludku, proto byl pacient následně indikován k CT vyšetření. Na kontrastním CT trupu bylo popsáno rozsáhlé pneumomediastinum, ztluštění distálního jícnu s lemem tekutiny a podezření na perforaci jícnu (obr. 1). Pacient byl přijat na jednotku intenzivní péče, empiricky zajištěn antibiotiky (imipenem a metronidazol i.v.) a i.v. podávanými inhibitory protonové pumpy.
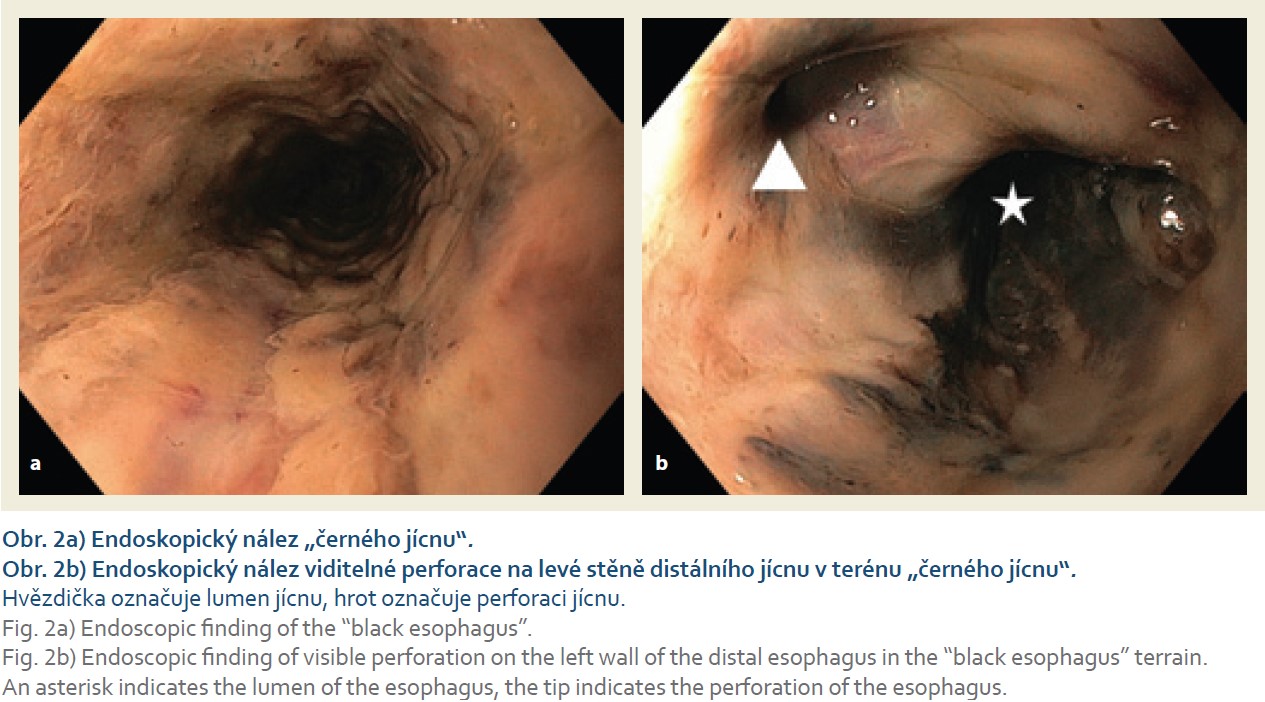
Bylo doplněno gastroskopické vyšetření, které potvrdilo drobnou perforaci (o velikosti cca 5 mm) 15 mm nad Z linií v terénu „černého jícnu“ a dvě nevelké ulcerace bulbu duodena s fibrinovou spodinou. Distální pól perforace jícnu byl označen klipem a k překrytí perforačního otvoru byl zaveden Danišův stent (obr. 2). Nutrice byla řešena zavedením nazojejunální sondy a enterální výživou v kombinaci s přechodnou doplňkovou parenterální výživou. Kontrolní snímek plic provedený 4. den hospitalizace pro dušnost prokázal progredující fluidothorax vlevo. Vzhledem k tomu byla provedena hrudní drenáž. Aplikace kontrastní látky cestou nazogastrické sondy (NGS) jednoznačně neprokázala leak do mediastina, ATB terapie byla posílena o flukonazol.
Stav byl 22. den hospitalizace komplikován vznikem empyému hrudníku vlevo s lokulovanými porcemi a bublinami plynu dle CT. Kontrolní CT hrudníku 30. den hospitalizace prokázalo regredující reziduální fluidothorax vlevo, kontrastní vyšetření bylo již stran komunikace s jícnem negativní. Postupně byl extrahován hrudní drén i NGS a 45. den hospitalizace nakonec endoskopicky také Danišův stent. Defekt v distálním jícnu byl zcela zhojen. Po 50 dnech hospitalizace byl pacient propuštěn domů s doporučením pokračovat v terapii blokátory protonové pumpy.
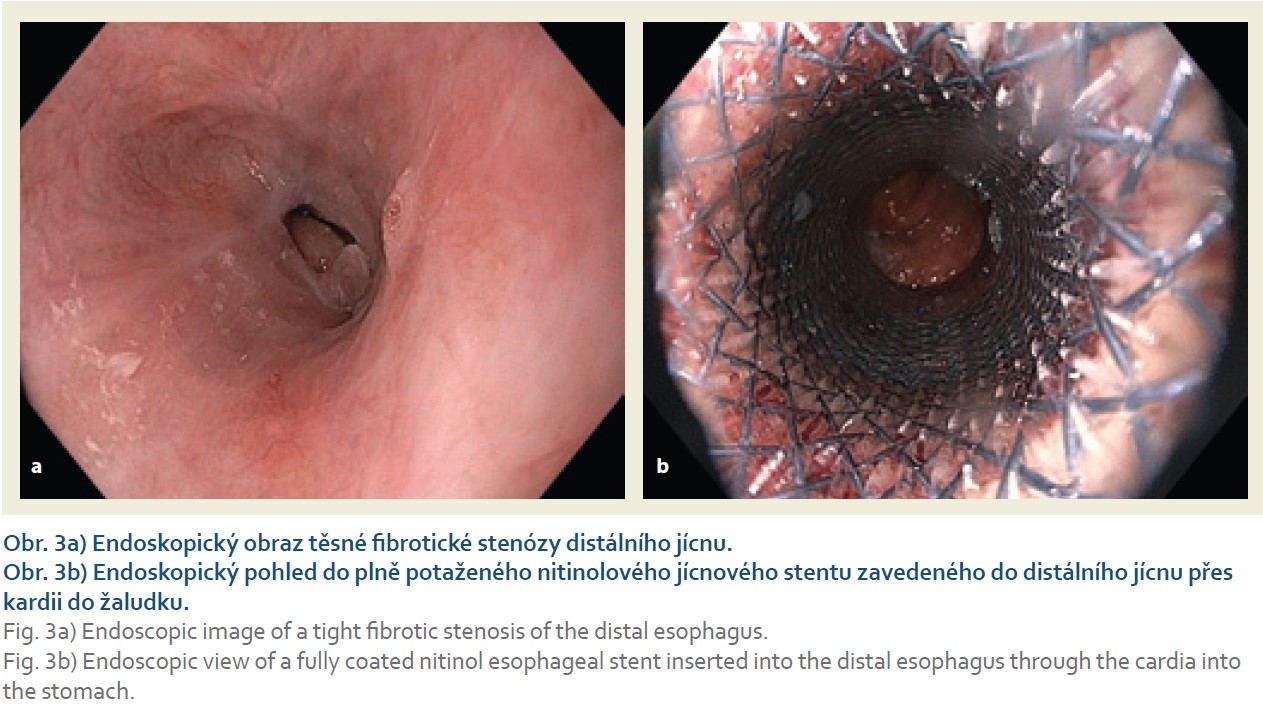
Za měsíc po propuštění přichází nemocný pro dysfagie tuhých soust. Při skiaskopii jícnu byla nalezena těsná stenóza distálního jícnu s podezřením na vlasovou píštěl v oblasti původní perforace. Následná gastroskopie prokázala stenózu distálního jícnu neprostupnou pro endoskop (obr. 3). Pod skiaskopickou kontrolou byl proto zaveden samoexpandibilní, plně potahovaný metalický stent (SEMS) SX-ELLA HV PLUS 85 × 25/20/24 mm. Týden poté bylo provedeno pro progredující dušnost CT vyšetření hrudníku, které prokázalo recidivu ohraničeného empyému vlevo. Přechodně byla znovuzavedena hrudní drenáž. Empirická antibiotická léčba byla upravována dle kultivačních nálezů s pozitivním vývojem klinického stavu a regresí empyému. Stent byl extrahován po 3 měsících, nemocný je asymptomatický.
Diskuze
Prezentovaná kazuistika je zajímavá z několika úhlů pohledu. Jedná se o popis relativně vzácného onemocnění jícnu se závažnými komplikacemi (perforace jícnu, mediastinitida, empyém hrudníku, stenóza jícnu), které byly řešeny konzervativně zavedením dvou potahovaných metalických stentů a opakovanou hrudní drenáží. Onemocnění bylo komplikováno perzistující komunikací s pleurální dutinou a recidivujícím epyémem hrudníku.
Akutní nekróza jícnu je vzácné onemocnění s potenciálně vysokou letalitou (až 32 %), především ve skupině nemocných s rizikovými faktory (polymorbidita, vyšší věk, vysoká tepová frekvence, nízká hladina hemoglobinu a albuminu) [3,10]. V rozsáhlém přehledu z roku 2019 bylo hodnoceno 130 případů s nálezem „černého jícnu“. Nejčastějšími symptomy onemocnění byla hemateméza (66 %), meléna (33 %), šok/synkopa (36 %), bolesti břicha či hrudníku (28 %) a dysfagie (12 %). Nález byl nejčastěji spojen s komorbiditami jako diabetes mellitus (38 %), arteriální hypertenze (37 %), abúzus alkoholu (25 %), chronická renální insuficience (16 %), hyperlipidemie (10 %), malignita (10 %) a diabetická ketoacidóza (9 %). V popisovaném souboru bylo zjištěno postižení distální třetiny jícnu v 50 %, panezofageální postižení v 34 % a izolované postižení horní části jícnu jen ve 2 % [10]. Při EGD je možné odebrání biopsie k vyloučení infekční příčiny AEN (Klebsiella pneumonie, Candida albicans, CMV a Herpes simplex virus) [5,11]. Diferenciálně diagnosticky se černé zabarvení sliznice jícnu může vyskytovat také u maligního melanomu, melanosis, acanthosis nigricans a v případě přítomnosti depozit uhelného prachu [12]. V našem případě byl popisován výskyt spontánní perforace černého jícnu u staršího polymorbidního pacienta (hypertenze, malignita), infekční etiologie potvrzena nebyla. Vstupní prezentace onemocnění byla bez klinických známek krvácení do trávicí trubice, příčinou stavu byla hypovolemie navozená úporným zvracením při vředové chorobě duodena a pylorostenóze.
Mezi časté projevy AEN patří akutní krvácení, které se vyskytuje až v 66 % případů. Až u 25 % pacientů je AEN komplikována vznikem striktury. Koexistence duodenálních ulcerací je spojena s rizikem vzniku ezofageální striktury v 35–50 % případů [4,10]. Mezi nejvážnější komplikaci akutní fáze AEN patří perforace jícnu, vyskytuje se až v 7 % případů [13]. Při klinickém vyšetření můžeme u pacienta s perforací jícnu najít podkožní emfyzém. Tato komplikace může rovněž vést ke vzniku akutní mediastinitidy, mediastinálního abscesu, empyému a k rozvoji septického stavu [14,15]. Perforaci jícnu diagnostikujeme nejlépe pomocí CT hrudníku se senzitivitou 92–100 % [16].
Specifická léčba AEN neexistuje, zásadní je terapie základního onemocnění, které se podílí na jeho vzniku. V úvodu by měla být léčba zaměřena na hemodynamickou stabilitu s intravenózním doplněním tekutin k zajištění dostatečné orgánové perfuze. Pacient by měl být zajištěn inhibitory protonové pumpy (PPI) i.v. v terapeutickém režimu, perorální příjem by měl být zastaven. Po jeho obnovení je doporučeno zvažovat podávání suspenze sukralfátu jako prevence dalšího poškozením jícnu pro schopnost vazby pepsinu a stimulaci mukózní sekrece [10,17]. Antibiotická léčba není nezbytná. Širokospektrá antibiotika by měla být empiricky nasazena při známkách sepse, horšení klinického stavu, u imunokompromitovaných pacientů nebo při podezření na perforaci [14]. Mezi podpůrnou léčbu patří také adekvátní nutrice, v úvodu parenterální cestou, dále antiemetická a analgetická terapie [10]. Léčba by měla být upravována individuálně, dle výsledku biopsie, s nasazením antifungální či antivirotické léčby.
Léčba komplikací černého jícnu zahrnuje endoskopickou zástavu krvácení preferenčně pomocí lokální aplikace adrenalinu submukózně [14]. Pokud nedojde k zástavě krvácení, je indikováno zavedení SEMS [18]. Zavedení NGS není obecně doporučováno pro riziko perforace, ale je ke zvážení u pacientů s nutností dekomprese při obstrukci výtokového traktu žaludku [17]. Iniciálním řešením stenózy jícnu je její balonková dilatace. Pro komplexní či refrakterní stenózy je indikováno zavedení SEMS. V případě refrakterní striktury by mělo být přistoupeno k chirurgickému řešení, doporučována je ezofagektomie [15]. Také perforace jícnu je indikací ke zvážení chirurgické léčby. V současnosti však přibývá kazuistik, kdy se jako úspěšná léčba perforace uplatňuje zavedení SEMS [14].
V naší kazuistice byla diagnostika perforace černého jícnu provedena bezprostředně po vstupním klinickém vyšetření pomocí CT a gastroskopie. Současná přítomnost mediastinitidy naznačuje, že k perforaci došlo s určitým časovým odstupem a vedla pravděpodobně ke komplikovanému průběhu onemocnění i přes včasné zahájení adekvátní léčby (ATB, PPI, zavedení stentu). Během hospitalizace se vyvinuly recidivující píštěl a empyém s nutností opakované stentáže a drenáže jícnu, stenóza jícnu s potřebou dilatace. Pacient byl však ušetřen rozsáhlého chirurgického výkonu v oblasti jícnu s významnou morbiditou i letalitou.
Závěr
Kazuistika prezentuje komplikovaný průběh relativně vzácného onemocnění: akutní nekrózy jícnu. Ačkoli jde často o náhodný nález s relativně dobrou prognózou (při adekvátní terapii zaměřené na obnovení dostatečné orgánové perfuze), ve významném procentu může být černý jícen spojen s vysokou letalitou a závažnými komplikacemi. I v těchto případech (perforace jícnu, mediastinitida) je ovšem možné zvažovat nechirurgickou léčbu založenou na uzavření komunikace mezi jícnem a okolními strukturami potahovaným stentem, terapii ATB, PPI a řešení dalších komplikací (drenáž empyému hrudníku, dilatace stenózy jícnu po zhojené perforaci). Chirurgické řešení zůstává přesto zlatým standardem.
ORCID autorů
T. Fejfar ORCID 0000-0002-4126-4067,
R. Repák ORCID 0000-0002-8288-2646,
Š. Šembera ORCID 0000-0003-0151-9982,
M. Kopáčová ORCID 0000-0002-5600-5594,
I. Tachecí ORCID 0000-0003-3583-2651.
Doručeno/Submitted: 25. 5. 2022
Přijato/Accepted: 1. 6. 2022
MUDr. Miloš Rys
Interní oddělení
Chrudimská nemocnice – Nemocnice Pardubického kraje, a. s.
Václavská 570
537 27 Chrudim
milos.rys@gmail.com
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Goldenberg SP, Wain SL, Marignani P. Acute necrotizing esophagitis. Gastroenterology 1990; 98(2): 493–496. doi: 10.1016/0016-5085(90)90844-q.
2. Lamers CR, Mares WGN, Bac DJ. Black esophagus: a case series and literature review of acute esophageal necrosis. Scand J Gastroenterol 2018; 53(10–11): 1421–1424. doi: 10.1080/00365521.2018.1513064.
3. Gurvits GE, Shapsis A, Lau N et al. Acute esophageal necrosis: a rare syndrome. J Gastroenterol 2007; 42(1): 29–38. doi: 10.1007/s00535-006-1974-z.
4. Gurvits GE, Cherian K, Shami MN et al. Black esophagus: new insights and multicenter international experience in 2014. Dig Dis Sci 2015; 60(2): 444–453. doi: 10.1007/s10620-014-33 82-1.
5. Ben Soussan E, Savoye G, Hochain P et al. Acute necrotizing esophagitis: a large retrospective case series. Endoscopy 2004; 56(2): 213–217. doi: 10.1016/s0016-5107(02)70180-6.
6. Rejchrt S, Douda T, Kopácová M et al. Acute esophageal necrosis (black esophagus): endoscopic and histopathologic appearance. Endoscopy 2004; 36(12): 1133. doi: 10.1055/s-2004-825971.
7. Siddiqi A, Chaudhary FS, Naqvi HA et al. Black esophagus: a syndrome of acute esophageal necrosis associated with active alcohol drinking. BMJ Open Gastroenterol 2020; 7(1): e000466. doi: 10.1136/bmjgast-2020-000466.
8. Schizas D, Theochari NA, Mylonas KS et al. Acute esophageal necrosis: a systematic review and pooled analysis. World J Gastrointest Surg 2020; 12(3): 104–115. doi: 10.4240/wjgs.v12.i3.104.
9. Day A, Sayegh M. Acute oesophageal necrosis: a case report and review of the literature. Int J Surg 2010; 8(1): 6–14. doi: 10.1016/ j.ijsu.2009.09.014.
10. Kim SM, Song KH, Kang SH et al. Evaluation of prognostic factor and nature of acute esophageal necrosis: restropective multicenter study. Medicine (Baltimore) 2019; 98(41): e17511. doi: 10.1097/MD.0000000000017511.
11. Abdullah HM, Ullah W, Abdallah M et al. Clinical presentations, management, and outcomes of acute esophageal necrosis: a systemic review. Expert Rev Gastroenterol Hepatol 2019; 13(5): 507–514. doi: 10.1080/17474124.2019.1601555.
12. Maher MM, Nassar MI. Black esophagus: a case report. Cases J 2008; 1(1): 367. doi: 10.1186/1757-1626-1-367.
13. Martins D, Marques R, Costa P et al. The dark side of the esophagus. Autops Case Rep 2021; 11: e2021284. doi: 10.4322/acr.2021.284.
14. Dias E, Santos-Antunes J, Macedo G. Diagnosis and management of acute esophageal necrosis. Ann Gastroenterol 2019; 32(6): 529–540. doi: 10.20524/aog.2019.0418.
15. Akaishi R, Taniyama Y, Sakurai T et al. Acute esophageal necrosis with esophagus perforation treated by thoracoscopic subtotal esophagectomy and reconstructive surgery on a secondary esophageal stricture: a case report. Surg Case Rep 2019; 5(1): 73. doi: 10.1186/s40792-019-0636-3.
16. Ali D, Detroz A, Gorur Y et al. Abrupt severe chest pain and vomiting: remember to think of a ruptured oesophagus (Boerhaave syndrome). Eur J Case Rep Intern Med 2019; 6(10): 001265. doi: 10.12890/2019_001265.
17. Mishkin DS, Geruld D. Acute esophageal necrosis (black esophageus). In: Rose BD (ed). UpToDate. Watham MA 2020.
18. Messner Z, Gschwantler M, Resch H et al. Use of the Ella Danis stent in severe esophageal bleeding caused by acute necrotizing esophagitis. Endoscopy 2014; 46(Suppl 1): E225–E226. doi: 10.1055/s-0034-1365384.