Stanovení lepku ve stolici jako metoda k ověření compliance s bezlepkovou dietou u dětí s nově diagnostikovanou celiakií
Radim Vyhnánek1, Ziad Khaznadar2, Roman Vyhnánek1, Milan Paulík2
+ Pracoviště
Souhrn
Úvod: Cílem studie bylo porovnat koncentraci lepku ve stolici pomocí měření z lepku odvozených imunogenních peptidů (GIP – gluten-related immunogenic peptides) s koncentrací protilátek proti tkáňové transglutamináze ve třídě IgA (anti-tTG IgA) v krvi u dětí s nově diagnostikovanou celiakií. Metody: Studie se zúčastnily děti, kterým byla na našem pracovišti diagnostikována od května 2018 do května 2020 celiakie a splnily podmínky studie. Při stanovení diagnózy jsme kromě anti-tTG IgA v krvi změřili GIP ve stolici. Tato vyšetření jsme zopakovali i při následné klinické kontrole. Obě metody – stanovení protilátek anti-tTG IgA v krvi i GIP ve stolici pomocí protilátky G12 – byly hodnoceny pomocí ELISA testu. Hodnoty jsme porovnali co do vztahu k příslušným horním hranicím normy. Výsledky: Studie se zúčastnilo 29 dětí (18 dívek) ve věku 2–15 let. U všech byly vstupní hodnoty GIP nad normu 0,15 µg/g (průměr 4,21; medián 3,29; standardní odchylka [SD] 3,7). Při kontrolním vyšetření (průměrně 4 měsíce od zahájení diety) byly koncentrace GIP u všech dětí až na tři (10,3 %) pod normu (průměr 0,29; medián 0,12; SD 0,73). V případě anti-tTG IgA byla jejich hodnota před zahájením diety průměrně 164 U/ml, s mediánem 195, SD 49, při horní hranici normy 9,9 U/ml. Při kontrolním odběru byly hodnoty anti-tTG IgA u všech dětí až na jedno nižší, ale pouze u deseti z nich (34,5 %) byly hodnoty v normě (průměr 27,9; medián 12,0; SD 38,9). Všechny děti deklarovaly striktní dodržování bezlepkové diety. Diskuze: Podle hodnocení koncentrace GIP ve stolici je adherence dětí s nově diagnostikovanou celiakií k bezlepkové dietě velmi dobrá, lepší než běžně literárně udávaná. Závěr: Hodnocení GIP ve stolici může být citlivějším ukazatelem dodržování bezlepkové diety zejména v prvních měsících od stanovaní diagnózy než anti-tTG IgA, u kterých je popsán výrazně pomalejší pokles do normy po zahájení bezlepkové diety.
Klíčová slova
lepek, imunogenní peptidy, celiakie, compliance
Úvod
Celiakie je autoimunitní onemocnění vyvolané konzumací lepku a příbuzných prolaminů u geneticky predisponovaných jedinců [1]. Je charakterizováno kombinací enteropatie, pozitivity specifických autoprotilátek, haplotypů HLA-DQ2 či HLA-DQ8 a různě vyjádřených klinických projevů závisejících na požití lepku [2], s prevalencí okolo 1 % [3]. Významnou roli v diagnostice i sledování pacientů s celiakií v dětském věku hrají autoprotilátky, zejména protilátky proti tkáňové transglutamináze ve třídě IgA (anti-tTG IgA). Normální hodnoty těchto protilátek (s výjimkou IgA deficitu a dříve zahájené bezlepkové diety) dokonce činí celiakii velmi nepravděpodobnou. Od roku 2020 připouští Evropská společnost pro dětskou gastroenterologii, hepatologii a výživu (ESPGHAN – European Society for Pediatric Gastroenterology, Hepatology and Nutrition) diagnostiku celiakie postavenou výhradně na hodnotě autoprotilátek, když při hodnotě anti-tTG IgA nad desetinásobek normy a pozitivitě protilátek proti endomysiu ve třídě IgA (anti-EMA IgA) v druhém odběru se má celiakie za prokázanou bez ohledu na případné klinické obtíže, bez nutnosti doplnění genetického vyšetření HLA-DQ2/8 haplotypů a v neposlední řadě enterobiopsie [4].
Sledování compliance s bezlepkovou dietou je jednou z nejdůležitějších součástí lékařských kontrol u dětí s celiakií. Komplikace neléčené celiakie mohou být četné a vážné [5]. Děti i jejich rodiče jsou v čase stanovení diagnózy o těchto rizicích poučeni, přesto je nutné při kontrolách možné obtíže připomínat, a to především v dětském věku ze dvou základních důvodů. Jednak je známo, že zejména ve věkové skupině adolescentů je adherence k bezlepkové dietě nižší než u ostatních věkových skupin [6], a jednak je celiakie v dětském věku z větší části než u dospělých stanovena i bez přítomných závažných klinických projevů (nejčastěji na základě screeningu rodinných příslušníků či v rámci „náhodného“ záchytu, kdy se vyšetření celkového IgA a anti-tTG IgA stalo v posledních letech součástí „běžného“ laboratorního vyšetření v alergologických či pediatrických ambulancí [7,8]).
Doposud bylo zlatým standardem monitorace dodržování bezlepkové diety stanovení autoprotilátek v krvi, u pacientů s normálními hodnotami celkového IgA to byly zejména anti-tTG IgA. Přestože protilátky ve třídě IgA mají tendenci klesat dříve než protilátky ve třídě IgG, které mohou přetrvávat i roky od zahájení diety, nejsou zejména v počátcích diety optimálním markerem compliance, protože k normalizaci těchto protilátek dochází průměrně okolo 9 měsíců od zahájení diety [9].
Nová metoda stanovení lepku ve stolici detekcí z lepku odvozených imunogenních peptidů (GIP – gluten-related immunogenic peptides) pomocí monoklonální protilátky G12 umožní ověřit obsah lepku ve stravě bez nutnosti sledování protilátkové odpovědi [10]. GIP jsou fragmenty lepkových proteinů, které jsou rezistentní vůči aktivitě peptidáz a vyvolávají imunitní reakci u pacientů s celiakií. Nejvíce imunogenním peptidem je 33merní peptid pocházející z alfa-gliadinu, který reaguje na monoklonální protilátku G12. Odolnost glutenových peptidů včetně imunogenního 33merního peptidu vůči štěpení v gastrointestinálním traktu zajišťuje, že významná část těchto peptidů je vylučována stolicí. Získání měřitelných množství imunogenní frakce lepku ve stolici tedy ukazuje na množství požitého lepku. Přítomnost GIP ve stolici představuje vysoce užitečný a přímý marker pro přesnou krátkodobou a dlouhodobou kontrolu bezlepkové diety [11].
V naší studii jsme chtěli ověřit hypotézu, že stanovení GIP ve stolici je citlivějším markerem compliance v úvodu dodržování bezlepkové diety než monitorování autoprotilátek, např. anti-tTG IgA.
Soubor pacientů a metodika
Vyšetřené děti
Všechny děti, kterým byla v gastroenterologické ambulanci Pediatrické kliniky 1. lékařské fakulty Univerzity Karlovy a Fakultní Thomayerovy nemocnice mezi květnem 2018 a květnem 2020 diagnostikována celiakie, byly pozvány k účasti ve studii. Podmínkou účasti byla běžná dieta před odběrem prvního vzorku stolice a podepsání informovaného souhlasu. Poprvé do gastroenterologické ambulance přicházely děti nikoli s průkazem, ale s podezřením na celiakii. Účast na studii byla nabídnuta všem dětem s vysokým podezřením na toto onemocnění už v rámci probíhajícího vyšetření tak, aby bylo zaručeno, že odběr prvního vzorku stolice proběhne ještě na běžné dietě. V případě, kdy u dítěte nebyla celiakie prokázána, jsme vzorek stolice přesto vyhodnotili a využili jako pozitivní kontrolu (není předmětem tohoto sdělení). Ke kontrolnímu vyšetření děti přicházely již se vzorkem stolice, který od odběru (nejdéle týden, zpravidla 1–2 dny) uchovávaly v lednici. V rámci této studie jsme nebrali ohled na metodu, kterou byla celiakie diagnostikována (biopsy vs. non-biopsy) [4] či indikaci k vyšetření, ať už to byla široká škála symptomů, „náhodný nález“ při laboratorním vyšetření, či screening v rámci asociovaných chorob či při pozitivní rodinné anamnéze bez symptomů typických pro celiakii.
Anti-tTG IgA
Vyšetření určená pro detekci anti-tTG IgA se v tomto případě provádí sérologicky na plně automatizovaném klinickém analyzátoru Alegria ELISA výrobce Orgentec Diagnostika GmbH. Tento přístroj slouží k analýze vzorků pomocí ELISA stripů, jedná se o CE-IVD systém. Metoda je založena na nepřímém ELISA testu.
Interpretace výsledků anti-tTG IgA:
- negativní ≤ 9,9 U/ml,
- pozitivní > 9,9 U/ml.
Rozsah stanovení protilátek je 0 až 200 U/ml. Výrobcem udávaná specificita, resp. senzitivita testu je 96,7 % a 100 %. Odběr vzorku proběhl v gastroenterologické ambulanci a týž den byl odeslán do imunologické laboratoře, kde byl zpracován podle správné laboratorní praxe.
GIP ve stolici
Vyšetření GIP ve stolici bylo provedeno pomocí komerční soupravy iVYLISA GIP STOOL od firmy Biomedal S. L. Jedná se o sendvičovou ELISA metodu, která umožňuje detekci a kvantifikaci glutenových imunogenních peptidů (příbuzných 33mer peptidu) ve vzorcích stolice. Během testu je vzorek přidán na vícejamkovou destičku potaženou monoklonální protilátkou G12, která specificky rozpoznává nejvíce imunotoxickou frakci lepku. Po promývacím kroku se přidá protilátka G12 konjugovaná s peroxidázou (HRP – horseradish peroxidase), čímž se získá měřitelný signál. Jedná se o tzv. direct, tedy přímou metodu, ve které platí pravidlo: čím vyšší je množství GIP přítomné ve vzorku, tím silnější bude signál. To spolu s extrémně vysokou specificitou a senzitivitou umožňuje této metodě přesně kvantifikovat GIP přítomný ve vzorcích stolice.
Metoda je navíc snadno škálovatelná a automatizovatelná:
- > 0,3 µg/g – pozitivní,
- > 0,15 µg/g, ale < 0,3 µg/g – slabě pozitivní,
- ≤ 0,15 µg/g – negativní.
Výrobcem udávaná specificita a senzitivita testů je 100 %, resp. 98,5 %.
Podrobněji k eluátu – při jeho přípravě musí vzorky stolice projít extrakčním procesem, aby byly toxické glutenové peptidy přístupné pro následnou analýzu. Nejprve je třeba vzorky stolic zcela rozmrazit. Vzorky stolice řádně homogenizujeme. Nesprávná homogenizace by mohla způsobit variabilitu v replikátech ze stejného vzorku. Do zkumavky se naváží 0,2–0,5 g jednotlivého vzorku stolice. Je třeba se vyvarovat překročení 0,5 g, protože dodané roztoky představují přesné množství potřebné pro analýzu 40 duplikovaných vzorků až do 0,5 g jednotlivého vzorku stolice. Poté se přidá potřebné množství extrakčního roztoku, které je dáno následujícím vzorcem:
Objem extrakčního roztoku (ml) = 9 × hmotnost naváženého vzorku stolice (g), Objem = 9 × 0,4 g (odvážený vzorek stolice) = 3,6 ml extrakčního roztoku.
Následuje prudké promíchání pomocí vortexu či podobného zařízení, aby se vzorek rozpustil. Míchání by mělo pokračovat, dokud na stěnách extrakční zkumavky není žádný kus vzorku stolice. Inkubace vzorku při 50 °C ve vodní lázni s regulovanou teplotou po dobu 60 min včetně pravidelného míchání vzorku (každých 15 min) převrácením či za použití vortexu po dobu 10 s. Suspenzi následně odstředíme při 2 500 g po dobu 10 min a supernatant přeneseme do čisté zkumavky. Po tomto postupu by měly být vzorky stolice analyzovány co nejdříve. Máme vyzkoušeno, že v chladu jsou vzorky stabilní maximálně do 24 hod, po zmražení do –20 °C vydrží i několik týdnů. Doporučuje se však analyzovat ihned.
V preanalytické fázi byli pacienti a jejich zákonní zástupci poučeni, že vzorek je nutné odebrat v nejkratším možném termínu před ambulantní kontrolou, maximálně však 7 dní, a do odevzdání vzorku u nás na ambulanci je nutné vzorek uchovat v lednici. Po obdržení vzorku jsme ihned odeslali do imunologické laboratoře ke zmrazení na –20 °C, kde vzorek zůstal do zpracování výsledku, maximálně však 6 měsíců.
Statistická analýza
Data souboru byla zpracovávána programy MS Excel 365, IBM SPSS version 21 a kalkulátory na stránce https: //scistatcalc.blogspot.com/. K posouzení významnosti poklesu hodnot GIP ve stolici a anti-tTG IgA v krvi byl použit McNemarův test. K porovnání procent poklesu GIP ve stolici a tTG IgA v krvi do normálních hodnot byl použit test významnosti rozdílů dvou proporcí.
Etické aspekty
Zákonní zástupci všech účastníků studie podepsali informované souhlasy, případně také děti samotné, v závislosti na jejich věku. Pro děti na prvním stupni základní školy byl připraven informovaný souhlas pro „menší děti“, pro děti od 2. stupně základní školy výše potom informovaný souhlas pro „větší děti“. Studii schválila etická komise Fakultní Thomayerovy nemocnice a Institutu klinické a experimentální medicíny.
Výsledky
Podmínky pro účast v prospektivní studii splnilo celkem 29 nově diagnostikovaných dětí s celiakií, z toho bylo 18 (62 %) dívek. Děti byly ve věkovém rozmezí 2–15 let, průměrně 8,2 let, kdy u dívek byl věkový průměr 7,7 let a u chlapců 8,8 let.
U všech dětí (100 %) byly vstupní hodnoty GIP, tedy před zahájením bezlepkové diety, nad normu 0,15 µg/g, průměrně 4,21 µg/g, s mediánem 3,29 µg/g a standardní odchylkou (SD) 3,7 µg/g. U většiny dětí byly hodnoty jasně pozitivní, jen u tří dětí byl obsah GIP ve stolici v zóně „slabé pozitivity“ od 0,16 do 0,30 µg/g. Při kontrolním vyšetření průměrně 4 měsíce od zahájení diety (SD 1,28 měsíce) byly koncentrace GIP u všech dětí až na tři (10,3 %) pod normu (průměr 0,29; medián 0,12; SD 0,73). Dle McNemarova testu se jedná o signifikantní rozdíl (p < 0,0001). U jednoho z těchto dětí byla koncentrace lepku v pásmu slabé pozitivity do 0,3 µg/g. U dvou dětí byla koncentrace lepku významně zvýšená a u jednoho z těchto dětí byla hodnota dokonce vyšší než hodnota vstupní (1,7 vs. 4,0 µg/g).
V případě anti-tTG IgA protilátek byla jejich hodnota před zahájením diety také u všech dětí (100 %) nad normu (9,9 U/ml), průměrně 164 U/ml, s mediánem 195 U/ml a SD 49 U/ml. Při kontrolním odběru byly hodnoty anti-tTG IgA u všech dětí až na jedno nižší, ale pouze u 10 z nich (34,5 %) byly hodnoty v normě (průměr 27,9; medián 12,0; SD 38,9 U/ml), rozdíl opět dle McNemarova testu signifikantní (p = 0,002) (graf 1).
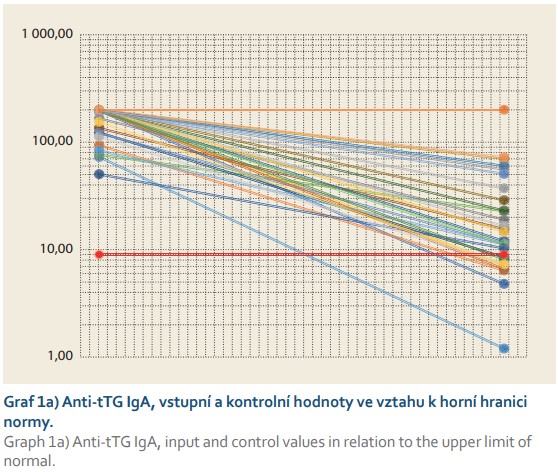
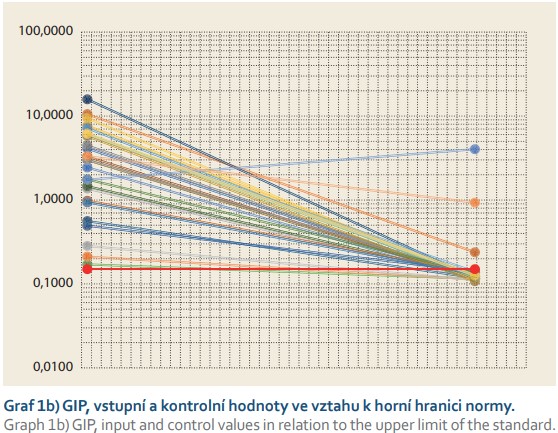
Pokles GIP ve stolici do normy (89,7 %) při kontrolním vyšetření byl významně větší než u anti-tTG IgA (34,5 %) (p < 0,001).
Všechny děti a jejich zákonní zástupci deklarovali striktní dodržování bezlepkové diety v posledních 4 týdnech před kontrolním vyšetřením.
Diskuze
V naší studii jsme se zaměřili na monitoraci dodržování bezlepkové diety v úvodních fázích onemocnění, kdy si děti a jejich rodiny postupně zvykají nejen na novou dietu, ale na zcela nový režim, kdy kromě nových stravovacích návyků musí zvládnout nové společenské výzvy [12]. Termín kontrolního vyšetření jsme stanovili na 4 měsíce od zahájení bezlepkové diety, kdy je předpoklad, že se děti již naučily správně bezlepkovou dietu dodržovat. Přestože jsme v průměru 4měsíčního intervalu dosáhli, SD času sběru stolice 1,28 měsíce ukazuje, že rozptyl času odběrů byl poměrně velký, což skýtá prostor pro možnou chybu, a to je potřeba mít na paměti při interpretaci výsledků. Důvodů je celá řada od žádosti rodiny k odložení termínu vyšetření pro kolizi s jinými závazky přes žádost o dřívější kontrolu z důvodů konzultace ohledně diety či zdravotního stavu po komplikace způsobené pandemií virem SARS-CoV-2, kdy se rušila odložitelná vyšetření. Zatímco u protilátek anti-tTG IgA je známo, že se normalizují v průměru po 9 měsících od zahájení bezlepkové diety [9], u GIP ve stolici je předpoklad, že by se v řádu dnů od zahájení striktní bezlepkové diety měla jejich koncentrace snížit do negativního pásma detekce [13], což je ale zároveň jedna z hlavních nevýhod testu, který je tak schopen zastihnout pouze recentní porušení diety.
Práce porovnávající stanovení GIP ve stolici a „zlatý standard“ monitorace dodržování bezlepkové diety u celiaků pomocí anti-tTG IgA protilátek v krvi se začaly objevovat v posledních letech. Vesměs poukazují na výhody nové metody v porovnání se sérologickým vyšetřením, např. v situacích náhlého zhoršení zdravotního stavu na podkladě jednorázového výrazného porušení diety [14]. Konstatují, že vyšetření GIP ve stolici je citlivým ukazatelem compliance, citlivějším než klinické vyšetření, dotazníky adherence k dietě či vyšetření autoprotilátek v krvi [15]. Spíše než jako náhradu sérologického testování doporučují vyšetření GIP ve stolici jako jeho doplněk [13], byť uvádějí také limitace této nové metody, např. nízkou senzitivitu ve vztahu k endoskopicky verifikovanému slizničnímu hojení [16]. Naše výsledky odpovídají závěrům výše zmíněných prací, byť se žádná nevěnovala specificky sledování pacientů na začátcích jejich diety. Jak bylo zmíněno, po 4 měsících bylo možno očekávat již úplnou negativitu GIP ve stolici, u našich pacientů byla negativita při použití striktnější normy ≤ 0,15 µg/g 89,7 %, což odpovídá datům o compliance v nejnižších věkových kategoriích, tj. 1–3 roky věku. Vzhledem k tomu, že věkový průměr našeho souboru byl 8,2 let, bylo možno dle dostupných prací očekávat compliance pouze okolo 70 % [14,17]. Postupného poklesu anti-tTG IgA dosáhlo 34,5 % dětí, většina z nich však nikoli do normy po 4 měsících od zahájení diety, což odpovídá dostupné literatuře [9].
Velký rozptyl hodnot GIP při vstupním vyšetření může odpovídat aktuální náloži lepku ve stravě dětí a souvisí mimo jiné s výše zmíněnou krátkou dobou detekovatelnosti. Vstupní hodnoty v pásmu slabé pozitivity u třech našich dětí si vysvětlujeme omezením lepku ve stravě ještě před definitivním potvrzením diagnózy, k čemuž mohou mít někteří lidé sklony i přes upozornění, že předčasné zahájení diety může stanovení diagnózy celiakie zkomplikovat.
Závěr
Z hlediska koncentrace GIP ve stolici je dodržování bezlepkové diety ve skupině našich dětí s nově diagnostikovanou celiakií velmi dobré.
Hodnocení GIP ve stolici může být citlivějším ukazatelem dodržování bezlepkové diety než anti-tTG IgA, zejména v úvodních měsících od stanovaní diagnózy, kdy vzhledem k popsanému výrazně pomalejšímu poklesu do normy nemůžeme u anti-tTG IgA ani při striktním dodržování bezlepkové diety čekat negativní výsledek.
Vyšetření GIP ve stolici je citlivějším markerem compliance s dietou než informace od samotných pacientů, toto vyšetření by tak bylo možno využít k vytipování subpopulace dětí a jejich rodin, které potřebují větší pomoc se správným dodržováním bezlepkové diety.
ORCID autorů
R. Vyhnánek ORCID 0000-0001-7796-4201,
Z. Khaznadar ORCID 0000-0002-8273-7369,
R. Vyhnánek ORCID 0000-0003-2353-6871.
Doručeno/Submitted: 23. 9. 2021
Přijato/Accepted: 31. 10. 2021
MUDr. Radim Vyhnánek
Pediatrická klinika
1. LF UK a Fakultní Thomayerova nemocnice
Vídeňská 800
140 59 Praha 4
radim.vyhnanek@ftn.cz
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Kubina M, Čierna I, Székyová D et al. Niektoré genetické determinanty celiakie, význam HLA typizácie v klinickej praxi a zastúpenie HLA-DQ haplotypov v súbore 306 detských pacientov. Gastroent Hepatol 2016; 70(6): 475–479. doi: 10.14735/amgh2016475.
2. Husby S, Koletzko S, Korponay-Szabó IR et al. European society for pediatric gastroenterology, hepatology, and nutrition guidelines for the diagnosis of coeliac disease. J Pediatr Gastroenterol Nutr 2012; 54(1): 136–160. doi: 10.1097/MPG.0b013e31821a23d0.
3. Singh P, Arora A, Strand TA et al. Global prevalence of celiac disease: systematic review and meta-analysis. Clin Gastroenterol Hepatol 2018; 16(6): 823–836.e2. doi: 10.1016/j.cgh.2017.06.037.
4. Husby S, Koletzko S, Korponay-Szabó I et al. European society paediatric gastroenterology, hepatology and nutrition guidelines for diagnosing coeliac disease 2020. J Pediatr Gastroenterol Nutr 2020; 70(1): 141–156. doi: 10.1097/MPG.0000000000002497.
5. Šibíková M, David J, Lhotská J et al. Závažný průběh celiakie, Čes-slov Pediat 2019; 74(5): 275–279.
6. Czaja-Bulsa G, Bulsa M. Adherence to gluten-free diet in children with celiac disease. Nutrients 2018; 10(10): 1424. doi: 10.3390/nu10101424.
7. Lebwohl B, Rubio-Tapia A. Epidemiology, presentation, and diagnosis of celiac disease. Gastroenterology 2021; 160(1): 63–75. doi: 10.1053/j.gastro.2020.06.098.
8. Chvátalová T, Vepřeková G, Houska H et al. Celiac disease – a missed diagnosis. Vnitr Lek 2012; 58(2): 99–103.
9. Sbravati F, Cosentino A, Lenzi J et al. Anti tissue transglutaminase antibodies‘ normalization after starting a gluten-free diet in a large population of celiac children-a real-life experience. Dig Liver Dis 2021. doi: 10.1016/j.dld.2021.06.026.
10. Comino I, Fernández-Bañares F, Esteve M et al. Fecal gluten peptides reveal limitations of serological tests and food questionnaires for monitoring gluten-free diet in celiac disease patients. Am J Gastroenterol 2016; 111(10): 1456–1465. doi: 10.1038/ajg.2016.439.
11. Morón B, Bethune MT, Comino I et al. Toward the assessment of food toxicity for celiac patients: characterization of monoclonal antibodies to a main immunogenic gluten peptide. PLoS One 2008; 3(5): e2294. doi: 10.1371/journal.pone.0002294.
12. Silvester JA, Weiten D, Graff LA et al. Living gluten-free: adherence, knowledge, lifestyle adaptations and feelings towards a gluten-free diet. J Hum Nutr Diet 2016; 29(3): 374–382. doi: 10.1111/jhn.12316.
13. Comino I, Real A, Vivas S et al. Monitoring of gluten-free diet compliance in celiac patients by assessment of gliadin 33-mer equivalent epitopes in feces. Am J Clin Nutr 2012; 95(3): 670–677. doi: 10.3945/ajcn.111.026708.
14. Moreno ML, Rodríguez-Herrera A, Sousa C et al. Biomarkers to monitor gluten-free diet compliance in celiac patients. Nutrients 2017; 9(1): 46. doi: 10.3390/nu9010046.
15. Porcelli B, Ferretti F, Biviano I et al. Testing for fecal gluten immunogenic peptides: a useful tool to evaluate compliance with gluten-free diet by celiacs. Ann Gastroenterol 2020; 33(6): 631–637. doi: 10.20524/aog.2020.0530.
16. Laserna-Mendieta EJ, Casanova MJ, Arias Á et al. Poor sensitivity of fecal gluten immunogenic peptides and serum antibodies to detect duodenal mucosal damage in celiac disease monitoring. Nutrients 2020; 13(1): 98. doi: 10.3390/nu13010098.
17. Frühauf P, Bronský J, Dědek P et al. Celiakie – doporučený postup pro diagnostiku a terapii u dětí a dospívajících. Čes-slov Pediat 2016; 71(3): 175–183.