Roboticky asistovaná léčba zhoubných nádorů kolorekta a hepatopankreatobiliární oblasti
Daniel Langer Orcid.org 1, Michal Vočka Orcid.org 2, Jaroslav Kalvach3, Jaroslav Pažin1, Miroslav Ryska3, Radek Pohnán Orcid.org 3
+ Pracoviště
Souhrn
Úvod: Česká republika patří mezi státy významně zatížené zhoubnými nádory. I přes řadu změn zavedených do léčby gastrointestinálních malignit zaujímá radikální odstranění nádoru v multimodálním terapeutickém procesu klíčové postavení, které je v současnosti nezastupitelné. Počátkem třetího tisíciletí byla miniinvazivní chirurgická léčba abdominálních novotvarů postupně rozšiřována o roboticky asistované výkony. Cílem sdělení je hodnocení přínosu robotické chirurgie v léčbě malignit kolorekta a hepatopankreatobiliární (HPB) oblasti a prezentace vlastních výsledků nerandomizované studie roboticky asistované léčby karcinomu rekta (KR). Materiál a metoda: Autoři sumarizují literárně dostupné studie srovnávající výsledky roboticky asistovaných a laparoskopických operací pro onkologická onemocnění kolorekta a HPB oblasti ze světových databází (PubMed, EMBASE, Medline a Cochrane Library) a prezentují vlastní výsledky nerandomizované studie. Soubor je tvořen 204 nemocnými s KR (< 15 cm od análního otvoru), kteří na našem pracovišti v období od 1. 1. 2016 do 31. 12. 2020 podstoupili roboticky asistovanou léčbu. Všechny demografické, klinické a onkologické údaje byly prospektivně získávány a analyzovány. Získaná data byla zpracována deskriptivními statistickými metodami. Výsledky: Během 5letého období podstoupilo na našem pracovišti robotickou operaci 204 nemocných s KR, 138 mužů a 66 žen. V 97 (47,5 %) případech bylo onemocnění diagnostikováno v pokročilém stadiu (III. a IV. stadium TNM klasifikace). Synchronní jaterní metastázy byly přítomny u 18 pacientů a ve dvou případech byly s KR diagnostikovány sekundarity plicní. K primární operační léčbě jaterních sekundarit bylo přistoupeno u osmi (44,4 %) nemocných a ve dvou případech byla jaterní ložiska radikálně odstraněna současně s primárním novotvarem. U 136 nemocných byl extraperitoneálně uložený novotvar ošetřen ve smyslu totální mezorektální excize a v 68 případech byla provedena parciální mezorektální excize. V celém souboru bylo zaznamenáno 18 komplikací. V pěti (3,6 %) případech se vyskytla porucha hojení anastomózy, která se klinicky manifestovala a vynutila si léčebnou intervenci. Jeden nemocný zemřel v souvislosti s dekompenzací chronického toxonutritivního onemocnění jater. Lokální recidiva, která byla v rámci dispenzarizace zaznamenána u šesti nemocných, byla v polovině případů radikálně odstraněna. Závěr: Klíčové postavení v léčbě kolorektálních a HPB novotvarů zaujímá léčba chirurgická, která v multimodálním terapeutickém algoritmu představuje jedinou potenciálně kurativní metodu. Roboticky asistovaná léčba malignit kolorekta a HPB oblasti se stala rutinní terapeutickou modalitou, která je frekventně využívána v celosvětovém měřítku. Na pracovišti autorů, obdobně jako v některých zahraničních centrech, v chirurgické léčbě KR dominují da Vinci asistované operace. Ve srovnání s otevřenými a laparoskopickými resekcemi KR dosahují roboticky asistované operace obdobných klinických a onkologických výsledků při nižší četnosti komplikací.
Klíčová slova
kolorektální karcinom, karcinom pankreatu, robotická chirurgie, jaterní malignity
Úvod
Česká republika patří mezi státy významně zatížené zhoubnými nádory. Gastrointestinální malignity, resp. zhoubné nádory kolorekta a HPB oblasti velmi významně přispívají k celkové onkologické zátěži české populace. Současná léčba zhoubného onemocnění kolorekta a HPB oblasti vyžaduje interdisciplinární spolupráci. Klíčové postavení v multimodální terapii zaujímá radikální odstranění nádorem postižených tkání, které v současnosti nelze ekvivalentně nahradit. Počátkem třetího tisíciletí byla miniinvazivní chirurgická léčba abdominálních novotvarů postupně rozšiřována o roboticky asistované výkony. Cílem sdělení je hodnocení přínosu robotické chirurgie v léčbě malignit kolorekta a HPB oblasti a prezentace vlastních výsledků nerandomizované studie roboticky asistované léčby karcinomu rekta.
Materiál a metoda
První zkušenosti s robotickou asistencí u resekcí tračníku (pro benigní onemocnění) byly publikovány Weberem et al v roce 2002 [1]. Následně uveřejněné práce hodnotily bezpečnost a proveditelnost robotických kolorektálních výkonů, výhody a nevýhody robotického systému [2]. Pilotní randomizovanou kontrolovanou studii srovnávající laparoskopické a robotické provedení totální mezorektální excize (TME) u nemocných s karcinomem rekta publikovali v roce 2008 Baik et al [3]. Porovnávanými hodnotami byly klinické i onkologické parametry, které nevykazovaly signifikantní rozdíl u sledovaných skupin. V roce 2011 byly publikovány výsledky projektu srovnávající robotické a laparoskopické provedení TME při operační léčbě karcinomu rekta [4]. Klinické i onkologické výsledky byly u obou skupin srovnatelné. Finální ekonomická zátěž byla (statisticky nevýznamně) vyšší u robotické skupiny operantů. Kim et al prezentovali randomizovanou kontrolovanou studii (RCT) se srovnatelnými klinickými, onkologickými i funkčními výsledky operační léčby nemocných s rektálním karcinomem uskutečněné laparoskopickou a robotickou technikou [5]. Metaanalýza randomizovaných kontrolovaných studií potvrdila nižší četnost konverzí na výkon otevřený a delší operační dobu ve skupině nemocných s karcinomem rekta (KR) ošetřených pomocí robotického systému ve srovnání s laparoskopickým souborem [6]. Mezinárodní multicentrická prospektivní randomizovaná kontrolovaná studie ROLARR srovnávající laparoskopickou a robotickou léčbu KR prokázala nižší počet konverzí a pozitivních cirkumferentních resekčních okrajů u robotické skupiny, i když výsledek nebyl statisticky významný. V ostatních parametrech byly výsledky srovnatelné v robotickém i laparoskopickém souboru. Významnou limitací této robustní práce byl nepoměr v operačních zkušenostech v neprospěch robotických chirurgů [7]. V písemnictví byly v souvislosti s léčbou KR uveřejněny práce potvrzující lepší klinické i funkční ukazatele po robotických operacích ve srovnání s výkony laparoskopickými [8–10]. Recentní metaanalýza (obsahující nerandomizované studie) potvrdila potenciální benefit a příznivější výsledky funkčních parametrů po robotických operacích než u nemocných po výkonech laparoskopických [11]. Na některých pracovištích jsou robotické systémy využívány při transanálních resekcích rekta (TaTME) [12].
Některé práce dokládají srovnatelné [13] nebo mírně optimističtější krátkodobé výsledky (méně konverzí a komplikací, vyšší počty získaných mízních uzlin, nižší krevní ztrátu, kratší dobu hospitalizace) po robotické pravostranné hemikolektomii pro malignitu ve srovnání s laparoskopickou technikou [14,15]. Dlouhodobé výsledky sledovaných ukazatelů jsou u obou technik obdobné [16,17]. Systematický literární přehled obsahující 15 prací (14 retrospektivních a 1 RCT) posuzujících více než 4 000 případů robotické a laparoskopické pravostranné resekce tračníku deklaruje v robotické skupině příznivější výsledky – nižší četnost poruchy hojení anastomózy, vyšší počet získaných mízních uzlin, nižší frekvenci konverzí a incizionálních hernií a kratší dobu hospitalizace [18]. V písemnictví byly prezentovány srovnatelné nebo mírně lepší výsledky roboticky asistované operační léčby nádorů lokalizovaných v levé části tračníku ve srovnání s laparoskopickými výkony, i když literární zmínky jsou relativně chudé [19,20].
Evoluce robotické chirurgie byla zaznamenána i v HPB oblasti. V roce 2009 byla publikována práce Patritiho et al [21], která referovala o jednodobém ošetření nemocných s metastazujícím kolorektálním karcinomem. Skupina sedmi pacientů podstoupila laparoskopickou resekci kolorekta (pro primární novotvar) se simultánním miniinvazivním (laparoskopickým či robotickým) ošetřením synchronních jaterních metastáz (bisegmentektomie, segmentektomie, metastasektomie nebo radiofrekvenční ablace (RFA)). Prospektivní studie srovnávající robotickou a laparoskopickou jaterní resekci pro nádorová ložiska byla prezentována v roce 2010 [22]. Během jednoho roku bylo do projektu zařazeno 32 nemocných s periferně lokalizovanou (primární či sekundární) jaterní malignitou (kolorektální sekundarity, hepatocelulární karcinom (HCC) a jiné), jejíž průměr nepřesahoval 5 cm. Perioperační i onkologické výsledky byly u obou skupin selektovaných nemocných obdobné. V roce 2011 byl otištěn článek [23], ve kterém byly prezentovány výsledky 70 robotických resekcí jater, které autoři provedli na dvou pracovištích (Itálie, USA). U 60 % operovaných se jednalo o zhoubná onemocnění. Velké jaterní resekce (≥ 3 jaterní segmenty) byly provedeny ve 27 (38,5 %) případech (4 konverze na výkon otevřený). Pooperační komplikace byly pozorovány u 21 % pacientů a byly léčeny konzervativně. Z prezentovaného souboru žádný pacient nezemřel. Jihokorejští autoři uveřejnili práci hodnotící robotické resekce jater u 30 po sobě jdoucích pacientů [24]. V 21 případech byla indikací k operaci malignita (13krát HCC). Pravá či levá hepatektomie byla provedena u 20 (66,7 %) pacientů (2 konverze na výkon otevřený). Komplikace byly zaznamenány u 43,3 % případů (2krát biliární leak). Rekurence choroby u nemocných s HCC během dispenzárních 11 měsíců zjištěna nebyla. Bezpečnost roboticky asistované (velké) resekce jater byla demonstrována literární zmínkou o využití da Vinci systému při příbuzenské transplantaci jater [25]. Recentní metaanalýza obsahující data šesti retrospektivních studií srovnávajících výsledky u 1 093 nemocných, kteří podstoupili robotickou nebo laparoskopickou operaci jater pro zhoubné onemocnění, potvrdila u robotického souboru vyšší podíl pravostranných hepatektomií, větší velikost nádorových lézí, nižší frekvenci konverzních operací při delším operačním čase [26]. V roce 2010 byla publikována práce prezentující výsledky roboticky asistované léčby u pacientů s onemocněním pankreatu [27]. Ze 134 nemocných byla pro nádorové onemocnění operována téměř polovina (47,8 %). Operace byly provedeny na dvou pracovištích (Itálie, USA) v období 2000–2009 jedním chirurgem, resp. autorem. Ve škále operačních výkonů dominovaly operace resekční (pankreatoduodenektomie 60krát, levostranná pankreatektomie 46krát). Publikované výsledky byly srovnatelné se závěry prací hodnotících léčbu z laparotomického přístupu. O rok později byla Buchsem et al prezentována studie srovnávající výsledky roboticky asistované a otevřené pankreatoduodenektomie na jednom pracovišti [28]. U robotické skupiny byl ve srovnání se skupinou otevřenou kratší operační čas, nižší krevní ztráta a vyšší počet identifikovaných mízních uzlin z resekátu. Da Vinci systém byl využit u technicky obtížných operací pankreatu s vaskulární resekcí [29]. Celkem pět onkologicky nemocných (věkového rozmezí 52–74 let) podstoupilo roboticky asistovanou operaci pankreatu s cévní resekcí (2krát pankreatoduodenektomie s resekcí portální žíly, 3krát levostranná pankreatektomie s resekcí truncus coeliacus či portální žíly). Všechny výkony byly dokončeny miniinvazivní technikou. Krevní transfuze podány nebyly a 6 měsíců po operaci nebyla u čtyř (80 %) pacientů prokázána recidiva onemocnění. Výsledky 44 studií (3 462 nemocných), z nichž šest prací posuzuje robotické vs. laparoskopické provedení pankreatoduodenektomie, byly součástí metaanalýzy, ve které byla robotická technika spojena s nižší frekvencí konverze na otevřený výkon, s nižším počtem aplikovaných transfuzí a kratší dobou hospitalizace [30].
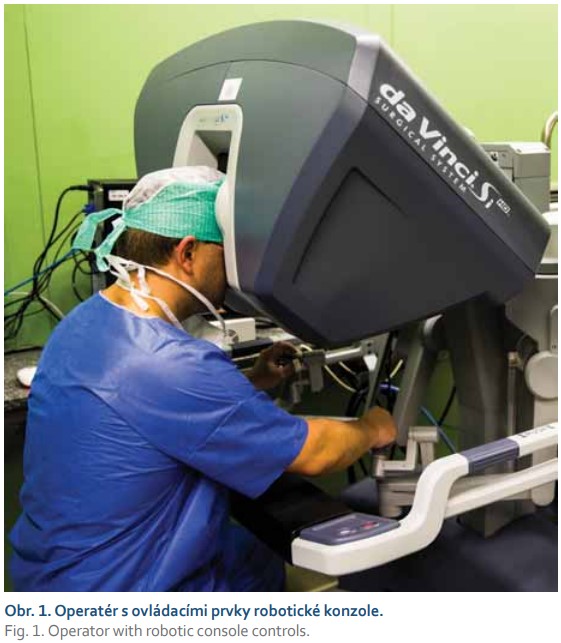
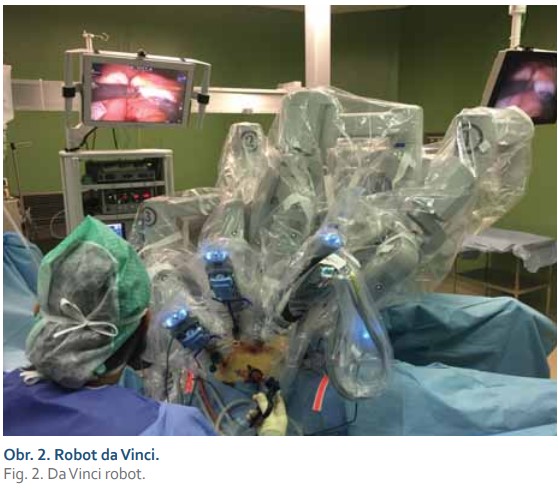
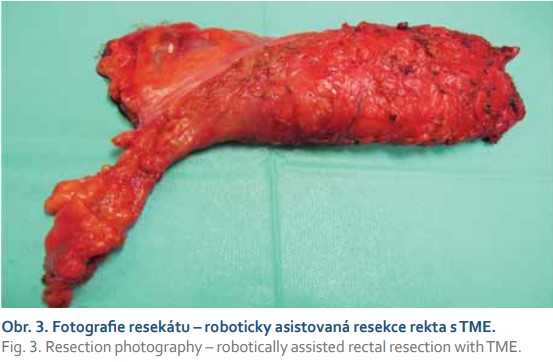
Soubor nerandomizované observační studie je tvořen 204 nemocnými s rektálním karcinomem (< 15 cm od análního otvoru), kteří na našem pracovišti v období od 1. 1. 2016 do 31. 12. 2020 podstoupili roboticky asistovanou léčbu. U všech nemocných bylo pečlivě stanoveno stadium onemocnění (staging) v rámci TNM klasifikace. Nedílnou součástí diagnostického algoritmu byla vyšetření zobrazovacími metodami (celotělové CT vyšetření a MR zobrazení pánve), jejichž výsledky byly zpracovány dle standardizovaného protokolu [31]. Léčebný postup u každého nemocného byl realizován na základě rozhodnutí multidisciplinárního týmu s ohledem na současné možnosti personalizované medicíny [32]. V souladu s doporučením ASCRS (American Society of Colorectal Surgeons) podstoupili všichni nemocní předoperační mechanickou střevní přípravu v kombinaci s perorálními antibiotiky [33]. Všichni pacienti podstoupili standardizovaný robotický operační výkon v souladu s metodikou Evropské akademie robotické kolorektální chirurgie (EARCS) [34]. Při operacích byl využíván robotický systém da Vinci Si® (Intuitive Surgical, Sunnyvale, CA, USA, obr. 1, 2) způsobem jediného přistavení („single docking“). U všech nemocných byla provedena mediolaterální disekce s vysokou nebo nízkou ligací dolní mezenterické tepny. Po dokončení mezorektální excize byla provedena transekce rekta staplerem. Tračník byl vyjmut z minilaparotomie. Kontinuita trávicího traktu byla obnovena primární end-to-end staplerovou anastomózou. Ve všech případech byl proveden air leak test. U nemocných s KR uloženým v orální třetině byla provedena parciální mezorektální excize (PME). TME byla nedílnou součástí operační léčby u extraperitoneálně lokalizovaných novotvarů. Po všech kontinentních výkonech s TME bylo plánováno provedení protektivní ileostomie. Před okluzí ileostomie byla u všech pacientů prováděna endoskopická kontrola kolorektální/koloanální anastomózy s posouzením integrity, stavu a průsvitu anastomózy, resp. s vyloučením možných píštělí a stenóz. Při abdominoperineálních resekcích byl preparát získáván z perineálního přístupu. Získané preparáty byly fotograficky dokumentovány (obr. 3) a nativně histopatologicky zpracovány dle Quirkeho protokolu [35]. U lokálně pokročilých extraperitoneálně uložených novotvarů byla primárně poskytována neoadjuvantní chemoradioterapie (CHRT) ve standardním režimu (LCRT – long-course chemoradiotherapy). Pakliže byl po 4 týdnech od ukončení neoadjuvantní CHRT vyšetřením magnetickou rezonancí prokázán pozitivní efekt CHRT, resp. radiosenzitivita, následoval operační výkon 8.–12. týden po ukončení CHRT. V opačném případě byla operace provedena 6. týden po neoadjuvanci. Neoadjuvantní krátký léčebný postup (SCRT – short-course radiotherapy) byl rezervován pro nemocné se synchronními jaterními sekundaritami nebo duplicitními malignitami a chirurgická léčba byla uskutečněna následně po ukončení SCRT. Po ukončení léčby byla u všech nemocných stanovena dispenzární péče. Všechny demografické, klinické a onkologické údaje byly prospektivně získávány a analyzovány. Získaná data jsme zpracovali deskriptivními statistickými metodami.
Výsledky
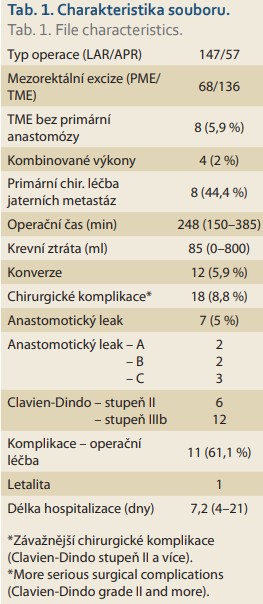
Během 5letého období od 1. 1. 2016 do 31. 12. 2020 podstoupilo na našem pracovišti robotickou operaci 204 nemocných s KR, 138 mužů a 66 žen (tab. 1). Průměrný věk souboru činil 63,8 let (32–85 let) a body mass index (BMI) 27,4 kg/m2 (17,3–46 kg/m2). Téměř u dvou třetin (64,7 %) nemocných byl novotvar lokalizován extraperitoneálně, resp. více než polovina (53,4 %) nádorů se nacházela v aborální třetině konečníku. V 97 (47,5 %) případech bylo onemocnění diagnostikováno v pokročilém stadiu (III. a IV. stadium TNM klasifikace). Synchronní jaterní metastázy byly přítomny u 18 pacientů a ve dvou případech byly s KR diagnostikovány sekundarity plicní. K primární operační léčbě jaterních sekundarit bylo přistoupeno u osmi (44,4 %) nemocných a ve dvou případech byla jaterní ložiska radikálně odstraněna současně s primárním novotvarem. Synchronní roboticky asistovaná léčba byla ve spolupráci s urology poskytnuta dvěma nemocným s KR a renální malignitou. Celkem 147 pacientů podstoupilo sfinkter zachovávající výkon. U 136 nemocných byl extraperitoneálně uložený novotvar ošetřen ve smyslu TME a v 68 případech byla provedena PME. U sedmi pacientů si nízká lokalizace tumoru vyžádala intersfinkterickou resekci. Neoadjuvantní protinádorovou terapii (CHRT) podstoupilo 79 (38,7 %) nemocných. Konvertovat a dokončit z laparotomického přístupu bylo nutno dvanáct (5,9 %) operací. Ke komplikovanému hojení anastomózy (anastomotický leak – AL) došlo u sedmi (5 %) nemocných. V pěti (3,6 %) případech se porucha hojení anastomózy klinicky manifestovala (AL – B, C) a vynutila si léčebnou intervenci (1× antibiotická léčba, 1× podtlaková terapie, 3× reoperace). Jeden nemocný zemřel v souvislosti s dekompenzací chronického toxonutritivního onemocnění jater. V sedmi (8,9 %) případech nebyla při histopatologickém zpracování preparátu malignita přítomna, resp. byla potvrzena kompletní patologická odpověď. Průměrná délka pooperační hospitalizace byla 7,2 dnů. Medián doby dispenzární péče činil 20 měsíců (průměr 23,2 měsíců). Lokální recidiva, která byla v rámci dispenzarizace zaznamenána u šesti (2,9 %) nemocných v průměrné době 9,8 měsíců od operační léčby, byla v polovině případů radikálně odstraněna.
Diskuze
Prognózu nemocného s kolorektální a HPB malignitou ovlivňuje hloubka nádorové invaze, počet tumorem postižených mízních uzlin, přítomnost vzdálených metastáz, resp. stadium choroby, léčba, její zahájení a kvalita [36]. Přesné stanovení pokročilosti zhoubného onemocnění je elementární podmínkou pro personalizovanou léčebnou strategii, která je stanovena na základě rozhodnutí multidisciplinárního týmu. Klíčové postavení v multimodální terapii zhoubných novotvarů kolorekta a HPB oblasti zaujímá operační léčba. Ve většině chirurgických oborů jsou preferovány miniinvazivní operační postupy i pro onkologická onemocnění. Robotizace laparoskopických výkonů postupně pronikla do jednotlivých chirurgických oborů a spektrum robotických operací se v krátkém období vyrovnalo škále laparoskopických výkonů. Roboticky asistovaná léčba, primárně využívaná pro benigní onemocnění, byla časně zařazena mezi léčebné modality malignit. Úvodní práce hodnotící bezpečnost a proveditelnost robotických kolorektálních výkonů a výhody a nevýhody robotického systému [37] byly následně doplněny randomizovanými kontrolovanými studiemi srovnávajícími klinické, onkologické a funkční výsledky operační léčby abdominálních malignit laparoskopickou a robotickou technikou.
Úvodní robotické operace na pracovišti autorů byly obdobné jako v zahraničních centrech [38]. Důvodem pomalejšího rozvoje miniinvazivního přístupu k jaterním resekcím (v poměru k miniinvazivní léčbě ostatních orgánů dutiny břišní) byly obavy spojené s rizikem masivního krvácení a plynové embolie [39]. V roce 2006, kdy v literatuře nebyly zkušenosti s robotickou jaterní chirurgií dostupné, autoři prezentovali své prvotní zkušenosti s roboticky asistovanými resekcemi jater [40]. V následujícím období nebylo možné robotickou jaterní chirurgii rozvíjet, jelikož tato léčebná modalita nebyla v ČR ze strany zdravotních pojišťoven hrazena. Plátcem zdravotní péče je garantována úhrada roboticky asistované léčby pouze u nemocných s KR. Na pracovišti autorů se v souladu s vývojem v zahraničních centrech podíl roboticky asistované terapie KR zvyšoval a v uvedeném 5letém období robotickou operaci podstoupila většina (více než dvě třetiny) nemocných s KR. Naše pracoviště se zařadilo mezi centra, která v léčbě KR rutinně využívají robotický systém da Vinci. Robotická technika umožnila v některých ukazatelích zlepšit klinické, onkologické i funkční výsledky a snížit výskyt komplikací včetně četnosti obávaného klinicky manifestního anastomotického leaku.
Závěr
Klíčové postavení v léčbě kolorektálních a HPB novotvarů zaujímá léčba chirurgická, která v multimodálním terapeutickém algoritmu představuje jedinou potenciálně kurativní metodu. Roboticky asistovaná léčba malignit kolorekta a HPB oblasti se stala rutinní terapeutickou modalitou, která je frekventně využívána v celosvětovém měřítku. Na pracovišti autorů, obdobně jako v některých zahraničních centrech, v chirurgické léčbě KR dominují da Vinci asistované operace. Ve srovnání s otevřenými a laparoskopickými resekcemi KR dosahují roboticky asistované operace obdobných klinických a onkologických výsledků při nižší četnosti komplikací.
Submitted/Doručeno: 9. 9. 2021
Accepted/Přijato: 27. 9. 2021
MUDr. Daniel Langer
Chirurgická klinika
2. LF UK a ÚVN Praha
U Vojenské nemocnice 1200
169 02 Praha 6
daniel.langer@uvn.cz
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Weber PA, Merola S, Wasieleweski A et al. Telerobotic-assisted laparoscopic right and sigmoid colectomies for benign dinase. Dis Colon Rectum 2002; 45(12): 1689−1696. doi: 10.1007/s10350-004-7261-2.
2. Rawlings AL, Woodland JH, Crawford DL. Telerobotic surgery for right and sigmoid colectomies: 30 consecutive cases. Surg Endosc 2006; 20(11): 1713–1718. doi: 10.1007/s00 464-005-0771-8.
3. Baik SH, Ko YT, Kang CM et al. Robotic tumor-specific mesorectal excision of rectal cancer: short-term outcome of a pilot randomized trial. Surg Endosc 2008; 22(7): 1601−1608. doi: 10.1007/s00464-008-9752-z.
4. Baek JH, Pastor C, Pigazzi A. Robotic and laparoscopic total mesorectal exciton for rectal cancer: a case-matched study. Surg Endosc 2011; 25(2): 521−525. doi: 10.1007/s00464-010-1204-x.
5. Kim MJ, Park SCh, Park JW et al. Robot-assisted versus laparoscopic surgery for rectal cancer: a phase II open label prospective randomized controlled trial. Ann Surg 2018; 267(2): 243–251. doi: 10.1097/SLA0000000000002321.
6. Prete FP, Pezzolla A, Prete F et al. Robotic versus laparoscopic minimally invasive surgery for rectal cancer. A systematic rereview and meta-analysis of randomized controlled trials. Ann Surg 2018; 267(6): 1034–1046. doi: 10.1097/SLA.0000000000002523.
7. Jayne D, Pigazzi A, Marshall H et al. Effect of robotic-assisted vs conventional laparoscopic surgery on risk of conversion to open laparotomy among patients undergoing resection for rectal cancer. The ROLARR randomized clinical trial. JAMA 2017; 318(16): 1569–1580. doi: 10.1001/jama.2017.7219.
8. Kim MJ, Park SCh, Park JW et al. Robot-assisted versus laparoscopic surgery for rectal cancer: a phase II open label prospective randomized controlled trial. Ann Surg 2018; 267(2): 243–251. doi: 10.1097/SLA0000000000002321.
9. D’Annibale A, Pernazza G, Monsellato I et al. Total mesorectal excision: a comparison of oncological and functional outcomes between robotic and laparoscopic surgery for rectal cancer. Surg Endosc 2013; 27(6): 1887–1895. doi: 10.1007/s00464-012-2731-4.
10. Crippa J, Grass F, Dozois E et al. Robotic surgery for rectal cancer provides advantageous outcomes over laparoscopic approach: results from a large retrospective cohort. Ann Surg 2020. doi: 10.1097/SLA.0000000000003805.
11. Kowalewski KF, Seifert L, Ali S et al. Functional outcomes after laparoscopic versus robotic-assisted rectal resection: a systematic review and meta-analysis. Surg Endosc 2021; 35(1): 81–95. doi: 10.1007/s00464-019-07361-1.
12. Hu JM, Chu ChH, Jiang JK et al. Robotic transanal total mesorectal excision assisted by laparoscopic transabdominal approach: a preliminary twenty-case series report. Asian J Surg 2020; 43(1): 330–338. doi: 10.1016/j.asjsur.2019.06.010.
13. Martinek L, You K, Giuratrabocchetta S et al. Does laparoscopic intracorporeal ileocolic anastomosis decreases surgical site infection rate? A propensity score-matched cohort study. Int J Colorectal Dis 2018; 33(3): 291–298. doi: 10.1007/s00384-017-2957-7.
14. Solaini L, Cavaliere D, Pecchini F et al. Robotic versus laparoscopic right colectomy with intracorporeal anastomosis: a multicenter comparative analysis on short-term outcomes. Surg Endosc 2019; 33(60): 1898–1902. doi: 10.1007/s00464-018-6469-5.
15. Xu H, Li J, Sun Y et al. Robotic versus laparoscopic right colectomy: a meta-analysis. World J Surg Oncol 2014; 12: 27. doi: 10.1186/14 77-7819-12-274.
16. Ma Sa, Chen Y, Chen Y et al. Short-term outcomes of robotic-assisted right colectomy compared with laparoscopic surgery: a systematic review and meta-analysis. Asian J Surg 2019; 42(5): 589–598. doi: 10.1016/j.asjsur.2018.11.002.
17. Park JS, Kang H, Park SY et al. Long-term oncologic after robotic versus laparoscopic right colectomy: a prospective randomized study. Surg Endosc 2018; 33(9): 2975–2981. doi: 10.1007/s00464-018-6563-8.
18. Waters PS, Cheung FP, Peacock O et al. Successful patient-oriented surgical outcomes in robotic vs laparoscopic right hemicolectomy for cancer – a systematic review. Colorectal Dis 2020; 22(5): 488–499. doi: 10.1111/codi.14822.
19. Kim JCh, Lee JL, Yoon YS et al. Robotic left colectomy with complete mesocolectomy for splenic flexure and descending colon cancer, compared with a laparoscopic procedure. Int J Med Robot 2018; 14(5): e1918. doi: 10.1002/rcs.1918.
20. Xu M, Zhao Z, Jia B et al. Perioperative and long-term outcomes of robot-assisted versus laparoscopy-assisted hemicolectomy for left-sided colon cancers: a retrospective study. Updates Surg 2021; 73(3): 1049–1056. doi: 10.10007/s13304-020-00959-4.
21. Patriti A, Ceccarelli G, Bartoli A et al. Laparoscopic and robot-assisted one-stage resection of colorectal cancer with synchronous liver metastases: a pilot study. J Hepatobiliary Pancreat Surg 2009; 16(4): 450−457. doi: 10.1007/s00534-009-0073-y.
22. Berber E, Akyildiz HY, Aucejo F et al. Robotic versus laparoscopic resection of liver tumors. HPB 2010; 12(8): 583−586. doi: 10.1111/j.14 77-2574.2010.00234.x.
23. Giulianotti PC, Coratti A, Sbrana F et al. Robotic liver surgery: results for 70 resections. Surgery 2011; 149(1): 29−39. doi: 10.1016/j.surg.2010.04.002.
24. Choi GH, Choi SH, Kim SH et al. Robotic liver resection: technique and results of 30 consecutive procedures. Surg Endosc 2012; 26(8): 2247−2258. doi: 10.1007/s00464-012-2168-9.
25. Giulianotti PC, Tzvetanov I et al. Robot-assisted right lobe donor hepatectomy. Transpl Int 2012; 25(1): 5−9. doi: 10.1111/j.1432-22 77.2011.01373.x.
26. Hu Y, Guo K, Xu J et al. Robotic versus laparoscopic hepatectomy for malignancy: a systematic review and meta-analysis. Asian J Surg 2021; 44(4): 615–628. doi: 10.1016/j.asjsur.2020.12.016.
27. Giulianotti PC, Sbrana F, Bianco FM et al. Robot-assisted laparoscopic pancreatic surgery: single-surgeon experience. Surg Endosc 2010; 24(7): 1646−1657. doi: 10.1007/s00464-009-0825-4.
28. Buchs NC, Addeo P, Bianco FM et al. Robotic versus open pancreaticoduodenectomy: a comparative study at a single institution. World J Surg 2011; 35(12): 2739−2746. doi: 10.1007/s00268- 011-1276-3.
29. Giulianotti PC, Addeo P, Buchs NC et al. Robotic extended pancreatectomy with vascular resection for locally advanced pancreatic tumors. Pancreas 2011; 40(8): 1264−1270. doi: 10.1097/MPA. 0b013e318220e3a4.
30. Kamarajah SK, Bundred J, Marc OS et al. Robotic versus conventional laparoscopic pancreaticoduodenectomy a systematic review and meta-analysis. Eur J Surg Oncol 2020; 46(1): 6–14. doi: 10.1016/j.ejso.2019.08.007.
31. Sahni VA, Silveira PC, Sainani NI et al. Impact of a structured report template on the quality of MRI reports for rectal cancer staging. AJR Am J Roentgenol 2015; 205(3): 584–588. doi: 10.2214/AJR.14.14053.
32. Ryska M, Langer D. Chirurgická léčba kolorektálního karcinomu. Onkologie 2013; 7(4): 179–182.
33. Ryska M, Langer D, Kalvach J. Některé současné aspekty chirurgické léčby kolorektálního karcinomu. Onkol Rev 2017; 2: 24–29.
34. Miskovic D, Ahmed J, Bissett-Amess et al. European consensus on the standardization of robotic total mesorectal excision for rectal cancer. Colorectal Dis 2019; 21(3): 270–276. doi: 101111/codi.14502.
35. Hoch J, Ferko A, Blaha M et al. Parametrické sledování kvality totální mezorektální excize a chirurgické léčby karcinomu rekta – výsledky multicentrické studie. Rozhl Chir 2016; 95(7): 262–271.
36. Dušek L et al. Czech cancer care in numbers 2008–2009. Praha: Grada Publishing 2009.
37. Rawlings AL, Woodland JH, Crawford DL. Telerobotic surgery for right and sigmoid colectomies: 30 consecutive cases. Surg Endosc 2006; 20(11): 1713–1718. doi: 10.1007/s00 464-005-0771-8.
38. Langer D, Pudil J, Ryska M. Robotická laparoskopická cholecystektomie. Rozhl Chir 2006; 85(9): 450−454.
39. Belli G. Guest editorial. HPB 2004; 6(4): 195–196. doi: 10.1080/13651820410023 932.
40. Ryska M, Froněk J, Rudiš J et al. Manuální a robotická laparoskopická resekce jater. Dvě kazuistiky. Rozhl Chir 2006; 85(10): 511–516.