Refrakterní celiakie a primární sklerózující cholangitida
Přemysl Frič1, Adam Houska Orcid.org , Ivo Buřič Orcid.org , Vít Campr Orcid.org , Petr Hrabal Orcid.org
+ Pracoviště
Souhrn
U ženy s rodinnou anamnézou intolerance lepku a depresí léčenou od mládí byla až ve věku 67 let diagnostikována refrakterní celiakie 1. typu (RC1) spolu s přidruženou primární sklerózující cholangitidou ve fázi pokročilé malnutrice. Rostoucí hodnoty onkomarkerů (CA19-9, CA125) spolu s výsledky zobrazovacích metod (MRCP, CT/PET) připouštěly možnost komplikujícího cholangiogenního karcinomu, který nebyl sekčně potvrzen. Tato okolnost však omezovala terapeutické možnosti doporučené pro RC1. Specificita onkomarkerů při rozsáhlém postižení imunitního systému dvěma chorobami podobné etiologie může být pravděpodobně ovlivněna více než obvykle.
Klíčová slova: refrakterní celiakie - primární sklerózující cholangitida - CA19-9 - CA125.
ÚVOD
Celiakie (C, synonyma: celiakální sprue, glutenová enteropatie) je hereditární autoimunitní onemocnění dětí i dospělých způsobené celoživotní nesnášenlivostí lepku a vyskytující se ve všech zemích světa. V úvodu české monografie o malabsorpčním syndromu vydané před 40 roky je uvedeno, že "osudy nemocných před stanovením definitivní diagnózy bývají pestré"(1). Pokud jde o C, zůstává toto vyjádření v české populaci nadále platné. C je diagnostikována zejména u dospělých nemocných nedostatečně často a naopak často pozdě. Kvalifikovaný odhad prevalence C v České republice je 1 : 200 - 1 : 250, tj. přibližně 40 000 - 50 000 nemocných. V současnosti je však diagnostikováno a dispenzarizováno jen 10 - 15 % z celkového počtu. Dokladem uvedených skutečností je i toto sdělení.
POPIS PŘÍPADU
Nemocná (67 let), vzdělání vysokoškolské, v důchodu, 3 děti (zdravé).
Rodinná anamnéza: Sestra dodržuje bezlepkovou dietu (BLD) pro střevní obtíže, které nebyly diagnosticky objasněny.
Osobní anamnéza: apendektomie, inguinální herniotomie, opakované pneumonie, cysta pravého ovaria.
Nynější onemocnění: V adolescenci sledována pro poruchy příjmu potravy. Dlouhodobě se léčí pro anxiózně-depresivní syndrom antidepresivy. Šest let léčena pro osteoporózu (bifosfonáty, vitamin D). Od září 2007 vyšetřována pro váhový úbytek cca 10 kg za 6 měsíců. Asi měsíc před hospitalizací byla provedena v jiném zařízení ambulantní gastroskopie (mykotická ezofagitida, chronická gastritida, bulbitida) a kolonoskopie (normální nález).
První hospitalizace (12. 5. - 16. 6. 2008)
Důvodem přijetí byly febrilie do 39 °C trvající 3 týdny, nechutenství a progresivní váhový úbytek. Gastrointestinální symptomy byly omezeny na občasnou průjmovitou stolici.
Fyzikální nález: Váha 34 kg, výška 154 cm, BMI 15. Kachektický habitus, výrazné atrofie kosterního svalstva, suchá kůže, prominence břicha s poklepovým zkrácením v podbřišku. Játra nezvětšena, slezina nehmatná.
Biochemie: Proteinémie 54,5 g/l, albumin 22,3 g/l, bilirubin 54 μmol/l, ALT 1, 3 μkat/l, AST 1,2 μkat/l, GMT 12 μkat/l, ALP 38 μkat/l, celkový cholesterol 6, 9 mmol/l, Fe 5,5 μmol/l, Na 120 mmol/l, K 4,0 mmol/l, Cl 95 mmol/l, urea 2,6 mmol/l, kreatinin 43 μmol/l, CRP 70 mg/l. Hematologie: Leu 11,8, Ery 2,4, Hb 75 g/l, HKT 0,23 arb.j., MCV 94 μm3, trombocyty 512.
Autoprotilátky k endomyziu a tkáňové transglutamináze: negativní.
Genetické vyšetření: HLA-DQB1*02: pozitivní.
Onkomakery: CA19-9 463 kU/l, CA125 183 kU/l.
Gynekologické vyšetření: cysta pravého ovaria.
USG břicha: mírná hepatomegalie, nehomogenní jaterní parenchym s difuzně vyšší echogenitou, cysty v obou jaterních lalocích, slezina 70 mm × 50 mm.
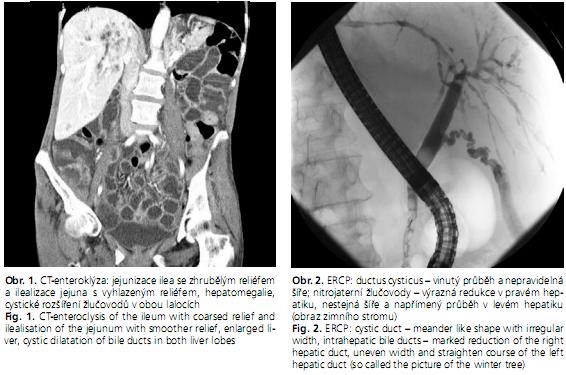
CT enteroklýza: inverze obrazu jejunoileálních řas (obr. 1).
ERCP: zánětlivé změny nitrojaterních žlučovodů v obou lalocích a ductus cysticus kompatibilní s diagnózou primární sklerózující cholangitidy (obr. 2).
Jaterní biopsie: hydropická dystrofie hepatocytů, zánětlivá celulizace portálních polí a v okolí drobných žlučovodů.
Endoskopie horní části trávicí trubice: Příznak mozaiky v bulbu a v duodenu do přechodu D2/D3; Kerkringovy řasy téměř chybí.
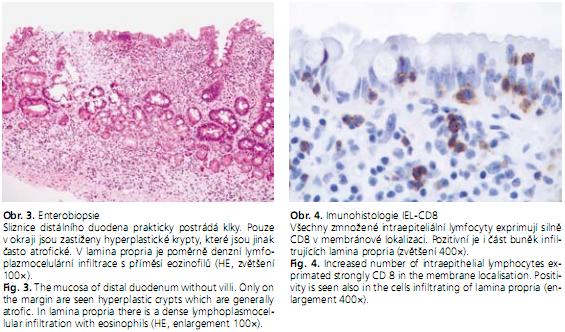
Histologie duodenální biopsie: Neklkatá sliznice místy s hyperplastickými kryptami, lamina propria prostoupena kulatobuněčným infiltrátem. Povrchové enterocyty nepravidelné, často nižší, vakuolizace cytoplazmy, snížení pohárkových buněk. Počet IEL na 100 enterocytů: 55 (obr. 3). Závěr: Celiakie typ 3c (totální atrofie sliznice)(2).
Imunohistologie: Všechny IEL silně exprimují CD3 i CD8 (obr. 4). Molekulární analýza klonality T-lymfocytů: Klonální přestavba genů pro receptor T-buněk (TCR) gama a delta nebyla prokázána. Závěr: Imunohistologická a molekulární analýza neprokázaly IEL fenotyp RC2.
Na základě vyšetření stanovena diagnóza refrakterní C bez preneoplastických IEL (RC1) a primární sklerózující cholangitidy (PSC) jako přidružená autoimunitní choroba. Vzhledem k hodnotám onkomarkerů uvažováno o cholangiogenním karcinomu jako komplikaci PSC.
Terapie: BLD, glukokortikoidy (nejprve Entocort 9 mg/den, poté Prednison 30 mg/den), kyselina ursodeoxycholová 250 mg 3× 2 tbl./den, bezlepková nutriční podpora.
Postupné zlepšení subjektivního stavu i laboratorních nálezů: Proteinémie 57,7 g/l, albumin 25,6 g/l, bilirubin 48,2 μmol/l, ALT 1,40 μkat/l, AST 1,26 μkat/l, GMT 5,99 μkat/l, ALP 14,71 μkat/l, CRP 17,0 mg/l. Hematologie: Leu 8,18, Ery 3,0, Hb 89 g/l, HTK 0,26.
Po 6 týdnech propuštěna do domácího ošetřování. Ambulantně pokračováno v terapii BLD, glukokortikoidy, doplňkovou nutriční terapií a substituční terapií podle zjištěných deficitů.
Druhá hospitalizace: (4. 8. - 22. 9. 2008)
Přijata pro další úbytek tělesné hmotnosti na 31 kg (BMI 12,5). Při laboratorní kontrole prokázáno zejména zhoršení jaterních funkcí (bilirubin 153 μmol/l, ALT 4,7 μkat/l, AST 2,6 μkat/l, GMT 7,3 μkat/l. ALP 11 μkat/l, proteinémie 56 g/l, albumin 27 g/l) a zvýšení CA19-9 na 713 kU/l.
Zahájena parenterální nutriční podpora, nitrožilní podání glukokortikoidů (Solu-Medrol 40 mg) a připojen azathioprin v počáteční dávce 75 mg.
MRCP: PSC intrahepatálních žlučovodů, progrese multicystického postižení jater, možnost drobného periferního cholangiogenního tumoru.
PET/CT: Nepravidelná dilatace nitrojaterních žlučovodů odpovídá PSC. V S5 a S6 dvě ložiska mírně zvýšené akumulace radiofarmaka mohou odpovídat neoplazii, ale i zánětlivý proces zvyšuje akumulaci glukózy.
Vzhledem k možnosti cholangiogenního karcinomu při PSC byla ukončena imunosupresivní terapie a postupně vysazeny glukokortikoidy. Bylo pokračováno v nutriční podpoře a byla zahájena enterální výživa nazojejunální sondou v nočním režimu. S výsledky vyšetření a diagnostickými závěry byla seznámena rodina i pacientka, která odmítla následnou péči typu LDN. Pacientka byla dimitována do domácí péče v kompenzovaném stavu a s poučením o zacházení s enterální pumpou.
Třetí hospitalizace (20. - 24. 10. 2008)
Pro zhoršení stavu byla znovu přijata jako terminální stav při nádorovém onemocnění a 5. den umírá pod obrazem jaterního selhání.
Pitevní nález: nápadný ikterus kůže, sklér i sliznic. Dutina břišní neobsahuje patologický obsah. Povrch jater hladký, parenchym červenohnědý s nepravidelnými šedožlutými ložisky. Dutiny vyplněné žlučí v obou lalocích do 15 mm. Nádor jater a žlučového systému neprokázán. Velikost sleziny nelze hodnotit, v místě orgánu pouze rezidua tkáně v okolí kaudy pankreatu.
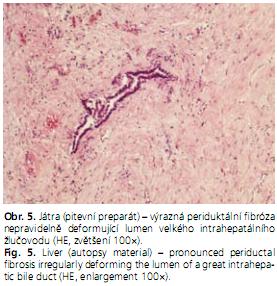
Mikroskopie: nepravidelně rozšířené žlučovody s vazivově ztluštělou stěnou, jejichž morfologie odpovídá změnám při primární sklerózující cholangitidě (obr. 5).
DISKUSE
V současné době je definitivně překonáno dogma, že C je dětskou nemocí, z níž se vyroste, jakož i další dogma, že C se vyskytuje jen v zemích mírného klimatu jako tzv. netropická sprue. Je tomu právě naopak: C se vyskytuje u dětí i dospělých ve všech zemích světa. Lékaři na celiakii málo myslí. Při tom C v rozvinutých zemích přibývá v důsledku zlepšené diagnostiky, screeningu i environmentálních faktorů. Současně se však mění také fenotyp tohoto onemocnění. Pouze u malých dětí převládají gastrointestinální příznaky. U starších dětí může být již v popředí porucha psychosomatického vývoje, anémie a malnutrice. V pubertě se může C spontánně zlepšit, aby se v dospělosti (nejčastěji mezi 25. - 40. rokem) znovu objevila. U dospělých je obraz C individuální a mimostřevní projevy jsou velmi časté (anémie, váhový úbytek, předčasná osteoporóza, herpetiformní dermatitida, ataxie, deprese, poruchy chování, amenorea, poruchy reprodukce, infertilita). V důsledku toho je velký počet nemocných sledován dlouhodobě pro atypické projevy lékaři jiných odborností a diagnóza C je často stanovena až po dlouhém trvání obtíží. Tyto skutečnosti potvrzují výsledky ankety, jíž se zúčastnilo 1480 českých celiaků. Během pěti let od začátku obtíží byla diagnóza C stanovena jen u dvou třetin respondentů a 48 % celiaků bylo sledováno pro své obtíže před stanovením diagnózy dvěma a více lékaři jiných odborností. Mnozí nemocní proto oprávněně považují diagnózu své nemoci za pozdní(3). Cílený screening rizikových skupin a chorob, osob s podezřelými symptomy a přidruženými autoimunitními chorobami je nejbližší a nejdůležitější úkol k časné diagnostice a terapii C.
U nemocné nebyly dlouhodobě vyhodnoceny dva významné rizikové faktory. C se vyskytuje u příbuzných 1. stupně v 8-20 % a tito jedinci jsou jednoznačně významnou rizikovou skupinou vyžadující screening(4). Deprese bývají poměrně častým symptomem již u mladých nemocných s C. Výskyt depresí i poruch chování je u celiaků mnohem vyšší než v ostatní populaci (31 % vs. 7 % a 28 % vs. 3 %) (5). U nemocné byla diagnóza stanovena až ve fázi refrakterní C (RC). Tato se vyskytuje u 10-20 % osob s C neodpovídajících na léčbu bezlepkovou dietou (BLD) a je její nejvýznamnější příčinou. Diagnostický postup zahrnuje genetické vyšetření HLA-DQ2, -DQ8 a biopsii aborálního duodena. Nepřítomnost rizikového genu prakticky vylučuje celiakii a revize této diagnózy je nezbytná. Při histologickém vyšetření biopsie se zjistí slizniční atrofie a výrazně zvýšený počet intraepiteliálních lymfocytů (IEL). Tyto jsou cytologicky normální, ale podle jejich imunofenotypu rozlišujeme RC 1. typu (RC1 - znaky CD3 a CD8 jsou uloženy v buněčné membráně) a RC 2. typu (RC2 - CD3 přítomen pouze v plazmě a CD8 chybí)(6). Kromě toho lze prokázat při RC2 přestavbu gama a delta řetězce receptoru T-lymfocytů(7). C u naší nemocné byla klasifikována podle obou metodických přístupů jako RC1. Výskyt pozdních komplikací C (kolagenní sprue, ulcerózní jejunoileitida, T-lymfom) je při RC1 výrazně nižší než při RC2. Stav nemocné však významně ovlivňovala pokročilá primární sklerózující cholangitida. Tato patří k přidruženým autoimunitním chorobám provázejícím celiakii a může se sama dále komplikovat vznikem cholangiogenního karcinomu.
Bezlepková dieta (BLD) zůstává od Dickeho objevu(8) již více než 50 let jedinou kauzální terapií C a radikálně změnila prognózu tohoto onemocnění. Mortalita před jejím zavedením činila 10-30 %, kdežto při časné diagnostice a dodržování BLD činí méně než 1 % a neliší se významně od mortality v příslušné věkové skupině ostatní populace. BLD poskytuje nemocnému šanci, že se u něho neobjeví přidružené autoimunitní choroby ani jiné komplikace. BLD však musí být úplná, nebo» pokud je lepek v potravě obsažen, je imunitní systém celiaka trvale pod zvýšeným antigenním tlakem (antigen drive) a vnímavost nemocných na zbytkové množství lepkových peptidů je individuálně velmi různá. Dlouhodobá přítomnost lepku v potravě vede u geneticky disponovaných jedinců k postupnému vyčerpání až kolapsu imunitního systému s rozvojem komplikací, z nichž k pokročilým patří hyposplenismus, kavitace mezenteriálních uzlin a zhoubné nádory (T-lymfom, karcinom).
Standardní terapie RC1 bez podezření na maligní nádor zahrnuje glukokortikoidy, popřípadě v kombinaci s imunosupresivy, a při nedostatečné odpovědi přicházejí v úvahu monoklonální protilátky k TNF-alfa(9). Podezření na cholangiogenní karcinom opírající se o stoupající hodnoty onkomarkerů a nejednoznačné výsledky zobrazovacích metod (MRCP, PET/CT) vedly u nemocné k omezení terapeutických možností. Cholangiogenní karcinom však nebyl sekčně potvrzen. Lze proto usuzovat, že hodnoty onkomarkerů mohou mít při postižení imunitního systému dvěma významnými autoimunitními chorobami specificitu nižší než jinak předpokládanou. Pokročilá destrukce imunitního systému je doložena nálezem malé sleziny při sonografickém vyšetření a prakticky jen zbytků slezinné tkáně při pitvě.
ZÁVĚR
Současné znalosti patofyziologie, diagnostiky a terapie C umožňují rozpoznání nemoci v časné fázi a přijetí adekvátních terapeutických opatření. Jelikož zbývá v české populaci velká populace dosud neidentifikovaných celiaků, zůstává tato choroba výzvou pro všechny odbornosti, jichž se dotýká, jakož i pro laickou veřejnost.
LITERATURA
- 1. Frič P. Malabsorpční syndrom. Praha: Státní zdravotnické nakladatelství 1969; s. 396.
- 2. Oberhuber G, Granditsch G, Vogelsang H. The histopathology of celiac disease: time for a standard report scheme for pathologists. Eur J Gastroenterol, Hepatol 1999; 11: 1185-1194.
- 3. Frič P, Bušinová I. Celiakie - pohledy z druhé strany. Interní Med 2008; 10: 482-484.
- 4. Frič P. Celiakální sprue - současnost a perspektiva. Postgrad Med 2006; 8: 588-593.
- 5. Pynnonen PA, Isometra ET, Aronen ET, et al. Mental disorders in adolescents with celiac disease. Psychosomatics 2004; 45: 325-335.
- 6. Putey-Mariaud de la Serre N, Cellier C, Jabri B, et al. Distinction between coeliac disease and refractory sprue: simple immunohistochemical method. Histopathology 2000; 17: 70-77.
- 7. Cellier C, Delabesse E, Helmer C, et al. Refractory sprue, coeliac disease, and enteropathy-associated T-cell lymphoma. Lancet 2000; 356: 203-208.
- 8. Dicke WK. Coeliakie:een onderzoek naar de nadelige invloed van sommige graansoorten op de lijder aan coeliakie. Thesis. Utrecht University, Holland, 1950: s. 114.
- 9. Frič P. Refrakterní celiakie. Medicína po promoci 2009; 10: 99-103.
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené