Receptorové mechanizmy aktivácie pažerákových nervov kyselinou
Peter Bánovčin Jr1, Martin Ďuriček Orcid.org 1, Rudolf Hyrdel Orcid.org 1
+ Pracoviště
Souhrn
Počas gastroezofágového refluxu (GER) dochádza k výraznému poklesu pH v lumen pažeráka. V úrovniach nervových zakončení sliznice pažeráka je ale vďaka jej bariérovej funkcii pH oveľa vyššie (pH 5,5–6,5). Napriek tomu, že bariérová funkcia sliznice je pri pažerákovej refluxovej chorobe (GERD) čiastočne porušená, dostatočne zabraňuje difúzii kyseliny do tkaniva a nedochádza k následnej deštrukcii buniek. Predpokladá sa, že pažerákové nociceptívne neuróny, ktoré sprostredkujú bolesť a pyrózu, exprimujú receptory vysoko senzitívne na kyselinu, a sú teda stimulované už pri miernom poklese pH. V recentných modelových štúdiách na morčatách sme dokázali, že už slabá kyselina (pH 5,5–6,5) môže masívne stimulovať spinálne nociceptívne C-vlákna. V súlade s týmto pozorovaním sme pomocou génovej analýzy zistili, že pažerákové aferentné nervové vlákna redundantne exprimujú viaceré receptory, ktoré sú vysoko citlivé na kyselinu. Identifikovali sme iónové kanály citlivé na kyselinu (ASICs – acid sensing ion channels), receptory spriahnuté s G-proteínom reagujúce na kyselinu (OGR1 – proton sensing G-protein coupled receptor) a TASK1 zo skupiny drasíkových kanálov zo skupiny K2P. Vysoká vnímavosť nociceptívnych nervov na kyselinu pri oslabenej báriérovej funkcii sliznice (napr. pri GERD) prispieva k vzniku ezofágových senzácií, ako je pyróza a bolesť pažerákového pôvodu. Receptory, ktoré sprostredkúvajú citlivosť na kyselinu, môžu v budúcnosti slúžiť ako nové terapeutické ciele pre aditívnu alebo alternatívnu liečbu k antisekrečnej liečbe.
Klíčová slova
ionové kanály citlivé na kyselinu, jícen, pyróza, refluxní choroba jícnuÚvod
Aferentné informácie z pažeráka sú sprostredkované do centrálneho nervového systéma (CNS) pomocou vágových a spinálnych aferentných nervových dráh. Vágové primárne aferentné neuróny sa nachádzajú v jugulárnych a nodóznych gangliách a centrálne majú synaptické zapojenia v mozgovom kmeni (nucleus tractus solitarii). Spinálne primárne aferentné neuróny sa nachádzajú v gangliách zadných miechových koreňov (spinal DRG – dorsal root ganglia) a centrálne majú synaptické zapojenia v mieche [1]. V staršej literatúre sa niekedy menej správne označujú vágové aferentné dráhy ako parasympatikové viscerálne aferentné nervy a spinálne aferentné dráhy ako sympatikové viscerálne aferentné nervy.
Vágové aj spinálne aferentné nervy poskytujú CNS informáciu o prítomnosti kyseliny v pažeráku. Predpokladá sa, že informácia sprostredkovaná vágovými dráhami ovplyvňuje hlavne reflexnú reguláciu motility pažeráka a sekundárne ovplyvňuje vnemy z pažeráka. Naproti tomu informácia sprostredkovaná spinálnymi aferetnými dráhami sa považuje za kľúčovú pre percepciu pyrózy a pažerákovej bolesti. Hoci je kyselina najdôležitejší noxický mediátor vo fyziológii a patofyziológii pažeráka [2,3], receptory a iónové kanály, ktoré sprostredkujú aktiváciu pažerákových vágových a spinálnych nervov kyselinou, nie sú známe. Za túto prekvapujúcu medzeru v biomedicínskom poznaní je zodpovedná najmä skutočnosť, že mechanizmy aktivácie pažerákových nervov kyselinou sa študujú relatívne ťažko, pretože pažeráková sliznica je relatívne nepriepustná pre kyselinu.
Našej skupine sa v posledných rokoch podarilo prekonať niektoré závažné prekážky štúdia aferentných nervových mechanizmov a urobiť pokrok v identifikácii receptorov a iónových kanálov citlivých na kyselinu v pažerákových nervoch [4,5].
Pretože pH v lúmen pažeráka dosahuje počas refluxu extrémne nízke hodnoty (pH < 4 až pH = 1), vzniká predstava, že receptory na kyselinu v nervových zakončeniach pažeráka sú citlivé práve na takéto extrémne nízke pH hodnoty. V skutočnosti je ale funkcia nervovej membrány aferentného nervového zakončenia aj krátkodobo nezlučiteľná s takouto aciditou. Pri pH 4 dochádza k okamžitej blokáde napäťovo riadených sodíkových kanálov nevyhnutných pre nervovú signalizáciu (vznik akčných potenciálov) a v krátkom čase dôjde k ireverzibilnej desenzibilizácii nervového zakončenia. Je preto prakticky vylúčené, aby bolo na úrovni nervových zakončení v pažeráku pH < 4.
V skutočnosti sa dá predpokladať, že pažerákové aferentné nervové zakončenia zodpovedné za percepciu kyseliny sú chránené pažerákovou slizničnou bariérou a reagujú na oveľa menšie odchýlky pH od fyziologických hodnôt. Inými slovami v dôsledku prítomnosti pažerákovej slizničnej bariéry je koncentrácia kyseliny (pH) vo vrstvách, kde sa nachádzajú nervové zakončenia, oveľa nižšia ako v lúmen pažeráka. Ak dôjde k porušeniu bariérovej funkcie sliznice (napr. pri gastroezofálnom refluxu (GER)) a pH v lúmen pažeráka poklesne (v dôsledku kyslého refluxu), znižuje sa pH aj na úrovni zakončení aferentných nervov v pažeráku. Hoci meranie pH v sliznici pažeráka in vivo je technologicky extrémne náročné (napr. použitím fluorescenčných pH indikátorov), priekopnícke štúdie v tejto oblasti potvrdzujú koncept, že pH v sliznici (kde sa nachádzajú nervové zakončenia) je oveľa vyššie ako pH v pažerákovom lúmen [6]. Predbežné odhady ukazujú, že ak je pH v lúmen pažeráka 1–4, je pH na úrovni nervových zakončení v sliznici pažeráka pravdepodobne v rozsahu 5,5–6,5 (tj. pri pH < 4 je koncentrácia H+ v sliznici pažeráka cca 1 000× nižšia ako v lúmen).
Metodiky štúdia aferentných nervov inervujúcich pažerák
V našich štúdiách [4,5] sme sa zamerali na nervové receptory, ktoré sú relatívne veľmi citlivé na kyselinu (tj. v rozsahu pH 5,5–6,5). Informácie o aktivácii pažerákových nervových zakončení kyselinou a o expresii receptorov na kyselinu v týchto zakončeniach je možné efektívne získať pomocou metodík extracelulárneho snímania nervovej aktivity a reverznej transkripcie polymerázové reťazové reakcie (RT-PCR); z individuálnych neurónov retrográdne značených z pažeráka. Kvôli úplnosti uvádzame prehľadný popis týchto metodík.
Extracelulárne snímanie nervovej aktivity zo spinálnych dorsal root ganglia nociceptorov inervujúcich pažerák
Toto snímanie bolo popísané v našich predchádzajúcich prácach [5,7]. Snímanie sme vykonali v podmienkach ex vivo v izolovanom perfundovanom preparáte pažeráka morčaťa so zachovanou spinálnou aferentnou inerváciu vľavo v rozsahu T1–T2. Pažerákový preparát sme umiestnili do perfúznej komôrky perfundovanej okysličeným Krebsovým roztokom. T1–T2 DRG sme presunuli cez úzke kanáliky do snímacej komôrky, kde boli individuálne upevnené. Do kraniálnej a kaudálnej časti pažeráka sme zaviedli polyetylénové kanyly. Z kaudálnej časti sme privádzali intraluminálne Krebsov roztok pri rôznych definovaných tlakoch (10, 30 a 60 mmHg) a pri tejto mechanickej stimulácii sme nahrávacím zariadením zaznamenávali nervovú aktivitu. Do T1–T2 DRG sme zaviedli aluminosilikátovú mikroelektródu a elektrickou stimuláciou pažeráka sme vyhľadávali aferentné nervové vlákna z pažeráka. Nervovú aktivitu sme zosilnili pomocou Microelectrode AC amplifier 1800 (A-M Systems), filtrovali, zobrazili na osciloskope a zaznamenali a analyzovali na počítači Apple (vzorkovacia frekvencia 33 kHz). Na hodnotenie odpovede nervových vláken na kyselinu sme použili HEPES roztok, ktorý bol pufrovaný pomocou kyseliny chlorovodíkovej na požadované pH.
Metodika pre RT-PCR z individuálnych neurónov retrográdne značených z pažeráka
Tato metodika bola detailne popísaná v našich predchádzajúcich štúdiách [4,5]. RT-PCR sme vykonali z individuálnych spinálnych DRG neurónov retrográdne značených z pažeráka pomocou neurálneho DiI tracera u morčiat. Retrográdny značkovač DiI sme selektívne naočkovali do pažeráka u anestezovaného zvieraťa a po 10–14 dňoch sme gangliá vypreparovali a enzymaticky disociovali na individuálne neuróny. Neuróny inervujúce pažerák (obsahujúce Dil retrográdne transportovaný do neurónov po injekcii do pažeráka) sme identifikovali pod fluorescenčným mikroskopom a za stálej perfúzie chladeným pufrovaným fyziologickým roztokom sme individuálne zbierali sklenenými mikropipetami pomocou kontrolovaného podtlaku do PCR skúmaviek. Následne sme na vzorkách individuálnych neurónov vykonali reverznú transkripciu pomocou špeciálneho kitu Super-Script (tm) III CellsDirect cDNA Synthesis System (Life Technologies) a potom PCR.
Obmedzená úloha TRPV1 v aktivácii pažerákových nervových zakončení kyselinou
Väčšina vágových a spinálnych pažerákových nervov (C-vláken), ktoré sprostredkúvajú noxické informácie vrátane pyrózy a bolesti, exprimuje kapsaicínový receptor TRPV1 [7–11], ktorý tiež môže byť aktivovaný kyselinou [12]. Preto sa TRPV1 označuje ako hlavný pažerákový receptor pre kyselinu [13]. Pre aktiváciu TRPV1 je ale potrebná relatívne vysoká acidita (pH ≤ 5) [12].
Na druhej strane v rôznych orgánových a bunkových systémoch boli objavené a popísané aj iné receptory a iónové kanály, ktoré môžu byť aktivované kyselinou. K týmto receptorom a iónovým kanálom patria 1. ASIC kanály (acid-sensing ion channels), 2. niektoré draslíkové kanály zo skupiny K2P (two-pore-domain potassium channels), 3. niektoré TRP (transient receptor potential) kanály a 4. receptory spriahnuté s G-proteínom reagujúce na kyselinu (proton-sensing G-protein coupled receptors) [13].
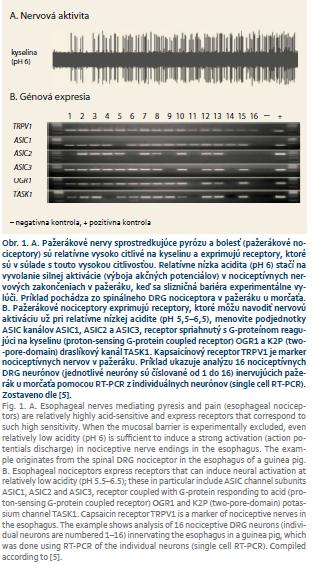
V našich štúdiách [5] pri experimentálnom vylúčení bariérovej funkcie sliznice sme zistili, že nervové zakončenia pažerákových nociceptorov (spinálnych DRG C-vlákien inervujúcich pažerák u morčaťa) sú relatívne vysoko citlivé na kyselinu. Kyselina stimulovala niektoré pažerákové nociceptory už pri pH 6,5 a pri pH 5,5 už boli aktivované prakticky všetky pažerákové nociceptory. Táto aktivácia bola relatívne silná – pri pH 6 dosiahla takmer polovicu maximálnej noxickej aktivácie pažerákových nociceptorov (obr. 1A). V súlade s doterajšími poznatkami, že kyselina pri pH > 5,5 stimuluje kapsaicínový receptor TRPV1 len minimálne, sme ukázali, že odpoveď pažerákových nociceptorov na kyselinu pri pH 6 nie je sprostredkovaná TRPV1 (nebola inhibovaná antagonistom TRPV1 I-RTX). Tento experiment ukázal, že iné receptory ako TRPV1 sú zodpovedné za aktiváciu nociceptívnych nervov v pažeráku kyselinou.
Expresia a úloha ASIC, K2P a receptorov spriahnutých s G-proteínom v aktivácii pažerákových nervových zakončení kyselinou
V ďalších štúdiách [4,5] sme sa preto sústredili na zisťovanie, ktoré receptory vysoko citlivé na kyselinu [13] sú exprimované v pažerákových nociceptoroch. Na analýzu expresie týchto receptorov sme použili unikátnu metodiku umožňujúcu detekciu génovej expresie v jednotlivých neurónoch (single cell RT-PCR) [14]. Študovali sme nociceptívne neuróny inervujúce pažerák u morčaťa, ktoré sme identifikovali pomocou retrográdneho fluorescentného značenia [4,5]. Najprv sme sa sústredili na pažerákové spinálne DRG nociceptory, ktoré sa považujú za hlavnú dráhu pre bolesť a pyrózu z pažeráka. Zistili sme, že vo veľkej väčšine pažerákových nociceptorov boli exprimované ASIC kanály (obr. 1B). ASIC1 a ASIC3 boli exprimované v približne 70 % nociceptorov a ASIC2 v 50 % nociceptorov. Celkovo takmer 90 % pažerákových spinálnych nociceptorov exprimovalo aspoň jeden ASIC kanál. Ohľadne špecifických podjednotiek, pažerákové nociceptory exprimovali obidva varianty ASIC1 (ASIC1a a ASIC1b), ale iba jednu variantu ASIC2 (ASIC2b, nie však ASIC2a) [5]. Podobne ako spinálne DRG nociceptory aj vágové pažerákové nociceptory exprimovali ASIC kanály [4]. Profil expresie ASIC kanálov v pažerákových vágových jugulárnych nociceptoroch bol prakticky identický so spinálnymi DRG nociceptormi. Pažerákové vágové nodózne nociceptory ale navyše exprimovali aj ASIC2a podjednotku, ktorá výrazne modifikuje odpoveď na kyselinu [4].
Z drasíkových kanálov zo skupiny K2P sme testovali tie, ktoré sú vysoko citlivé na kyselinu (TASK1, TASK3 a TALK1). Zistili sme, že 75 % pažerákových nociceptorov exprimuje TASK1. Naproti tomu tieto nervy neexprimovali TASK3 a TALK1. Z receptorov spriahnutých s G-proteínom reagujúcich na kyselinu (proton sensing G-protein coupled receptors) exprimovali pažerákové nociceptory OGR1 (85 %), ale len zriedkavo ostatných členov tejto skupiny receptorov (G2A, GPR4 a TDAG8). Pažerákové spinálne DRG nociceptory neexprimovali TRP kanály, ktoré sú citlivé na kyselinu (PKD2L1 and TRPV4).
Záver
Naše výsledky ukazujú, že nociceptívne nervy v pažeráku exprimujú redun-dantné kombinácie receptorov vysoko citlivých na kyselinu (ASIC, TASK1 a OGR1) a relatívne silne reagujú na kyselinu už pri pH 5,5–6,5 (obr. 1) [4,5]. Tieto výsledky sú v dobrom súlade s meraním pH v sliznici pažeráka. V zdravej sliznici sa pH prakticky nemení z fyziologických hodnôt, ani keď je pH v lúmen pažeráka blízko pH 1 [6].
Doteraz ale neboli publikované štúdie hodnotiace pH v sliznici pažeráka u pacientov s GER. Štúdie hodnotiace bariérovú funkciu pažerákovej sliznice ale ukazujú, že parametre slizničnej bariéry sú kvantitatívne len mierne znížené pri GER [15–18], čo naznačuje, že rezistencia pre difúziu kyseliny je stále prítomná. Okrem toho pufrovacia kapacita extracelulárnej tekutiny ďalej minimalizuje výchylky pH v sliznici. Z toho vyplýva, že sa pravdepodobne do sliznice pažeráka dostáva aj pri GER a kyslom refluxe len relatívne málo kyseliny (tj. pH v sliznici klesá na pH 5,5–6,5 aj keď je v lúmen extrémne nízke pH 1). Toto je aj v súlade s nezlučiteľnosťou bunkových funkcií s nižším extracelulárnym pH (pH < 5). Je preto logické očakávať, že nervové zakončenia pažerákových nociceptívnych nervov [19] sú relatívne vysoko citlivé na kyselinu, aby mohli sprostredkovať nociceptívnu informáciu (vedúcu niekedy k pyróze a bolesti) už pri malých zmenách slizničného pH, ktoré ohrozujú pažerák poškodením. Z terapeutického hľadiska by mohla inhibícia receptorov citlivých na kyselinu pomôcť ako aditívna liečba k supresii sekrécie žalúdočnej kyseliny.
Mechanizmy aktivácie nervových zakončení v pažeráku sú len veľmi málo prebádané [1]. V literatúre je prekvapivo len niekoľko publikovaných štúdií, ktoré väčšinou len nepriamo alebo v obmedzenej miere skúmajú mechanizmy aktivácie pažerákových nervových zakončení kyselinou [20,21]. Dôvodom je veľká technická a koncepčná náročnosť takýchto štúdií [4,5]. Publikované práce v princípe nie sú v rozpore s našimi výsledkami, ale metodické aspekty, rozdiely v stimulačných protokoloch a medzidruhové rozdiely sťažujú priame porovnávanie výsledkov.
Práca bola podporená Grantom Ministerstva zdravotníctva SR 2012 a BioMed Martin (ITMS: 26220220187) podporené EÚ.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Doručeno/Submitted: 20. 8. 2015
Přijato/Accepted: 3. 10. 2016
MUDr. Peter Bánovčin Jr, PhD.
Interná klinika gastroenterologická
JLF UK a UN Martin
Kollárova 2
036 59 Martin
Slovenská republika
pbanovcin@gmail.com
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Page AJ, Blackshaw LA. Roles of gastro-oesophageal afferents in the mechanisms and symptoms of reflux disease. Handb Exp Pharmacol 2009; 194: 227–257. doi: 10.1007/978-3-540-79090-7_7.
2. Orlando RC. Pathophysiology of gastroesophageal reflux disease. J Clin Gastroenterol 2008; 42 (5): 584–588. doi: 10.1097/MCG.0b013e31815d0628.
3. Boeckxstaens GE, Rohof WO. Pathophysiology of gastroesophageal reflux dis-ease. Gastroenterol Clin North Am 2014; 43 (1): 15–25. doi: 10.1016/j.gtc.2013.11. 001.
4. Dusenkova S, Ru F, Surdenikova L et al. The expression profile of acid sensing ion channel (ASIC) subunits ASIC1a, ASIC1b, ASIC2a, ASIC2b and ASIC3 in the esophageal vagal afferent nerve subtypes. Am J Physiol Gastrointest Liver Physiol 2014; 307 (9): G922–G930. doi: 10.1152/ ajpgi. 00129.2014.
5. Ru F, Banovcin P Jr, Kollarik M. Acid sensitivity of the spinal dorsal root ganglia C-fiber nociceptors innervating the guinea pig esophagus. Neurogastroenterol Motil 2015; 27 (6): 865–874. doi: 10.1111/ nmo.12561.
6. Tanaka S, Chu S, Hirokawa M et al. Direct measurement of acid permeation into rat oesophagus. Gut 2003; 52 (6): 775–783.
7. Ru F, Surdenikova L, Brozmanova M et al. Adenosine-induced activation of esophageal nociceptors. Am J Physiol Gastrointest Liver Physiol 2011; 300 (3): G485–G493. doi: 10.1152/ajpgi.00361. 2010.
8. Brozmanova M, Ru F, Surdenikova L et al. Preferential activation of the vagal nodose nociceptive subtype by TRPA1 agonists in the guinea pig esophagus. Neurogastroenterol Motil 2011; 23 (10): e437–e445. doi: 10.1111/j.1365-2982.2011.01768.x.
9. Yu S, Ru F, Ouyang A et al. 5-Hydroxytryptamine selectively activates the vagal nodose C-fibre subtype in the guinea-pig oesophagus. Neurogastroenterol Motil 2008; 20 (9): 1042–1050. doi: 10.1111/j.1365-2982.2008.01136.x.
10. Yu S, Undem BJ, Kollarik M. Vagal afferent nerves with nociceptive properties in guinea-pig oesophagus. J Physiol 2005; 563 (Pt3): 831–842.
11. Surdenikova L, Ru F, Nassenstein C et al. The neural crest-and placodes-derived afferent innervation of the mouse esophagus. Neurogastroenterol Motil 2012; 24 (10): e517–e525. doi: 10.1111/nmo.12002.
12. Julius D. TRP channels and pain. Annu Rev Cell Dev Biol 2013; 29: 355–384. doi: 10.1146/annurev-cellbio-101011-155833.
13. Holzer P. Acid sensing by visceral affer-ent neurones. Acta Physiol (Oxf) 2011; 201 (1): 63–75. doi: 10.1111/j.1748-1716. 2010.02143.x.
14. Liu Q, Tang Z, Surdenikova L et al. Sensory neuron-specific GPCR Mrgprs are itch receptors mediating chloroquine-induced pruritus. Cell 2009; 139 (7): 1353–1365. doi: 10.1016/j.cell.2009.11.034.
15. Weijenborg PW, Smout AJ, Verseijden C et al. Hypersensitivity to acid is associated with impaired esophageal mucosal integrity in patients with gastroesophageal reflux disease with and without esophagitis. Am J Physiol Gastrointest Liver Physiol 2014; 307 (3): G323–G329. doi: 10.1152/ ajpgi.00345.2013.
16. Farré R, Blondeau K, Clement D et al. Evaluation of oesophageal mucosa integrity by the intraluminal impedance technique. Gut 2011; 60 (7): 885–892. doi: 10.1136/gut.2010.233049.
17. Jovov B, Que J, Tobey NA et al. Role of E-cadherin in the pathogenesis of gastroesophageal reflux disease. Am J Gastroenterol 2011; 106 (6): 1039–1047. doi: 10.1038/ajg.2011.102.
18. Weijenborg PW, Rohof WO, Akkermans LM et al. Electrical tissue impedance spectroscopy: a novel device to measure esophageal mucosal integrity changes during endoscopy. Neurogastroenterol Motil 2013; 25 (7): 574–578. doi: 10.1111/nmo.12106.
19. Kollarik M, Ru F, Brozmanova M. Vagal afferent nerves with the properties of nociceptors. Auton Neurosci 2010; 153 (1–2): 12–20. doi: 10.1016/j.autneu.2009.08. 001.
20. Harrington AM, Brierley SM, Isaacs NJ et al. Identifying spinal sensory pathways activated by noxious esophageal acid. Neurogastroenterol Motil 2013; 25 (10): e660–e668. doi: 10.1111/nmo.12180.
21. Banerjee B, Medda BK, Lazarova Z et al. Effect of reflux-induced inflammation on transient receptor potential vanilloid one (TRPV1) expression in primary sensory neurons innervating the oesophagus of rats. Neurogastroenterol Motil 2007; 19 (8): 681–691.