Niektoré genetické determinanty celiakie, význam HLA typizácie v klinickej praxi a zastúpenie HLA-DQ haplotypov v súbore 306 detských pacientov
Michal Kubina1, Iveta Čierna1, Dagmar Székyová1, László Kovács Orcid.org 1
+ Pracoviště
Souhrn
Celiakia je chronická imunitne sprostredkovaná enteropatia tenkého čreva vyvolaná požívaním lepku a postihujúca geneticky predisponovaných jedincov. Postihuje 1 % populácie, napriek tomu, že takmer 40 % ľudí je nosičom hlavného predisponujúceho faktoru a conditio sine qua non – HLA-DQ2/DQ8 haplotypu. Berúc do úvahy exklúzne kritérium nosičstva HLA-DQ2/DQ8 ako hlavného predisponujúceho faktora celiakie sme podrobili 306 pacientov sledovaných pre celiakiu v gastroenterologickej ambulancii II. detskej kliniky LF UK a DFNsP v Bratislave vyšetreniu HLA-DQ2 haplotypu. Celkom 17 % (54 zo 306) pacientov, ktorí neboli nosičmi HLA-DQ haplotypu asociovaného s celiakiou, sme podrobili záťaži lepkom a podarilo sa nám vylúčiť celiakiu u 50 pacientov (16 %). U troch pacientov sme preukázali neceliakálnu intoleranciu lepku.
Klíčová slova
HLA-DQ antigény, HLA-DQ2 antigen, HLA-DQ8 antigeny, celiakie, haplotypy, imunogenetikaÚvod
Celiakia je chronická imunitne sprostredkovaná enteropatia tenkého čreva s autoimunitnými črtami. Je vyvolaná požívaním lepku a postihuje geneticky predisponovaných jedincov.
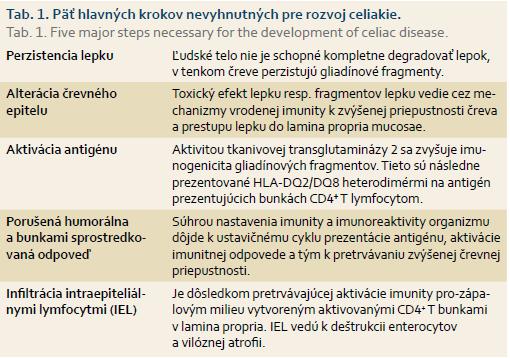
Cieľom daného článku je podat prehľad známych genetických determinantov celiakie a ich významu pre klinickú prax. Zároveň prezentujeme distribúciu HLA haplotypov u pacientov v nami sledovanej skupine celiatikov a využitie negatívnej prediktívnej hodnoty HLA haplotypizácie (tab. 1).
Prepuknutie celiakie
Celiakia sa histologicky charakterizuje selektívnou deštrukciou enterocytov tenkého čreva s intraepiteliálnou lymfocytózou. Bazálna membrána epitelu však ostáva neporušená, bez tvorby ulcerácií [1]. Spustenie patologickej imunitnej odpovede charakteristickej pre celiakiu je podmienené prítomnosťou gluténových oligopeptidov v lamina propria mucosae.
Pre vysoký obsah prolínu a lyzínu sú prolamíny (v alkohole rozpustná proteínová zložka obilovín) odolné voči degradácii žalúdočnými a pankreatický́mi peptidázami ako aj peptidázami kefkového lemu enterocytov. V lumene čreva pretrvávajú nestrávené 30–130-jednotkové oligopeptidy prolamínov [2]. Tieto sa do lamina propria mucosae dostávajú buď transcelulárnym prenosom závislým od receptora, alebo paracelulárne.
Paracelulárny prestup je umožnený porušením súdržnosti tesných spojov epitelu. U celiatikov sa zistila zvýšená koncentrácia zonulínu (ZO-1, prehaptoglobulin-2) [3]. Ide o analóg toxínu zonula occludens produkovanom Vibrio cholerae s funkciou reverzibilne modulovať priepustnosť tesných spojení v črevnom epitele [4]. Stimuláciou CXCR3 receptoru na apikálnej strane enterocytov gluténovými peptidami dochádza k zvýšenému uvoľňovaniu ZO-1 a následnej zvýšenej paracelulárnej priepustnosti epitelu [5].
Druhým spôsobom vstupu gluténových fragmentov do črevnej steny je transcelulárny retrotransport komplexu sekrečného IgA1 a fragmentu gluténu prostredníctvom endocytózy sprostredkovanom receptorom a lyzozomálnym transportom. Endocytovaný fragmet lepku zostáva intaktný a môže byť priamo substrátom pre tkanivovú transglutaminázu (tTG) 2. U pacientov so selektívnym deficitom IgA sú transportovené komplexy gluténu s IgG [6].
Neopomenuteľný je priamy efekt lepku na črevný epitel. Natívny glutén zvyšuje v čreve tvorbu IL-15 a tým aj priepustnosť epitelu. Obdobný efekt majú gliadínové peptidy aj u zdravých jedincov, u nich sa však nespustí odpoveď adaptívnej imunity [7].
Antigény, ktoré preniknú do lamina propria, zväčša navodzujú imunotoleranciu. Imunotolerancia je podmienená vytvorením antigén-špecifických regulačných T lymfocytov. U celiatikov však dochádza k diferenciácii glutén špecifických efektorových T lymfocytov typu CD4+. Tieto produkujú proinflamačné cytokíny (INF-γ, IL-21 [8]), ktoré aktivujú cytotoxické T lymfocyty s následnou deštrukciou enterocytov [9]. Špecifické T lymfocyty naviac asistujú B lymfocytom pri ich diferenciácii na plazmatické bunky tvoriace protilátky proti gliadíniu a tTG2. Spustenie patologickej imunitnej odpovede u pacientov s celiakiou je teda zjavne podmienené „odlišným“ nastavením vrodenej a adaptívnej zložky ich imunity.
U celiatikov bola pozorovaná aj zvýšená aktivácia signálnej cesty INF-γ a znížená expresia IL-2 [10]. IL-2 vylučovaný autokrinne stimulovanými T bunkami je kľúčovým cytokínom T bunkovej aktivácie, proliferácie a stimuluje preferenčnú Th1 slizničnú odpoveď [11]. Ani bezlepková diéta neupravuje túto zvýšenú́ aktiváciu, čo len dokazuje a priori alterované nastavenie imunitného systému postihnutých jedincov.
Úloha tTG je zásadná v patogenéze celiakie. Fragmenty gluténu vo svojom natívnom stave majú veľmi nízku afinitu k HLA-DQ2/DQ8. tTG2 je všade sa vyskytujúci enzým s funkciou determinovanou jej lokalizáciou. V čreve ide o primárne intracelulárny enzým, ktorý sa aktivuje pri bunkovom poškodení, vtedy stúpa aj jeho expresia [12]. tTG2 špecificky deamiduje glutamínové zvyšky gliadínov, glutenínov, sekalínov a hordeínov v proteínovej sekvencii Glu-X-Pro (kde X je akákoľvek aminokyselina) [13]. Tým vzniká negatívny náboj fragmentov s doménami špecifickými pre HLA-DQ2/DQ8 a zvyšuje sa ich afinita k antigén prezentujúcim bunkám s daným receptorom, čo umožní silnú väzbu s T bunkovým receptorom [14].
Aveníny sú vzhľadom na nízky podiel prolínu deamidované v minimálnom množstve, preto sú zväčša dobre tolerované pacientami s celiakiou, len ojedinele vyvolávajú obdobnú odpoveď ako gliadíny a gluteníny.
Genetika
Predpokladá sa, že za vznik celiakie až v 87 % zodpovedajú genetické faktory [15], z toho MHC-HLA II (DQ2/ /DQ8) oblasť je zodpovedná za približne 41 % [16]. Faktory prostredia sa teda podieľajú trinástimi percentami na rozvoji celiakálnej choroby.
Na spustenie patologickej reakcie pri celiakii možno aplikovať model „viacerých zásahov“, kde je nevyhnutný sled udalostí v permisívnom prostredí na prepuknutie ochorenia. Varianty mimo MHC HLA II prispievajú značnou mierou k nastoleniu týchto podmienok [17].
HLA-DQ2/DQ8
Haplotyp DQ2 a DQ8 ľudského leukocytového antigénu druhej triedy (HLA II) predstavujú najlepšie preskúmaný genetický rizikový faktor pre rozvoj celiakie a jeho asociácia s celiakiou bola opísaná už v 70. rokoch 20. storočia [18]. Takmer každý pacient s celiakiou je pozitívný na HLA-DQ2, resp. DQ8 [19].
Heterodimér HLA-DQ2.5 vytvára najsilnejšiu väzbu s fragmentami lepku a prezentuje väčšie spektrum epitopov v porovnaní s HLA-DQ2.2 a DQ8 [20]. Na aktiváciu antigén prezentujúcej bunky (APC) s HLA-DQ2.5 heterodimérom postačuje menšie množstvo fragmentov lepku, ktoré prenikli do lamina propria, k navodeniu prielomovej aktivácie CD4+ T lymfocytom a spusteniu imunopatologickej kaskády.
Podmienkou aktivácie patologickej imunitnej odpovede pri celiakii je prezentácia gluténových peptidov antigén prezentujúcimi bunkami T lymfocytom typu CD4+. Preto je predisponujúci HLA haplotyp sine qua non pre rozvoj celiakie. Výskyt haplotypov HLA-DQ2 a DQ8 sa pohybuje vo svete v rozmedzí 0–28 % a 1–9 % [22]. V Európe je spoločný výskyt HLA-DQ2/DQ8 na úrovni 25–40 % [23], ochorenie sa však rozvinie u menej ako 2 % z nich.
Vlastné pozorovania
Diagnostika celiakie u detí v minulosti (pred rutinnou dostupnosťou vyšetrení anti-tTG IgA a endomyziálnych protilátok (EMA) ako aj aplikácie flexibilných endoskopov) sa opierala o zhod- notenie klinických ťažkostí pacienta, kapsulovú biopsiu duodena, odpoveď na bezlepkovú diétu a reštitúciu architektúry sliznice na bezlepkovej diéte (tzv. opakované biopsie). V našej práci sme sa rozhodli pomocou HLA-DQ haplotypizácie overiť správnosť diagnózy určenej tradičnými metódami v skupine pacientov sledovaných na našej klinike. Zároveň sme aj určili distribúciu haplotypov HLA-DQ v populácii sledovaných celiatikov.
Do súboru boli zaradení pacienti sledovaní pod hlavičkou MKCH 10: K90.0 – Celiakia v gastroenterologickej ambulancii II. detskej kliniky LF UK a DFNsP v Bratislave. Pacienti s diagnózou stanovenou pred rokom 2010 boli vyšetrení v období od 1. 9. 2012 do 1. 9. 2013.
U 306 pacientov vo veku od 3 do 19 rokov bol stanovený haplotyp HLA-DQ sekvenovaním DNA, krv na genetickú analýzu bola odobratá počas rutinného kontrolného vyšetrenia. IgA kompetentných pacientov, ktorým chýbal predisponujúci haplotyp, sme podrobili záťaži lepkom – min. dve jedlá denne s obsahom lepku po dobu troch mesiacov. Pacienti v prípade rozvoja klinických ťažkostí boli inštruovaní kontaktovať ambulanciu. Po troch mesiacoch sme vykonali kontrolné laboratórne vyšetrenie (tzv. prvá kontrola) – hladiny anti-tTG IgA a EMA, krvný obraz, metabolizmus železa a klinické vyšetrenie.
Následne boli pacienti kontrolovaní o šesť mesiacov po prvej kontrole a o 1,5 roka po prvej kontrole s opakovaním sérologického vyšetrenia (anti-tTG IgA, EMA) ako aj vyšetrenia krvného obrazu a metabolizmu železa ako markera rozvoja malabsorpcie.
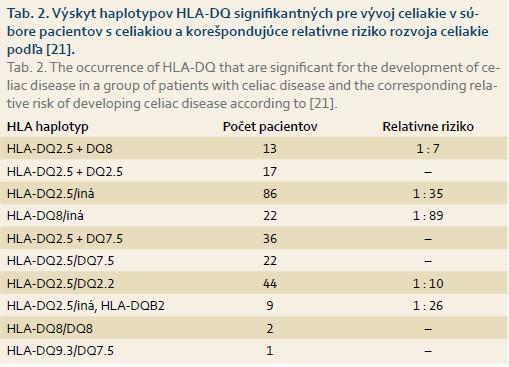
Z uvedeného súboru 82 % (252 zo 306) pacientov malo haplotyp HLA-DQ patognomický pre celiakiu (140 dievčat a 112 chlapcov), 18 % (54 zo 306) pacientov nemalo haplotyp patognomický pre celiakiu. Zastúpenie patognomických haplotypov uvádzame v tab. 2.
U 54 pacientov, ktorí neboli nosičmi HLA-DQ haplotypu asociovaného s celiakiou, bola indikovaná záťaž lepkom. Celkom 50 z 54 (92,6 %) pacientov bolo po opakovaných kontrolách na bežnej strave bez akýchkoľvek laboratórnych a klinických príznakov malabsorpčného syndrómu a boli vyradení zo sledovania.
U štyroch pacientov (7 %) sa na záťaži lepkom rozvinuli klinické ťažkosti v priebehu prvých troch mesiacov, z toho u jedného pacienta došlo k signifikantnému vzostupu anti-tTG IgA a EMA protilátok. Opakované genetické vyšetrenie potvrdilo haplotyp kompatibilný s celiakiou, a preto tento pacient pokračoval na bezlepkovej diéte s diagnózou celiakie verifikovanou expozičným testom. U ostatných troch (5,6 %) pacientov nedošlo k vzostupu hladín špecifických protilátok, avšak vzhľadom na klinické ťažkosti pri konzumácii lepku a ich ústup po opätovnom vysadení ako aj negatívne špecifické IgE protilátky proti lepku sme stav hodnotili ako neceliakálnu gluténovú senzitivitu a pacienti pokračovali v bezlepkovej die?te s vyl??eńte s vylúčenou celiakiou a prognosticky lepšou diagnózou.
Diskusia
Celiakiu si možno predstaviť ako tzv. genetický determinizmus. Jemné naladenie a variácie adaptívnej a špecifickej imunity, expresia receptorov na enterocytoch, parakrinná signalizácia a HLA-DQ haplotyp sú všetko manifestácie genetického kódu. Ak je nastavenie systému „správne“ a pridáme nevyhnutný stimul (lepok) prípadne aj s narušením črevnej bariéry (infekcia gastrointestinálneho traktu), dôjde k prepuknutiu ochorenia. Na druhej strane pri nepermisívnom milieu adaptívnej a humorálnej imunity nedochádza ani pri značnej stimulácii k rozvoju celiakie.
Preto vo svetle genetickej podstaty ochorenia nie je prekvapujúci záver kohortovej prospektívnej štúdia TEDDY z roku 2014 s HLA rizikovou populáciou detí z Nemecka, Fínska, Švédska a USA, že zavedenie lepku pred 17. týždňom alebo po 26. týždni života nie je asociované so zvýšeným rizikom celiakie počas päťročného sledovania. Autori taktiež nepozorovali protektívny vplyv dojčenia na rozvoj celiakie v tejto populáci [24]. Obdobné boli aj výsledky metaanalýzy zavádzania lepku a dojčenia u detí kaukazskej populácie – obdobie zavádzania lepku (v intervale medzi 4.–7. mesiacom), ani súbežné, alebo prolongované dojčenie, či jeho absencia nemá vplyv na prevalenciu celiakie v sledovaných časových intervaloch (3. a 5. rok života) [25]. Oddialenie zavádzania lepku (6.–7. mesiac života) však oddiali nástup ochorenia [26], čo môže pozitívne vplývať na prospievanie jedinca.
Navyše fragmenty gliadínu ako aj gliadín + IgA imunokomplexy prechádzajú do materského mlieka zdravých matiek (bez celiakie) vo významnom množstve [27]. Stimulujeme imunitný systém detí od prvého dňa života? Rozbieha sa subklinická celiakia už od narodenia a naplno prepukne až po zavedení lepku do stravy vo väčšom množstve, tzn. po prekročení stimulačného prahu? Hypotézu prekročenia prahovej stimulácie podporuje aj zistenie, že oneskorené zavedenie lepku oddiali nástup celiakie, ale prevalencia v piatom roku života sa signifikantne nezmení [24].
K porušeniu bariérovej funkcie čreva a prestupu lepku do lamina propria často vzniká pri akútnych gastroenteritídach, obzvlášť rotavírusových. Nebolo by vhodnejšie v populácii s prevalenciou HLA-DQ2/DQ8 na úrovni 40 % do reštitúcie črevnej steny a bariérovej funkcie prechodne podávať bezlepkovú stravu za účelom minimalizovania stimulácie predisponujúcich jedincov?
Sezonalita výskytu celiakie dávaná do súvisu s častejším výskytom akútnych gastrointestinálnych ochorení je dobre dokumentovaná [28].
Neliečená celiakia vedie k významnej morbidite, napriek tomu výskyt predisponujúcich HLA-DQ2/DQ8 sa koncentruje v primárne lepok konzumujúcich spoločenstvách (napr. tzv. Celiac belt v Indii) [29]. Selekčná výhoda tohto haplotypu zatiaľ nie je objasnená.
Záver
V skupine celiatikov boli po prehodno- tení štandardné HLA sérotypy HLA-DQ2 a DQ8 a jeden „neštandardný“ HLA haplotyp, konkrétne HLA-DQ9.3 + + DQ7.5 zastúpené v 99,6 % (251 z 252 pacientov).
Stanovenie HLA-DQ haplotypu je silný nástroj využiteľný aj pri výbere pacientov vyžadujúcich ďalšie monitorovanie pre možný rozvoj celiakie (pacienti s ochoreniami asociovanými s celiakiou, ako napr. autoimunitná tyreoiditída, trizómia 21 a iné). Prognostickú a diagnostickú hodnotu má pre vysoké zastúpenie HLA-DQ2/DQ8 ha- plotypov v populácii však nízku. Aj tu treba zdôrazniť, že ako každá laboratórna metóda má aj HLA haplotypizácia svoje úskalia a je nutná správna interpretácia. Navyše aj pacienti HLA-DQ2/DQ8 negatívni môžu mať celiakiu.
HLA typizácia je ďalší krok smerom k medicíne šitej na mieru a má nesporný benefit pre stratifikáciu pacientov, uľahčenie diagnostiky v sporných prípadoch a sledovanie rizikových populácií pre svoju takmer 100% negatívnu prediktívnu hodnotu. Sama o sebe však nemá významnú pozitívnu prediktívnu hodnotu.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare he they have no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Přijato/Accepted: 20. 11. 2016
MUDr. Michal Kubina
II. detská klinika
LF UK a DFNsP Bratislava
Limbová 1
833 40 Bratislava
Slovenská republika
michalkubina@gmail.com
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Chen L. The gastrointestinal tract. In: Robbins S et al. Robbins and Cotran pathologic basis of disease. 7th ed. Philadelphia: Saunders 2005: 843.
2. Koehler P, Wieser H, Konitzer K (eds). Celiac disease and gluten: multidisciplinary challenges and opportunities. Amsterdam: Academic Press 2014: 46.
3. Tripathi A, Lammers KM, Goldblum S et al. Identification of human zonulin, a physiological modulator of tight junctions, as prehaptoglobin-2. Proc Natl Acad Sci 2009; 106 (39): 16799–16804. doi: 10.1073/pnas.0906773106.
4. Fasano A. Zonulin and Its regulation of intestinal barrier function: the biological door to inflammation, autoimmunity, and cancer. Physiol Rev 2011; 91 (1): 151–175. doi: 10.1152/physrev.00003. 2008.
5. Lammers KM, Lu R, Brownley J et al. Gliadin induces an increase in intestinal permeability and zonulin release by binding to the chemokine receptor CXCR3. Gastroenterology 2008; 135 (1): 194–204. doi: 10.1053/j.gastro.2008.03.023.
6. Heyman M, Abed J, Lebreton C et al. Intestinal permeability in coeliac disease: insight into mechanisms and relevance to pathogenesis. Gut 2012; 61 (9): 1355–1364. doi: 10.1136/gutjnl-2011-300327.
7. Bernardo D, Garrote JA, Fernández-Salazar L et al. Is gliadin really safe for non-coeliac individuals? Production of interleukin 15 in biopsy culture from non-coeliac individuals challenged with gliadin peptides. Gut 2007; 56 (6): 889–890.
8. Nilsen EM, Lundin KE, Krajci P et al. Gluten specific, HLA-DQ restricted T cells from coeliac mucosa produce cytokines with Th1 or Th0 profile dominated by interferon gamma. Gut 1995; 37 (6): 766–776.
9. Sollid LM. Molecular basis of celiac disease. Annu Rev Immunol 2000; 18 (1): 53–81.
10. Lahdenperä A, Ludvigsson J, Fälth-Magnusson K et al. The effect of gluten-free diet on Th1-Th2-Th3-associated intestinal immune responses in celiac disease. Scand J Gastroenterol 2015; 46 (5): 538–549. doi: 10.3109/00365521.2011.551888.
11. Monteleone G, Monteleone I, Fina D et al. Interleukin-21 enhances T-helper cell type I signaling and interferon- g production in Crohn’s disease. Gastroenterology 2005; 128 (3): 687–694.
12. Siegel M, Strnad P, Watts RE et al. Extracellular transglutaminase 2 is catalytically inactive, but is transiently activated upon tissue injury. PloS One 2008; 3 (3): 1861. doi: 10.1371/journal.pone.0001861.
13. Vader LW, de Ru A, van der Wal Y. Specificity of tissue transglutaminase explains cereal toxicity in celiac disease. J Exp Med 2002; 195 (5): 643–649.
14. Petersen J, Montserrat V, Mujico JR et al. T-cell receptor recognition of HLA-DQ2-gliadin complexes associated with celiac disease. Nat Struct Mol Biol 2014; 21 (5): 480–488. doi: 10.1038/nsmb.2817.
15. Ricaño-Ponce I, Wijmenga C, Gutierrez-Achury J et al. Genetics of celiac dis- ease. Best Pract Res Clin Gastroenterol 2015; 29 (3): 399–412. doi: 10.1016/j.bpg.2015.04.004.
16. Gutierrez-Achury J, Zhernakova A, Pulit SL et al. Fine mapping in the MHC region accounts for 18% additional genetic risk for celiac disease. Nature Genetics 2015; 47 (6): 577–578. doi: 10.1038/ng.3268.
17. Koning F. Pathophysiology of celiac dis- ease. J Pediatr Gastroenterol Nutr 2014; 59 (Suppl 1): S1–S4. doi: 10.1097/01.mpg.0000450391.46027.48.
18. Stokes PL, Asquith P, Holmes GK et al. Histocompatibility antigens associated with adult coeliac disease. Lancet 1972; 2 (7769): 162–164.
19. Karell K, Louka AS, Moodie SJ et al. HLA types in celiac disease patients not carrying the DQA1*05-DQB1*02 (DQ2) heterodimer: results from the european genetics cluster on celiac disease. Hum Immunology 2003; 64 (4): 469–477.
20. Vader W, Stepniak D, Kooy Y et al. The HLA-DQ2 gene dose effect in celiac disease is directly related to the magnitude and breadth of gluten-specific T cell responses. Proc Natl Acad Sci U S A 2003; 100 (21): 12390–12395.
21. Megiorni F, Mora B, Bonamico M et al. HLA-DQ and risk gradient for celiac disease. Human Immunology 2009; 70 (1): 55–59. doi: 10.1016/j.humimm.2008.10.018.
22. Gonzalez-Galarza FF, Christmas S, Middleton D et al. Allele frequency net: a database and online repository for immune gene frequencies in worldwide populations. Nucleic Acids Res 2011; 39 (Database issue): D913–919. doi: 10.1093/nar/gkq1128.
23. Sollid LM. Molecular basis of celiac disease. Annu Rev Immunol 2000; 18: 53–81.
24. Aronsson CA, Lee HS, Liu E et al. Age at gluten introduction and risk of celiac disease. Pediatrics 2015; 135 (2): 239–245. doi: 10.1542/peds.2014-1787.
25. Szajewska H, Shamir R, Chmielewska A et al. Systematic review with meta-analysis: early infant feeding and coeliac disease – update 2015. Aliment Pharmacol Ther 2015; 41 (11): 1038–1054. doi: 10.1111/apt.13163.
26. Sarno M, Discepolo V, Troncone R et al. Risk factors for celiac disease. Ital J Pediatr 2015; 41: 57. doi: 10.1186/s13052- 015-0166-y.
27. Chirdo FG, Rumbo M, Añón MC et al. Presence of high levels of non-degraded gliadin in breast milk from healthy mothers. Scand J Gastroenterol 1998; 33 (11): 1186–1192.
28. Ivarsson A, Hernell O, Nyström L et al. Children born in the summer have increased risk for coeliac disease. J Epidemiol Community Health 2003; 57 (1): 36–39.
29. Lionetti E, Catassi C. Co-localization of gluten consumption and HLA-DQ2 and -DQ8 genotypes, a clue to the history of celiac disease. Dig Liver Dis 2014; 46 (12): 1057–1063. doi: 10.1016/j.dld.2014.08. 002.