Eradikace perianálních píštělí u IBD nemocných pomocí metody Advancement Flap a rizikové faktory neúspěšného hojení
Zuzana Šerclová Orcid.org 1, Ondřej Ryska Orcid.org 1, Jaroslav Kalvach2, Jaroslav Marvan3
+ Pracoviště
Souhrn
Komplexní perianální píštěle významně ovlivňují život nemocných s nespecifickými střevními záněty (IBD). Konzervativní léčba nevede ke kompletnímu zhojení. Úspěšnost chirurgické léčby uzavřením vnitřního ústí pomocí posuvného laloku (advancement flap – AF) se pohybuje mezi 24 a 100 %. Cílem studie bylo identifikovat rizikové faktory poruchy hojení AF u pacientů s IBD a zhodnotit dlouhodobé výsledky eradikace píštělí. Metoda: Do studie byli zařazeni nemocní s IBD z prospektivní databáze operovaní metodou AF v letech 2005– 2013. Eradikaci píštělí předcházela dlouhodobá drenáž. Pokračující sekrece ze zevního ústí do tří měsíců od AF byla klasifikována jako selhání hojení laloku. Pokud se objevila píštěl později, byla označena za recidivu. Statistická analýza byla provedena za použití MedCalc 11.4.4.0 softwaru. Výsledky: Celkem 101 pacientů – 59 (58 %) žen, průměrného věku 35 ± 10 let, bylo sledováno 17 (4– 88) měsíců. Interval od první drenáže do eradikace trval 11 (1– 58) měsíců. K primárnímu zhojení došlo u 88 (87 %) pacientů. Recidivu píštěle mělo šest (6 %) nemocných. Konkomitantní léčba neovlivnila hojení. Významným rizikovým faktorem selhání byla rektovaginální lokalizace píštěle (RR: 2,88; CI 95%: 1,1– 7,8). Délka léčby předcházející převzetí do péče na pracoviště autorů byla u pacientů se zhojeným lalokem kratší (0,5 (0– 8) let vs 3 (0– 10) let; p = 0,001). Závěr: Eradikace perianálních píštělí u IBD pomocí AF je úspěšná s nízkou frekvencí selhání (13 %) a recidiv (6 %). Významným rizikovým faktorem nezhojení byla rektovaginální lokalizace píštěle. Časné ošetření perianální nemoci podle protokolu vede k signifikantně vyšší frekvenci zhojení laloku.
Klíčová slova
IBD, advancement flap, komplexní perianální píštěle, rizikové faktoryPerianální píštěle se u Crohnovy nemoci (CN) vyskytují v 17– 43 % a výjimečně se objeví i u nemocných s ulcerózní kolitidou [1]. U většiny pacientů s CN je současně postiženo tenké či tlusté střevo. Vlastní perianální CN významně negativně ovlivňuje kvalitu života nemocných, kteří v 73 % trpí depresivními stavy a ve 13 % mají dokonce sebevražedné myšlenky [2]. Pokud vede biologická léčba ke snížení aktivity nemoci, dochází ke zlepšení kvality života [3]. Píštěle se však touto léčbou kompletně neodstraní, což umožňuje znovuvzplanutí nemoci. Kombinace chirurgické a konzervativní léčby (anti‑TNF, +/ – imunosupresiva) je pravděpodobně efektivnější než samostatná léčba chirurgická či medikamentózní, nicméně dlouhodobá a kvalitní data nejsou k dispozici [4]. Většina prací se věnuje spíše chirurgické drenáži než radikálnějším operacím vedoucím k odstranění píštělí. Jednou z možností úplné eradikace komplexních píštělí (mnohočetné či větvené píštěle zasahující porci svěrače, vaginální píštěle) [5] je metoda ošetření vnitřního ústí pomocí endorektálního posuvného laloku (advancement flap – AF) s předpokladem dlouhodobé remise onemocnění a dlouhodobého zlepšení kvality života. V systematickém přehledu 35 většinou retrospektivních studií publikovaných do roku 2008 je zahrnuto 1 654 pacientů, kteří podstoupili odstranění píštěle pomocí AF, 91 z nich trpělo CN. Pacientky s vaginální píštělí byly z přehledu vyřazeny. Metoda byla úspěšná v 81 % (24– 100 %) u nemocných bez CN a v 64 % (33– 93 %) s CN. Ve 13 % (bez CN) a v 9 % (s CN) byla pooperačně pozorována inkontinence [6]. Technika AF vyžaduje zručnost a zkušenost, což pravděpodobně ovlivňuje úspěšnost a pooperační kontinenci nemocných. V Clevelandské studii je retrospektivně zpracováno 98 nemocných (41 % s CN), kteří podstoupili AF pro komplexní píštěl s celkovou úspěšností 93 % (98 % bez CN, 87 % s CN), kontinence byla po operaci zlepšena oproti stavu před operací.
Z výše uvedených důvodů provádíme eradikaci píštělí pomocí AF u pacientů s nespecifickými střevními záněty (IBD). Podmínkou je relativně klidný nález v rektu, stav bez septických perianálních a pánevních projevů a kontrolovaná luminální nemoc.
Cílem studie bylo na základě dat z prospektivní databáze nemocných identifikovat rizikové faktory poruchy hojení AF u pacientů s IBD.
Sekundárním cílem bylo zhodnotit dlouhodobé výsledky eradikace píštělí technikou AF u těchto nemocných.
Metodika
Do studie byli zařazeni pacienti s IBD indikovaní k pokusu o eradikaci komplexní perianální píštěle metodou AF v letech 2006– 2013 operovaní a sledovaní stejným týmem v Nemocnici Na Bulovce, ÚVN a Nemocnici Hořovice. Pacienti byli po převzetí do péče iniciálně vyšetřeni v celkové anestezii a byla založena dlouhodobá trasovací drenáž všech traktů. Používané drény byly z PVC o šířce 2– 8 mm. V případě přetrvávání infiltrátu nebo recidiv abscesů byla provedena redrenáž píštělí opět v celkové anestezii. Při nedostatečné drenáži byly provedeny discize sekundárních traktů s cílem zjednodušit průběh píštěle. Během celé léčby byla sledována a eventuálně upravována konkomitantní medikace. Drenáž byla ponechána až do provedení AF.
Pacienti byli indikováni k pokusu o eradikaci technikou AF v případě regredujícího lokálního nálezu, bez abscesů, bez stenózy anorekta a bez rozsáhlé zánětlivé infiltrace. Podmínkou byla také kontrolovaná luminální choroba. Vyloučeni byli malnutriční pacienti a pacienti s exacerbací onemocnění.
Před plánovaným AF byla podána antibiotická profylaxe (Metronidazole 1 g i.v. 60 min před operací). Pacienti byli připraveni výplachem rekta – Yalem. Po intubaci byli na operačním stole polohováni na zádech s dolními končetinami v gynekologické poloze. Nejdříve byla provedena revize perinea a sliznice rekta. Při vhodném lokálním nálezu byl lalok vymezen podpichem sliznice fyziologickým roztokem s adrenalinem 1 : 10 000. Báze flapu tvořila zpravidla více než polovinu obvodu anorekta. Po uvolnění slizničního laloku bylo excidováno vnitřní ústí píštěle a provedena sutura defektu ve svěrači (vicryl+ 3/ 0). Celý trakt nebyl excidován. Poté byl lalok postupně vyšit jako záplata 1– 2 cm pod vnitřní ústí. Po operaci byli pacienti sledováni na standardním oddělení. Dostávali pravidelně antibiotika (Metronidazole i.v. 500 mg po 6 hod, po dimisi p.o. 500 mg po 12 hod) a analgetika dle standardního schématu. Perorální příjem byl obnoven v den operace. Dimise proběhla po vyloučení pooperačních komplikací, při dostačující perorální analgezii a po obnově střevní pasáže, zpravidla 2.– 3. pooperační den.
K hodnocení stavu píštěle byla používána standardní metoda – fistula drainage assessment – FDA [5]. V pooperačním sledování byla nezhojená píštěl s přetrvávající sekrecí zevním ústím do tří měsíců od operace klasifikována jako selhání hojení flapu. Nález píštěle více než tři měsíce od operace byl označen jako recidiva. V obou případech byla píštěl znovu zadrénována a po splnění výše zmíněných indikačních kritérií byl proveden nový AF.
K identifikaci rizikových faktorů hojení a recidivy byly prospektivně sledovány parametry zahrnující předoperační medikaci, typ píštěle, věk pacienta nebo délku trvání choroby.
Pro účely popisné statistiky jsou data prezentována jako střední hodnoty (medián) s odpovídajícím rozptylem nebo jako průměr se směrodatnou odchylkou. K hodnocení kategorických dat byl použit chí‑ kvadrát test. K hodnocení jednotlivých skupin pacientů byl použit Mann‑Whitney test.
Statistická významnost byla definována jako hodnota p < 0,05. Pro statistickou analýzu byl použit software MedCalc 11.4.4.0.
Výsledky
Do studie bylo zařazeno celkem 101 pacientů – 59 (58 %) žen a 42 (42 %) mužů, průměrného věku 35 ± 10 let. Ve většině případů se jednalo o perianální píštěle při CN – 91 (90 %) pacientů, v 10 % s ulcerózní kolitidou. V celé skupině bylo provedeno celkem 118 AF. Ve 101 (86 %) případech se jednalo o primární AF, ve třech (2,5 %) případech o plánovanou eradikaci druhé píštěle a u devíti nemocných byl lalok opakován pro selhání hojení či recidivu (14 operací). Interval od prvního vyšetření v celkové anestezii do pokusu o eradikaci píštěle činil 11 (1– 58) měsíců. Během tohoto období byly v průměru provedeny dvě (1– 22) intervence (redrenáž, discize) u jednoho pacienta. Nemocní byli sledováni celkem 17 (4– 88) měsíců.
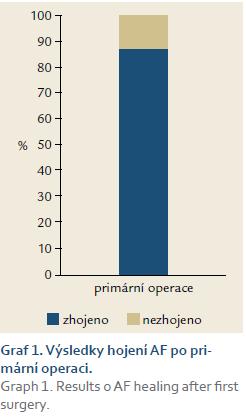
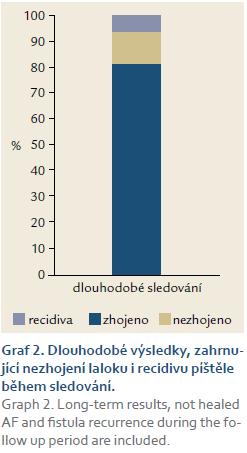
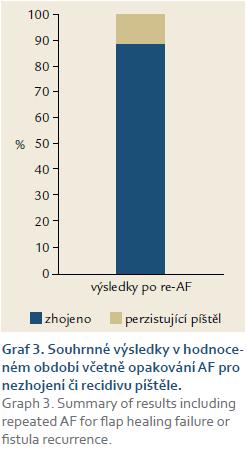
Ke zhojení laloku po primární operaci došlo u 88 (87 %) (graf 1) pacientů. K recidivě došlo ve sledovaném období u šesti (6 %) nemocných (graf 2). Při opakování laloku pro nezhojení či recidivu byla metoda v hodnoceném období celkově úspěšná u 90 (86 %) pacientů (graf 3).
Ve skupině s nezhojeným AF byl střední věk pacientů v době diagnózy IBD a perianálního postižení 26 (8– 57) let, resp. 32 (18– 56) let, což bylo srovnatelné s hodnotami ve skupině se zhojeným lalokem – 25,0 (11– 40) let (p = 0,55) a 31 (19– 44) let (p = 0,79).
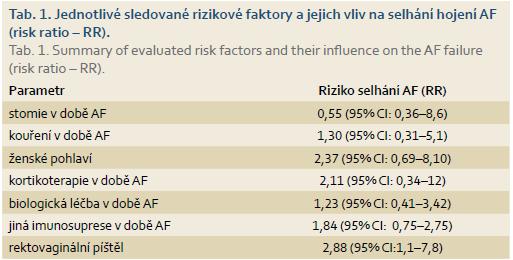
Konkomitantní konzervativní léčba významně neovlivnila hojení. Střevní derivace v době provedení AF nesignifikantně zvyšovala úspěšnost hojení. U žen byl pozorován trend k horšímu hojení. Rektovaginální píštěl byla významným rizikovým faktorem selhání hojení AF (tab. 1).
Délka léčby předcházející převzetí do péče na pracoviště autorů byla u pacientů se zhojeným a nezhojeným lalokem 0,5 (0– 8) let, resp. 3 (0– 10) roky; p = 0,001.
Diskuze
Zhojení píštělí metodou AF u IBD pacientů bylo popsáno na menších sestavách. Ve starší floridské studii byla úspěšnost u 71 % z 26 nemocných [8], v již zmíněné sestavě z Clevelandu u 87 % ze 40 nemocných. Obě pracoviště se pacienty s IBD zabývají dlouhodobě, jiné práce udávají mnohem horší výsledky [6].
Vysoká úspěšnost zhojení píštěle v naší sestavě (87 %) mohla být způsobena též zkušeností s IBD pacienty, ale také popsaným protokolem, který zahrnuje poměrně dlouhý interval od první transanální drenáže k indikaci k AF (11 (1– 58) měsíců). Tento interval umožňuje zhojení perianálních zánětlivých změn a pečlivou eradikaci abscesů. Podobný postup byl publikován u nemocných s komplexní kryptoglandulární píštělí (nemocní bez IBD), u kterých tříměsíční drenáž předcházející AF umožnila přihojení laloku v 78 % [9].
Nízká frekvence recidivy (6 %) je jistě ovlivněna středně dlouhým intervalem sledování (medián 17 měsíců), nicméně nemocní jsou prospektivně sledováni i nadále, což umožní i zhodnocení dlouhodobějších výsledků.
Mezi faktory, které by mohly ovlivnit hojení, byla sledována konkomitantní konzervativní léčba. Užívání kortikoidů v abdominální chirurgii zvyšuje frekvenci pooperačních komplikací [10] a byl popsán trend horšího hojení AF [13,14]. V naší sestavě nebylo hojení AF u nemocných užívajících kortikoidy z indikace luminální nemoci ovlivněno.
Biologická léčba a případně imunosupresiva v kombinaci s chirurgickou léčbou snižují symptomy perianální nemoci [3] a vedou ke statisticky významně kratšímu intervalu k remisi (p < 0,05) a delší době do recidivy než samostatné podání biologické léčby (2,6 (SD 0,7) měsíců) či samotná operace (3,6 (SD 0,5) měsíců) [11]. V těchto sestavách je chirurgickou léčbou myšlena drenáž a ne definitivní ošetření vnitřního ústí píštěle, tedy její příčiny. V naší sestavě nebyla úspěšnost zhojení biologickou léčbou ani imunosupresivy významně ovlivněna. Kuřáctví je nezávislým faktorem agresivního chování nemoci [12]. V naší sestavě se úspěšnost eradikace píštělí u kuřáků nelišila od nekuřáků.
Jediným faktorem, který významně negativně ovlivňoval hojení, byl anorektovaginální typ píštěle (2,88; (95% CI: 1,1– 7,8). Shodný trend byl zaznamenán u ženského pohlaví, což souvisí s tím, že 30 % pacientek mělo píštěl směřující do vaginy (18/ 59). Nižší úspěšnost metody u vaginálních píštělí je opakovaně popsána v literatuře [14,15], ale přesto dochází ke zhojení po této lokální operaci v 54– 71 % [15]. Ostatní možnosti chirurgické léčby vaginálních píštělí jsou mnohem komplexnější a většinou vyžadují střevní derivaci, často trvalou. V naší sestavě došlo k primárnímu zhojení u 62 % nemocných (13/ 18), proto AF v této indikaci ve shodě s literaturou [14] považujeme za vhodnou možnost léčby. Nicméně konkomitantní konzervativní léčba by měla být u těchto pacientek maximalizována.
Závěr
Eradikace perianálních píštělí u IBD pomocí metody AF je úspěšná s nízkou frekvencí selhání (13 %) a recidiv (6 %). Opakované provedení AF pro neúspěšnost či recidivu zvyšuje procento pacientů bez píštělí (86 %) ve středně dlouhém sledovaném období (17 (4– 88) měsíců). Jediným významným rizikovým faktorem nezhojení laloku a pokračování píštěle byla anorektovaginální lokalizace píštěle. Časné ošetření perianální nemoci podle protokolu, včetně opakovaných drenáží, vede k signifikantně vyšší frekvenci zhojení laloku. Výsledky je třeba ověřit v delším časovém intervalu sledování.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Doručeno/Submitted: 30. 12. 2014
Přijato/Accepted: 29. 1. 2015
MUDr. Zuzana Šerclová
Chirurgické oddělení
Nemocnice Hořovice a. s.
K nemocnici 1106/14, 268 31 Hořovice
sercl@seznam.cz
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Schwartz DA, Pemberton JH, Sandborn WJ. Diagnosis and treatment of perianal fistulas in Crohn disease. Ann Intern Med 2001; 135(10): 906– 918.
2. Mahadev S, Young JM, Selby W et al. Self‑ reported depressive symptoms and suicidal feelings in perianal Crohn‘s disease. Colorectal Dis 2012; 14(3): 331– 335. doi: 10.
1111/ j.1463‑ 1318.2011.02613.x.
3. Ng SC, Plamondon S, Gupta A et al. Prospective assessment of the effect on quality of life of anti‑tumour necrosis factor therapy for perineal Crohn‘s fistulas. Aliment Pharmacol Ther 2009; 30(7): 757– 766. doi: 10.1111/ j.1365‑ 2036.2009.04088.x.
4. Yassin NA, Askari A, Warusavitarne J et al.
Systematic review: the combined surgical and medical treatment of fistulising perianal Crohn‘s disease. Aliment Pharmacol Ther 2014; 40(7): 741– 749. doi: 10.1111/ apt.12906.
5. Sandborn WJ, Fazio VW, Feagan BG et al.
AGA technical review on perianal Crohn’s disease. Gastroenterology 2003; 125(5): 1508– 1530.
6. Soltani A, Kaiser AM. Endorectal advancement flap for cryptoglandular or Crohn‘s fistula‑ in‑ano. Dis Colon Rectum 2010; 53(4): 486– 495. doi: 10.1007/ DCR.0b013e 3181ce 8b01.
7. Jarrar A, Church J. Advancement flap repair: a good option for complex anorectal fistulas. Dis Colon Rectum 2011; 54(12): 1537– 1541. doi: 10.1097/ DCR.0b013e31822d7ddd.
8. Joo JS, Weiss EG, Nogueras JJ et al. Endorectal advancement flap in perianal Crohn‘s disease. Am Surg 1998; 64(2): 147– 150.
9. Van der Hagen SJ, Baeten CG, Soeters PB et al. Staged mucosal advancement flap for the treatment of complex anal fistulas: pretreatment with noncutting Setons and in case of recurrent multiple abscesses a diverting stoma. Colorectal Dis 2005; 7(5): 513– 518.
10. Yamamoto T, Allan RN, Keighley MR. Risk factors for intra‑ abdominal sepsis after surgery in Crohn‘s disease. Dis Colon Rectum 2000; 43(8): 1141– 1145.
11. Sciaudone G, Di Stazio C, Limongelli P
et al. Treatment of complex perianal fistulas in Crohn disease: infliximab, surgery or combined approach. Can J Surg 2010; 53(5): 299– 304.
12. Lakatos PL, Czegledi Z, Szamosi T et al. Perianal disease, small bowel disease, smoking, prior steroid or early azathioprine/ biological therapy are predictors of disease behavior change in patients with Crohn‘s disease. World J Gastroenterol 2009; 15(28): 3504– 3510.
13. Mizrahi N, Wexner SD, Zmora O et al. Endorectal advancement flap: are there predictors of failure? Dis Colon Rectum 2002; 45(12): 1616– 1621.
14. Sonoda T, Hull T, Piedmonte MR et al. Outcomes of primary repair of anorectal and rectovaginal fistulas using the endorectal advancement flap. Dis Colon Rectum 2002; 45(12): 1622– 1628.
15. Valente MA, Hull TL. Contemporary surgical management of rectovaginal fistula in Crohn‘s disease. World J Gastrointest Pathophysiol 2014; 5(4): 487– 495. doi: 10.4291/ wjgp.v5.i4.487.