Autoimunní hepatitida po očkování proti covidu-19
Veronika Pítová1, Jan Šperl Orcid.org 1, Pavel Taimr Orcid.org 1, Ondřej Fabián2, Tomáš Miřejovský3, Libor Janoušek Orcid.org 4, Jaroslav Chlupáč5,6, Julius Špičák Orcid.org 1, Soňa Fraňková Orcid.org 1
+ Pracoviště
Souhrn
V této kazuistice popisujeme případ 61letého muže, který byl přijat k hospitalizaci pro únavu a ikterus < 3 týdny po očkování proti viru SARS-CoV-2 první dávkou vakcíny Comirnaty (Pfizer/BioNTech). Z provedených vyšetření (anamnéza, laboratorní vyšetření, zobrazovací metody, jaterní biopsie) byla diagnostikována autoimunní hepatitida. U pacienta se rozvinulo akutní jaterní selhání a nezareagoval na podání kortikoidů. Byl zařazen na čekací listinu a podstoupil transplantaci jater, která vedla k záchraně života pacienta.
Klíčová slova
autoimunitní hepatitida, COVID-19, očkování, jaterní selhání
Úvod
Autoimunní hepatitida (AIH) je zánětlivé onemocnění jater charakterizované zvýšenými hodnotami sérových aminotransferáz (ALT, AST), přítomností autoprotilátek, hypergamaglobulinemií a typickým histologickým nálezem. Klinicky se může manifestovat akutním jaterním selháním, častější je však chronický průběh vedoucí ke vzniku jaterní fibrózy až jaterní cirhózy. Základem dlouhodobé léčby je podávání kortikoidů a/nebo azathioprinu. V případě akutního jaterního selhání či dekompenzované jaterní cirhózy má být zvážena možnost transplantace jater.
Popis případu
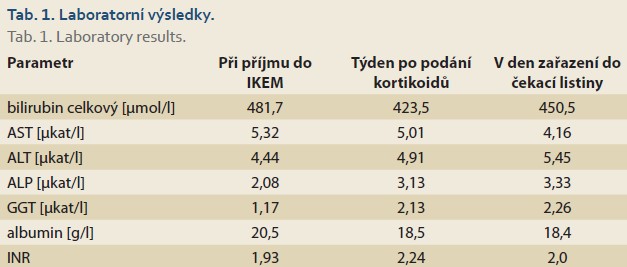
Popisujeme případ 61letého muže, který byl přijat do okresní nemocnice ve Středočeském kraji 24. 5. 2021 pro únavu a ikterus. Pacient byl obézní (BMI 37 kg/m2), léčil se s arteriální hypertenzí trojkombinací antihypertenziv (ACE inhibitor, betablokátor, diuretikum) a pro hyperurikemii užíval allopurinol. V posledním roce u něj nedošlo k žádné změně farmakoterapie. Před 2 roky mu byla zjištěna mírná elevace aktivit jaterních enzymů v rámci interního předoperačního vyšetření před náhradou pravého kolenního kloubu, blíže však vyšetřen nebyl. Dne 2. 5. 2021 byl pacient očkovaný proti viru SARS-CoV-2 první dávkou vakcíny Comirnaty (Pfizer/BioNTech). Již po očkování pociťoval zvýšenou únavu, která neustupovala, a 21. 5. 2021 jeho manželka poprvé zpozorovala zežloutnutí kůže a sklér. Při příchodu do nemocnice měl bilirubin 482,3 µmol/l, AST 16,46 µkat/l, ALT 23 µkat/l, ALP 3 µkat/l, GGT 2 µkat/l, albumin 33 g/l, INR 1,3, negativní sérologii hepatitidy A, B a C. Byl mu proveden ultrazvuk a CT břicha, které byly bez zjevné patologie žlučových cest, nebylo prokázáno ložiskové postižení jater, byla zjištěna cholecystolitiáza a jaterní steatóza. Přesto byla provedena endoskopická retrográdní cholangiopankreatografie (ERCP) s papilotomií a zavedením biliárního stentu, konkrementy ve žlučových cestách prokázány nebyly. Při dalším pátrání po příčině jaterního onemocnění byla zjištěna hypergamaglobulinemie a bylo vysloveno podezření na autoimunní hepatitidu. Pacient byl referován do IKEM a 11. 6. 2021 byl přijat na lůžko Kliniky hepatogastroenterologie. Vyloučili jsme: virové hepatitidy (A, B, C, E), deficit 1-antitrypsinu, hladina ceruloplasminu byla v normě, negativní byla sérologie HIV, CMV, EBV a HSV, negativní protilátky anti-AMA, anti-LKM, anti-SMA, ANCA. Byla zjištěna pozitivita antinukleárních (ANA) protilátek (titr 1: 2 560) a elevace IgG (45 g/l; norma 5,40–18,2 g/l). Vybrané laboratorní výsledky jsou uvedeny v tab. 1.
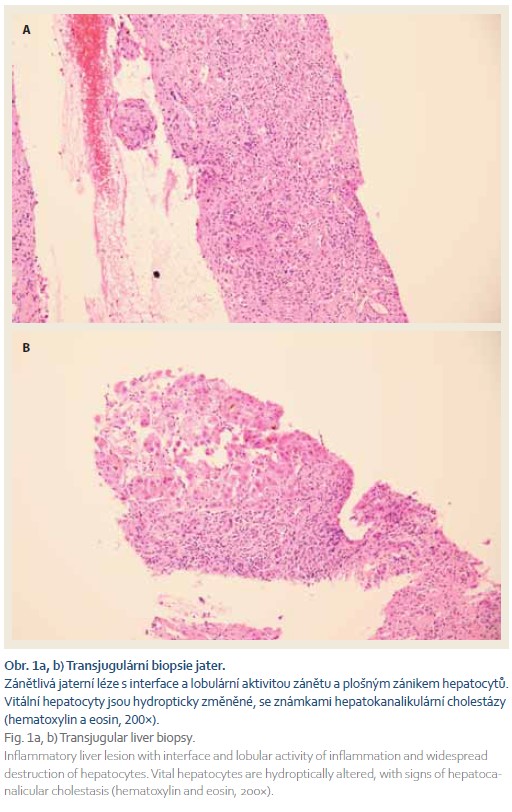
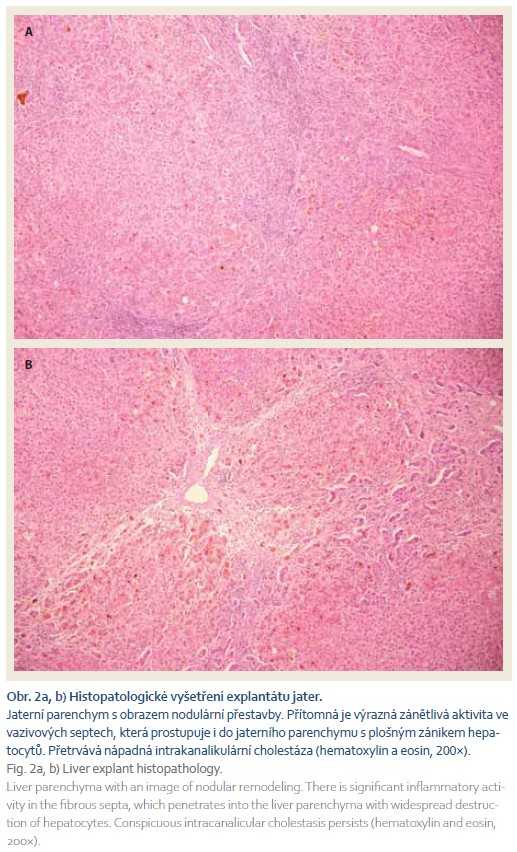
Vzhledem ke koagulopatii jsme provedli jaterní biopsii transjugulární cestou. Histologické vyšetření (obr. 1a a 1b) bylo v souladu s klinicky zvažovanou diagnózou AIH (zánětlivá jaterní léze s lobulární aktivitou zánětu, plazmocyty a centrolobulární nekrózou) a byla popsána již septální fibróza. Zahájili jsme léčbu kortikoidy (prednison 80 mg/den), která vedla pouze k mírnému poklesu bilirubinu, avšak nedošlo ke zlepšení syntetické funkce jater. Rozhodli jsme se zahájit protokolární vyšetření před transplantací jater, která neshledala kontraindikaci k výkonu, a pacient byl 25. 6. 2021 zařazen do čekací listiny (WL) k ortotopické transplantaci jater. V průběhu hospitalizace došlo k rozvoji jaterní encefalopatie a anasarky. Dne 22. 7. 2021 pacient podstoupil ortotopickou transplantaci jater. Výkon byl chirurgicky nekomplikovaný kromě vyšší krevní ztráty (8 litrů) s nutností náhrady krevními deriváty, z toho důvodu bylo rozhodnuto o ponechání 4 longet (tzv. packing) a naplánování revize břišní dutiny. Dne 24. 7. 2021 byla provedena operační revize, odstranění longet a definitivní sutura rány. Extubace byla následována kvalitativní poruchou vědomí přetrvávající do 27. 7. 2021. Imunosuprese byla podávána ve standardní trojkombinaci tacrolimus, mykofenolát mofetil a prednison. Rozvoj funkce jaterního štěpu byl rychlý, jaterní testy postupně klesaly až na normální hodnoty. Pacient byl propuštěn do domácí péče 23. pooperační den. V explantátu jater byla zjištěna cirhotická přestavba, vysoká zánětlivá aktivita v septech a uzlech jaterního parenchymu (interface aktivita). Místy byly přítomny i plošné nekrózy a početnější plazmocyty, tedy změny typické pro AIH. Histologické vyšetření explantátu jater je na obr. 2a a 2b.
Diskuze
Rozvoj AIH po očkování mRNA vakcínou proti covidu-19 bylo v literatuře doposud popsáno v několika kazuistických sděleních. První případ popsali Bril et al již v březnu 2021 [1]. Jednalo se o 35letou ženu, zdravotnici z Alabamy (USA), 3 měsíce po porodu. Během těhotenství se u ní rozvinula gestační hypertenze, pro kterou byla zahájena léčba labetalolem. Dne 4. 1. 2021 byla očkována první dávkou vakcíny Comirnaty. Týden po očkování došlo k rozvoji pruritu, následně ikteru a 13. den po vakcinaci byla přijata k hospitalizaci. Na základě laboratorních a histologických výsledků byla stanovena diagnóza AIH a nasazena léčba kortikoidy. Dva měsíce po nasazení kortikoidů s postupným snižováním dávek u ní došlo k normalizaci jaterních testů a bilirubinu. V reakci na vydání tohoto článku bylo publikováno několik dalších případů rozvoje AIH po vakcinaci různými vakcínami proti covidu-19. Jejich souhrn je uveden v tab. 2.
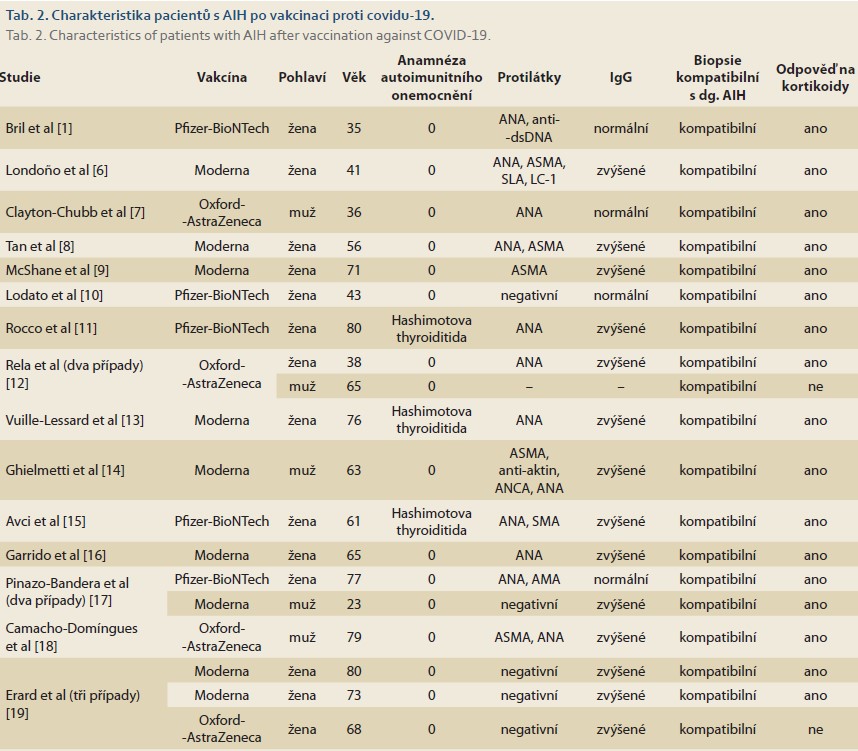
V naprosté většině případů došlo ke zlepšení klinického stavu a laboratorního nálezu pacientů po zahájení léčby kortikoidy. Ve dvou z publikovaných zahraničních případů také došlo k rozvoji jaterního selhání. První pacient transplantaci jater odmítl a druhá pacientka byla sice zařazena na čekací listinu k transplantaci jater, ale do 3 dnů zemřela. I v našem případě došlo k rozvoji jaterního selhání, které však neskončilo fatálně díky možnosti a provedení ortotopické transplantace jater. Z explantátu zjištěná jaterní cirhóza mohla být způsobena dříve nediagnostikovanou AIH, v úvahu rovněž připadá nealkoholická steatohepatitida jako preexistující onemocnění jater (pacient byl obézní, negoval nadměrný přísun alkoholu). Mohlo tedy jít o tzv. flare AIH navozený očkováním či o de novo vzniklou AIH způsobující akutní jaterní selhání nasedající na chronické selhání jater při jaterní cirhóze (ACLF – acute-on-chronic liver failure). Histologické vyšetření explantátu jater v této otázce nebylo diagnosticky přínosné, ve stadiu jaterní cirhózy obvykle steatóza, která je jinak nedílnou součástí histologické diagnózy nealkoholické steatohepatitidy, není přítomna, neboť vymizí s pokročilým jaterním onemocněním. V literatuře jsou popsány případy rozvoje autoimunitní hepatitidy po očkování proti viru chřipky a viru hepatitidy A [2,3]. Přesný mechanizmus vzniku není jasný, ale roli pravděpodobně hraje genetická predispozice, expozice cizím antigenům homologním s lidskými antigeny (tzv. molekulární mimikry) a stimulace imunitního systému složkami vakcíny [4]. Vojdani et al zjistili, že protilátky proti spike proteinu viru SARS-CoV-2 mají také vysokou afinitu k proteinům lidských tkání, mimo jiné i nukleárnímu antigenu. mRNA vakcíny od firem Pfizer/BioNTech a Moderna vedoucí k tvorbě protilátek proti covidu-19 mohou u predisponovaných jedinců vést k rozvoji autoimunitního onemocnění [5]. K rozvoji AIH může dojít nejen po mRNA vakcínách, ale i po vektorových či jiných vakcínách. Adjuvans vakcín mohou přispět k jejich imunogenicitě [6]. Přesný mechanizmus vzniku autoimunitních onemocnění po vakcinaci různými vakcínami proti covidu-19 zatím není zcela jasný.
Závěr
Očkování mRNA vakcínou proti viru SARS-CoV-2 bylo následováno rozvojem akutního jaterního selhání při AIH krátce po podání první dávky vakcíny. Mohlo se jednat o velmi vzácný nežádoucí účinek vakcinace, přesto je zřejmé, že přínosy vakcinace jsou mnohonásobně vyšší než její potenciální rizika.
ORCID autorů
J. Šperl ORCID 0000-0001-8619-2610,
O. Fabián ORCID 0000-0002-0393-2415,
T. Miřejovský ORCID 0000-0002-4616-4321,
J. Chlupáč ORCID 0000-0003-1482-6105.
Doručeno/Submitted: 29. 8. 2022
Přijato/Accepted: 3. 11. 2022
MUDr. Veronika Pítová
Klinika hepatogastroenterologie
Institut klinické a experimentální medicíny
Vídeňská 1958/9
140 21 Praha 4
veronika.pitova@ikem.cz
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Bril F, Al Diffalha S, Dean M et al. Autoimmune hepatitis developing after coronavirus disease 2019 (COVID-19) vaccine: Causality or casualty? J Hepatol 2021; 75(1): 222–224. doi: 10.1016/j.jhep.2021.04.003.
2. Sasaki T, Suzuki Y, Ishida K et al. Autoimmune hepatitis following influenza virus vaccination: Two case reports. Medicine (Baltimore) 2018; 97(30): e11621. doi: 10.1097/MD.0000000000011621.
3. Berry PA, Smith-Laing G. Hepatitis A vaccine associated with autoimmune hepatitis. World J Gastroenterol 2007; 13(15): 2238–2239. doi: 10.3748/wjg.v13.i15.2238.
4. Segal Y, Shoenfeld Y. Vaccine-induced autoimmunity: the role of molecular mimicry and immune crossreaction. Cell Mol Immunol 2018; 15(6): 586–594. doi: 10.1038/cmi.2017.151.
5. Vojdani A, Kharrazian D. Potential antigenic cross-reactivity between SARS-CoV-2 and human tissue with a possible link to an increase in autoimmune diseases. Clin Immunol 2020; 217: 108480. doi: 10.1016/j.clim.2020.108 480.
6. Londoño MC, Gratacós-Ginès J, Sáez-Peñataro J. Another case of autoimmune hepatitis after SARS-CoV-2 vaccination – still casualty? J Hepatol 2021; 75(5): 1248–1249. doi: 10.1016/j.jhep.2021.06.004.
7. Clayton-Chubb D, Schneider D, Freeman E et al. Autoimmune hepatitis developing after the ChAdOx1 nCoV-19 (Oxford-AstraZeneca) vaccine. J Hepatol 2021; 75(5): 1249–1250. doi: 10.1016/j.jhep.2021.06.014.
8. Tan CK, Wong YJ, Wang LM et al. Autoimmune hepatitis following COVID-19 vaccination: True causality or mere association? J Hepatol 2021; 75(5): 1250–1252. doi: 10.1016/j.jhep.2021.06.009.
9. McShane C, Kiat C, Rigby J et al. The mRNA COVID-19 vaccine – A rare trigger of autoimmune hepatitis? J Hepatol 2021; 75(5): 1252–1254. doi: 10.1016/j.jhep.2021.06.044.
10. Lodato F, Larocca A, D‘Errico A et al. An unusual case of acute cholestatic hepatitis after m-RNABNT162b2 (Comirnaty) SARS-CoV-2 vaccine: Coincidence, autoimmunity or drug-related liver injury. J Hepatol 2021; 75(5): 1254–1256. doi: 10.1016/j.jhep.2021.07.005.
11. Rocco A, Sgamato C, Compare D et al. Autoimmune hepatitis following SARS-CoV-2 vaccine: May not be a casualty. J Hepatol 2021; 75(3): 728–729. doi: 10.1016/j.jhep.2021.05.038.
12. Rela M, Jothimani D, Vij M et al. Auto-immune hepatitis following COVID vaccination. J Autoimmun 2021; 123: 102688. doi: 10.1016/j.jaut.2021.102688.
13. Vuille-Lessard É, Montani M, Bosch J et al. Autoimmune hepatitis triggered by SARS-CoV-2 vaccination. J Autoimmun 2021; 123: 102710. doi: 10.1016/j.jaut.2021.102710.
14. Ghielmetti M, Schaufelberger HD, Mieli-Vergani G et al. Acute autoimmune-like hepatitis with atypical anti-mitochondrial antibody after mRNA COVID-19 vaccination: A novel clinical entity? J Autoimmun 2021; 123: 102706. doi: 10.1016/j.jaut.2021.102706.
15. Avci E, Abasiyanik F. Autoimmune hepatitis after SARS-CoV-2 vaccine: New-onset or flare-up? J Autoimmun 2021; 125: 102745. doi: 10.1016/j.jaut.2021.102745.
16. Garrido I, Lopes S, Simões MS et al. Autoimmune hepatitis after COVID-19 vaccine – more than a coincidence. J Autoimmun 2021; 125: 102741. doi: 10.1016/j.jaut.2021.102741.
17. Pinazo-Bandera JM, Hernández-Albújar A, García-Salguero AI et al. Acute hepatitis with autoimmune features after COVID-19 vaccine: coincidence or vaccine-induced phenomenon? Gastroenterol Rep (Oxf) 2022; 10: goac014. doi: 10.1093/gastro/goac014.
18. Camacho-Domínguez L, Rodríguez Y, Polo F et al. COVID-19 vaccine and autoimmunity. A new case of autoimmune hepatitis and review of the literature. J Transl Autoimmun 2022; 5: 100140. doi: 10.1016/j.jtauto.2022.100140.
19. Erard D, Villeret F, Lavrut PM et al. Autoimmune hepatitis developing after COVID 19 vaccine: Presumed guilty? Clin Res Hepatol Gastroenterol 2022; 46(3): 101841. doi: 10.1016/ j.clinre.2021.101841.