Subkutánní infliximab v léčbě refrakterních pacientů s Crohnovou nemocí – pilotní studie imunogenicity léčiva
Karin Černá 1, Dana Ďuricová1, Martin Lukáš1, Naděžda Machková1, Veronika Hrubá1, Kristýna Kaštylová1, Katarína Mitrová1, Marta Kostrejová1, Kristýna Kubíčková1, Štěpán Peterka1, Martin Kolář1, Jakub Jirsa1, Gabriela Vojtěchová1, Milan Lukáš1
+ Pracoviště
Souhrn
Úvod: Přestože je infliximab (IFX) dosud „zlatým standardem“ biologické léčby Crohnovy nemoci (CN), jeho účinnost se může lišit v závislosti na mnoha faktorech. Jedním z nich je individuální reakce pacienta na lék. Významným klinickým problémem je imunogenicita IFX, kdy může až u 60 % léčených pacientů dojít k vývoji protilátek proti léčivu, což vede ke ztrátě odpovědi na léčbu a/nebo k nežádoucím reakcím na terapii. Od roku 2020 je k léčbě nemocných s CN k dispozici infliximab k subkutánnímu podání (IFX-SC), jehož farmakokinetika se vyznačuje stabilní a vysokou údolní koncentrací léčiva (TL – trough level) v krevním oběhu. Je možné, že jedním z důsledků této vlastnosti IFX-SC je jeho nižší míra imunogenicity. Předkládáme prospektivní studii sledování pacientů s diagnózou CN s velmi těžkým až refrakterním průběhem, kteří byli léčeni IFX-SC. Cílem studie bylo sledování imunogenicity IFX-SC včetně sledování dynamiky TL a protilátek proti léčivu (anti-IFX). Je popsána dynamika klinických, zobrazovacích a laboratorních markerů CN v průběhu jednoho roku sledování a léčby. Materiál a metodika: Do studie bylo zařazeno 23 pacientů s diagnózou CN s anamnézou selhání 2–6 předchozích linií biologické léčby, přičemž jednou z proběhlých terapií byl nitrožilní infliximab (IFX-IV). Pacienti byli rozděleni do dvou ramen indukční léčby na základě přítomnosti anti-IFX. Udržovací terapie představovala 120 mg s.c. à 14 dní, v případě potřeby intenzifikace se jednalo o 240 mg s.c. à 14 dní. Nemocní byli sledováni v týdnech (W – week) W0, W4, W14, W30 a W52, přičemž byly zaznamenány Harvey-Bradshawův index (HBI), sérová hladina C-reaktivního proteinu (CRP), fekální koncentrace kalprotektinu (FC), hladina léku (TL IFX) a anti-IFX. Dále bylo stanoveno endoskopické a ultrasonografické skóre nemoci (SES-CD a IUS) a u všech pacientů byl vyšetřen haplotyp HLA DQA1*05. Data byla analyzována pomocí softwaru MedCalc® s použitím neparametrických statistických metod a binární logistické regrese. Výsledky: U 13 z 23 pacientů (56,5 %) bylo zaznamenáno 52týdenní setrvání na léčbě IFX-SC se signifikantním poklesem všech sledovaných klinických, zobrazovacích i laboratorních markerů aktivity CN. V průběhu terapie došlo u 8 ze 16 vstupně anti-IFX pozitivních osob k sérokonverzi k negativním anti-IFX (50 %). Žádný z pacientů léčených IFX-SC ve W52 již nepotřeboval konkomitantní léčbu imunomodulátory. Během 52 týdnů terapie nebyla ve sledované kohortě zaznamenána ani jedna nová senzibilizace infliximabem. Závěr: Subkutánní cesta podání infliximabu může být vhodným a úspěšným řešením v situaci, kdy je žádoucí reindukce terapie infliximabem, a to včetně pacientů s přítomností neutralizujících protilátek proti léčivu.
Klíčová slova
infliximab, subkutánní infliximab, Crohnova nemoc, protilátky proti infliximabu, imunogenicita, údolní koncentrace infliximabu, biologická léčba, idiopatické střevní záněty

Úvod
Infliximab (IFX) je biologický léčivý přípravek používaný v Evropské unii k léčbě idiopatických střevních zánětů (IBD – inflammatory bowel disease) od roku 1999. K vývoji léčiva přispěl mj. americký lékař a mikrobiolog slovenského původu Ján T. Vilček, jehož studie [1] se podílely na patentu uděleném v roce 1995 společnosti Centocor na léčivý přípravek s komerčním názvem Remicade. Od roku 2013 jsou schváleny k použití tzv. biosimilární verze IFX, např. molekuly CT-P13, SB2 nebo GP2013. Biosimilární přípravky jsou léky, které jsou podobné originálnímu biologickému léku a prokázaly svou podobnost ve struktuře, účinnosti a bezpečnosti.
Infliximab je dosud jedním z nejpoužívanějších a neúčinnějších biologických léčiv v terapii IBD. Účinnost IFX závisí na mnoha faktorech – na závažnosti onemocnění, lokalizaci zánětu, dávkování léčiva, komedikaci, intervalu podávání a na individuální reakci jednotlivých pacientů na lék.
Jedním z problémů provázejících biologickou terapii IFX je skutečnost, že velká chimérická molekula glykoproteinové povahy se může stát cílem pacientova imunitního systému. Vznikají protilátky proti léčivu, důsledkem čehož je ztráta odpovídavosti na léčbu a/nebo vznik nežádoucích polékových reakcí včetně časných a/nebo oddálených reakcí přecitlivělosti. Primární neodpovídavost na terapii IFX je udávána v rozmezí 10–30 % [2], sekundární ztráta odpovědi se může ročně týkat až 13 % léčených nemocných [3]. Údaje o imunogenicitě IFX u nemocných s IBD se značně liší, mohou se vyskytovat až u 60 % pacientů [4]. Selhání biologické terapie jedním biologikem z důvodu jeho imunogenicity je rizikovým faktorem pro neodpovídavost v dalších liniích biologické terapie [5].
V roce 2020 byl k použití u nemocných s IBD schválen biosimilární CT-P13 k podkožnímu podání (IFX-SC). Kromě uživatelských benefitů vyplývajících ze subkutánní aplikace léku (tedy komfort pro pacienta, úspora času pro pacienta i zdravotnické zařízení, vyřešení problému s podáním léku u osob s komplikovaným žilním vstupem apod.) se záhy ukázalo, že IFX-SC vede k dosažení signifikantně vyšších údolních koncentrací léčiva (trough levels, TL IFX) a tyto hladiny jsou v čase stabilní. Stabilita TL IFX bez velkých výkyvů je nejspíše důvodem dalšího benefitu IFX-SC, kterým je nižší imunogenicita léčiva [6].
Cílem této práce bylo sledování imunogenicity a výskytu neutralizujících protilátek proti IFX-SC (anti-IFX) u refrakterních pacientů s Crohnovou nemocí (CN), kteří v minulosti selhali na dvou a více liniích biologické léčby, přičemž jedním z dříve podávaných biologik byl IFX-IV. Sekundárním cílem práce byla analýza 52týdenního setrvání na léčbě IFX-SC, faktorů ovlivňujících tuto perzistenci na terapii a vývoj klinických a laboratorních markerů u nemocných s roční perzistencí na terapii IFX-SC.
Pacienti a metodika
V prospektivní studii sledování pacientů jednoho terciárního IBD centra tvořili kohortu nemocní s diagnózou CN s velmi těžkým až refrakterním průběhem, kteří selhali na dvou a více liniích biologické léčby, přičemž jedním z dříve podávaných/selhaných biologik byl IFX-IV. U uvedených nemocných rozhodl ošetřující lékař o „switchování“ ze stávajícího biologického léčiva na IFX-SC.
Před indukcí léčby IFX-SC byla u všech pacientů vyšetřena aktuální hladina anti-IFX v séru. Pacienti bez cirkulujících anti-IFX následně dostali dvě indukční dávky IFX-IV v dávce 5 mg/kg v rozmezí 14 dnů a 4 týdny po druhé nitrožilní indukční dávce pokračovali v udržovací léčbě IFX-SC 120 mg à 14 dní. U pacientů s přítomností anti-IFX v séru byla indukční léčba realizována čtyřmi subkutánními injekcemi IFX-SC v dávce 120 mg jednou týdně, následnou udržovací terapii rovněž představoval IFX-SC v dávce 120 mg jednou za 2 týdny. Pokud ošetřující lékař rozhodl o potřebě intenzifikace terapie IFX-SC, dávka léku byla navýšena na 240 mg jednou za 2 týdny.
U všech sledovaných pacientů byly v týdnech (W – week) W0, W4, W14, W30 a W52 zaznamenány: Harvey-Bradshawův index (HBI), sérová hladina C-reaktivního proteinu (CRP), fekální koncentrace kalprotektinu (FC) a hladina neutralizujících protilátek proti infliximabu (anti-IFX) detekovaná s pomocí „drug sensitive“ testu. Kromě W0 byla ve všech časových bodech provedena vyšetření sérových koncentrací infliximabu (TL IFX). Ve W0, W30 a W52 bylo provedeno ultrasonografické vyšetření střev a stanoven index aktivity nemoci (IUS – intestinal ultrasound score) dle metodiky popsané Kucharczikem et al [7]. Ve W0 a W52 byli nemocní vyšetřeni endoskopicky se stanovením endoskopického skóre aktivity nemoci (SES-CD – simple endoscopic score for Crohn’s disease) [8]. U všech nemocných byl vyšetřen haplotyp HLA DQA1*05 (rs 2097432) metodou qPCR.
Data byla analyzována s pomocí softwaru MedCalc® Statistical Software version 22.007 (MedCalc Software Ltd, Belgie). Kvantitativní proměnné byly testovány na normalitu pomocí Shapiro-Wilkova testu, a protože nebylo prokázáno normální rozdělení dat, byly použity neparametrické statistické přístupy. Spojité proměnné byly prezentovány jako mediány a interkvartilové rozmezí (IQR), u kategoriálních proměnných byly uvedeny jejich absolutní a relativní počty. K porovnání analyzovaných skupin byly použity Kruskal-Wallisův a chí-kvadrát test. K analýze faktorů ovlivňujících 52týdenní perzistenci na léčbě IFX-SC byla použita binární logistická regrese. Za signifikantní byla přijata hodnota p ≤ 0,05.
Projekt byl schválen Etickou komisí Klinického centra ISCARE č. 2022/IVa.
Výsledky
V týdnu W0 zahájilo studii celkem 23 pacientů s CN, 12 mužů a 11 žen s mediánem věku 31 let (IQR 26–35 let). Medián trvání CN byl 14 let (IQR 11–18,75 roku) a medián času od poslední podané dávky IFX-IV byl 8 let (IQR 4,5–11 let).
U nemocných zařazených do studie byl IFX-SC třetí až sedmou linií biologické terapie (medián předchozího počtu biologik byl roven 4, IQR 3–5). Hlavním důvodem pro ukončení léčby IFX-IV v minulosti byla infuzní alergická reakce u 3 pacientů (13 %), závažné infekční komplikace u 2 pacientů (9 %), těžká paradoxní psoriáza u 1 nemocného (4 %) a zejména ztráta odpovědi na terapii s progresí nemoci u 17 pacientů (74 %). Ke dříve podávaným biologickým léčivům kromě IFX-IV patřily adalimumab, ustekinumab, vedolizumab, etrolizumab a risankizumab, čtyři pacienti byli v minulosti léčeni mj. duální terapií (tedy kombinací adalimumab + vedolizumab a infliximab + ustekinumab).
Základní klinické údaje o pacientech uvádí tab. 1.
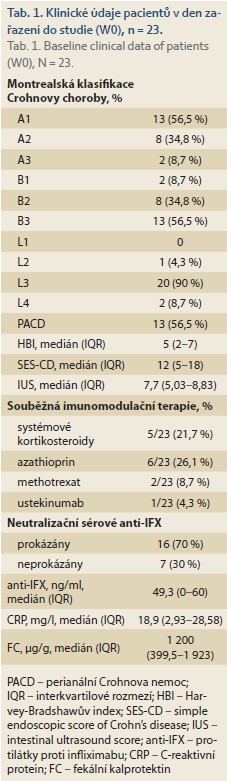
Setrvání na léčbě IFX-SC v průběhu sledovaných 52 týdnů
Ve sledovaném období 52 týdnů došlo k vyřazení dvou nemocných ze studie již po první indukční dávce léku. V týdnech W14 a W30 pokračovalo ve studii 18 z původních 23 pacientů (78,3 %) a v týdnu W52 celkem 13 z původního počtu pacientů (56,5 %). Příčiny ukončení léčby IFX-SC v průběhu 52týdenního sledování shrnuje tab. 2.
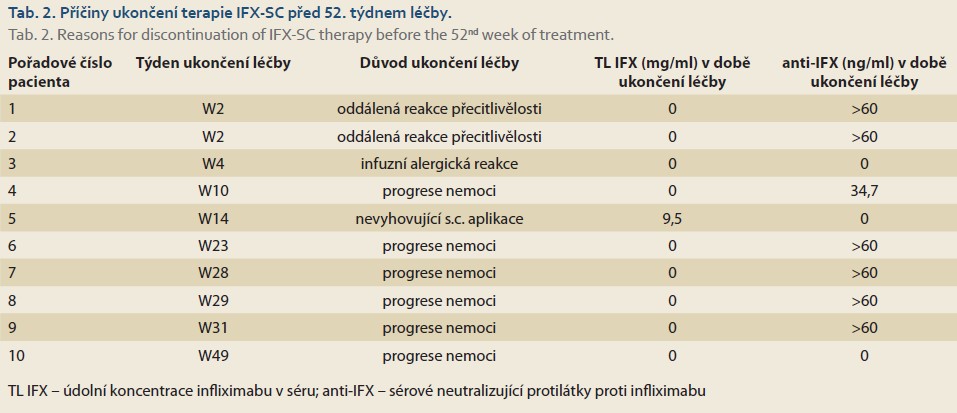
Lze konstatovat, že k selhání léčby IFX-SC došlo především u osob s nulovými TL IFX a s perzistencí anti-IFX.
Na začátku sledování (ve W0) užívalo 13 z 23 pacientů (56,5 %) systémové imunomodulátory, tj. kortikosteroidy, thiopuriny nebo methotrexát, jeden nemocný kromě IFX-SC dostával též ustekinumab (tzv. duální terapie). Na konci sledovaného období ve W52 neužíval ani jeden ze 13 pacientů setrvávajících na léčbě žádný z uvedených imunomodulátorů, pouze mladý muž s těžkým průběhem nemoci nadále dostával duální léčbu IFX-SC v kombinaci s ustekinumabem.
V průběhu 52 týdnů sledování nedošlo ani u jednoho nemocného ke vzniku klinicky závažné infekce, která by vedla k nutnosti ukončení léčby. Nebyly zaznamenány závažné kožní ani kloubní komplikace s možnou souvislostí s podáním IFX-SC.
Vývoj tvorby neutralizačních anti-IFX
V průběhu 52 týdnů terapie došlo k sérokonverzi z původní anti-IFX pozitivity k negativním anti-IFX u 8 z původně 16 anti-IFX pozitivních osob (50 %). Všichni pacienti po této sérokonverzi setrvali po dobu 52 týdnů na léčbě IFX-SC. Týdne W52 v klinické remisi dosáhli pouze pacienti s negativními anti-IFX (graf 1).
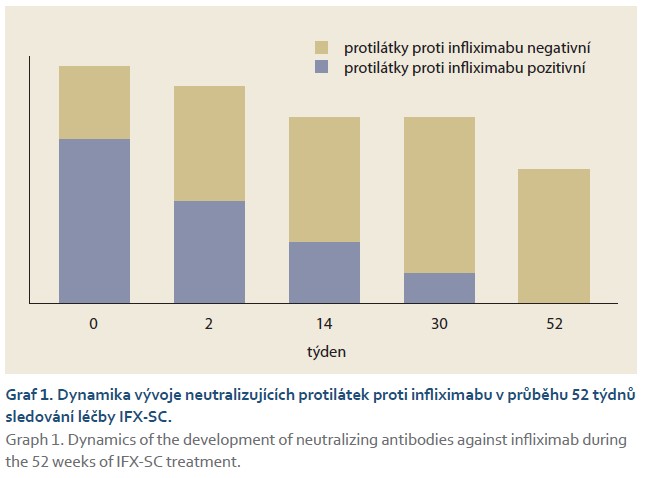
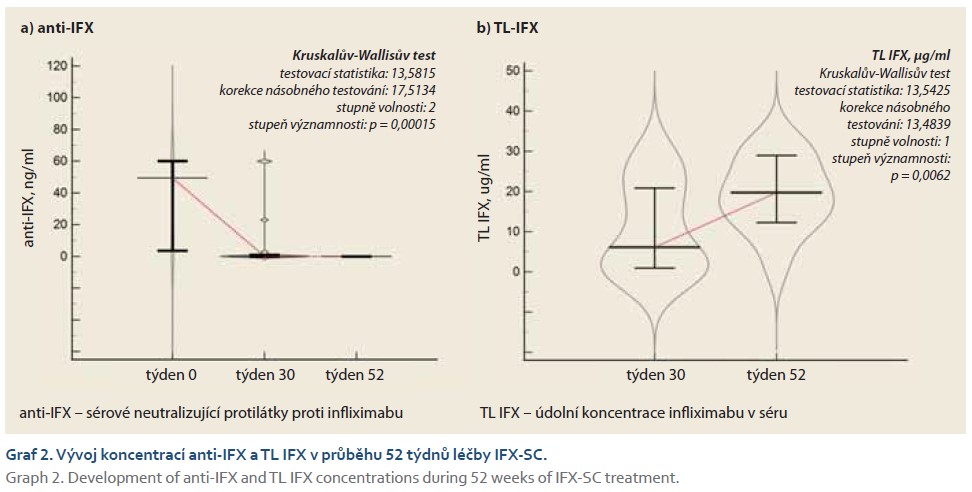
Sérokonverze z anti-IFX pozitivního do anti-IFX negativního stavu byla provázena signifikantním vzestupem TL IFX (graf 3).
U žádného pacienta, který zahajoval léčbu s negativními anti-IFX, nedošlo nově v průběhu léčby k indukci tvorby protilékových protilátek.
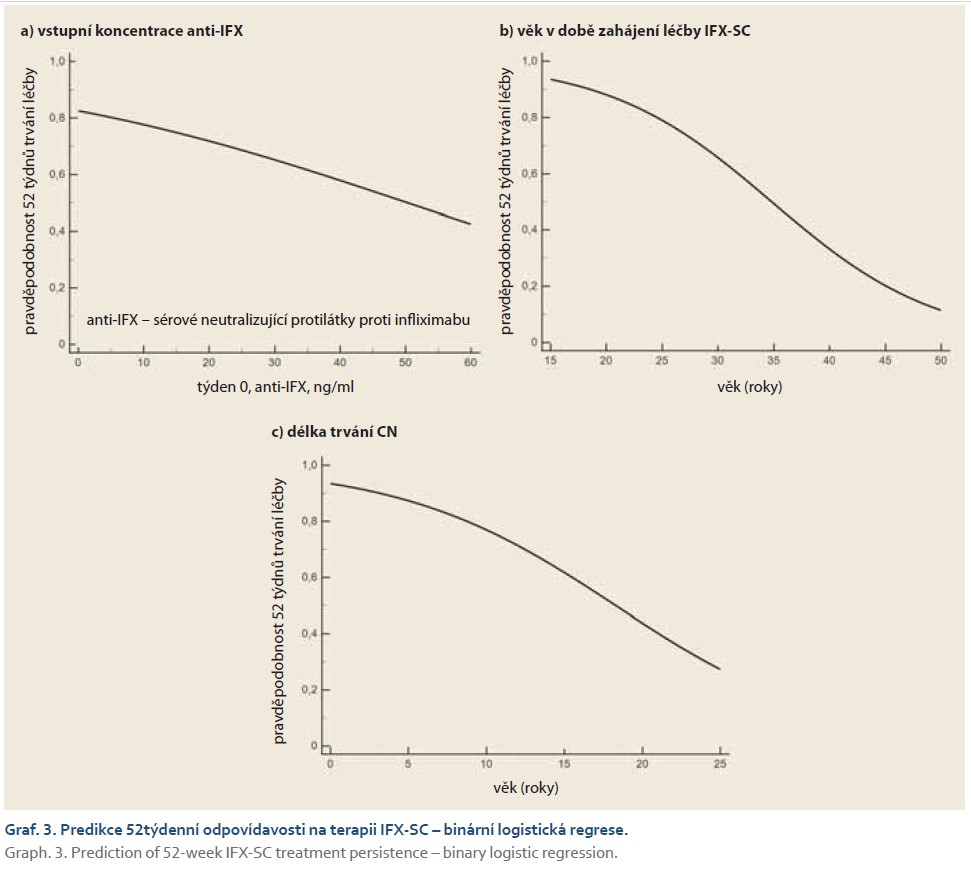
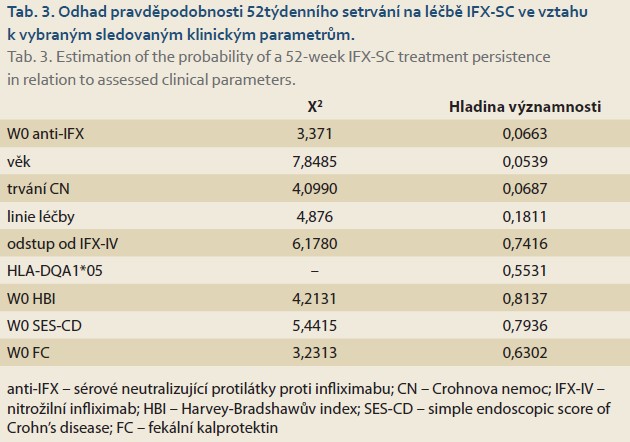
Binární logistickou regresí nebyl identifikován žádný vstupní faktor, který by byl signifikantně sdružen s 52týdenní odpovídavostí na léčbu IFX-SC. Genotyp HLA-DQA1*05 ani vstupní hodnoty tíže systémového a střevního zánětu neměly vliv na roční perzistenci na léčbě. Trend ke statistické významnosti byl patrný u hladin anti-IFX, věku pacientů a u délky trvání CN (tab. 3, grafy 3a–c).
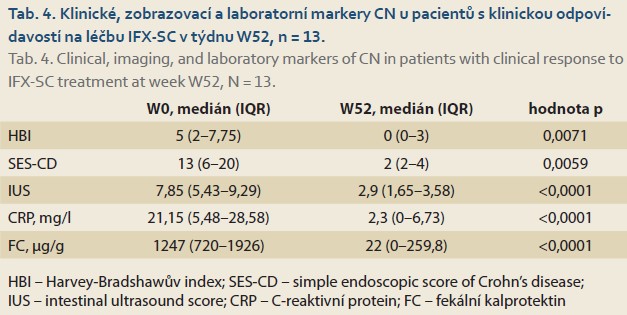
Klinický stav pacientů v týdnu W52
Celkem 56,5 % zařazených pacientů dosáhlo W52. U všech je patrný signifikantní pokles všech sledovaných klinických, zobrazovacích i laboratorních markerů aktivity CN (tab. 4).
Diskuze
Předkládaná studie je první českou prací, která poukazuje na možnost reindukce infliximabu subkutánním podáním u pacientů, kteří dříve selhali na léčbě nitrožilním léčivem. Za důležitou lze považovat skutečnost, že u poloviny z pacientů, kteří léčbu IFX-SC zahajovali s přítomností neutralizujících protilátek proti infliximabu, došlo během několika týdnů léčby k sérokonverzi a k vymizení těchto protilátek. Během ročního sledování pak ani u jednoho ze vstupně anti-IFX negativních pacientů nedošlo k nové senzibilizaci s tvorbou protilátek proti léčivu.
Možná nižší míra imunogenicity by mohla být slibnou výhodou IFX-SC. Tradičně se má za to, že subkutánně podávaná biologika jsou imunogennější než intravenózní léčba díky teoretické expozici antigen prezentujícím buňkám v epidermis a dermis [9], ačkoli objektivní důkazy podporující vyšší tvorbu protilátek po podání léčiva touto cestou jsou rozporuplné [10]. Existuje několik dosud diskutovaných hypotéz, proč je IFX-SC méně imunogenní než IFX-IV. Patří k nim mj.:
1. teorie o stabilitě sérových hladin léčiva, která při subkutánním podání brání velkým výkyvům „peak-trough“, a tudíž snižuje imunogenicitu molekuly IFX [6], nebo
2. hypotéza o tom, že vyšší TL IFX-SC spouští mechanizmy navození tolerance v nadbytku antigenu nebo snižují tvorbu imunogenních komplexů antigen-protilátka [11]. Zde ovšem není zcela jasné, proč by se tyto mechanizmy přednostně aktivovaly při stabilních mírných hladinách léčiva při subkutánní léčbě, a nikoli při vysokých „peak“ koncentracích při intravenózní léčbě.
Na nižší imunogenicitu IFX-SC upozornily již dřívější práce. Ve Schreiberově otevřené, randomizované, placebem kontrolované studii podkožního podávání infliximabu pacientům s aktivní CN [12] byly analyzovány anti-IFX a jejich neutralizační potenciál s pomocí „drug-tolerant“ metody ECLIA. V této studii se u 7 z 12 pacientů (58 %) v intravenózní větvi ve srovnání s pouhými 3 z 30 (10 %) v subkutánní větvi objevily do 30. týdne protilátky proti léčivu. Po 54 týdnech terapie mělo v subkutánním rameni studie signifikantně méně pacientů neutralizační protilátky proti léčivu proti intravenózní větvi (18 vs. 37 %; p = 0,019). V největší dosud publikované reálné kohortě 181 pacientů po změně léčby z intravenózní na subkutánní se protilátky proti léčivu objevily pouze u 14 pacientů (8 %) [13].
V naší kohortě dosáhlo 52týdenní perzistence na léčbě IFX-SC 56,5 % pacientů. Jelikož se jednalo o refrakterní pacienty po několikanásobném selhání jiných biologických léčiv (pro některé z léčených subjektů byl IFX-SC až sedmou linií biologické terapie), lze tuto „treatment persistence“ považovat za uspokojivou. Pro takto specifickou skupinu pacientů je však dosud k dispozici málo dat z reálné klinické praxe. Pro srovnání lze uvést výsledky studie německých autorů [14], kteří publikovali 70% setrvání na léčbě IFX-SC do týdne W12 u 10 pacientů s předchozí senzibilizací na IFX-IV.
Studie prokázala, že podkožní podání infliximabu významně zvyšuje bezpečnost léčby, protože v týdnu W52 nebylo potřebné u žádného z pacientů pokračujících v terapii IFX-SC podávat konkomitantní imunosupresiva a/nebo kortikosteroidy. Nedávná D‘Haensova studie [15] prokázala srovnatelnou klinickou účinnost a farmakokinetiku IFX u pacientů, kteří dostávali IFX-SC se souběžnými perorálními imunomodulátory (azathioprin nebo methotrexát), nebo bez nich.
Přísný výběr refrakterních pacientů s anamnézou přechozích terapeutických selhání je příčinou nízké četnosti sledované kohorty. Extrapolace získaných dat je proto omezená a jejich reprezentativnost pro standardní IBD populaci nízká. Naše data naznačují, že selhání terapie IFX-SC by mohlo být pravděpodobnější u osob se vstupně vysokými koncentracemi anti-IFX, toto riziko by mohlo dále stoupat s věkem a s délkou trvání nemoci. V žádné z uvedených analýz nebylo dosaženo statistické signifikance, nicméně tyto parametry byly identifikovány jako rizikové faktory neodpovídavosti na IFX terapii již v předchozích studiích [16–18].
Přínos studie lze spatřovat v poukázání na to, že nová subkutánní cesta podání infliximabu může být vhodným a úspěšným řešením v situaci, kdy je žádoucí reindukce terapie infliximabem u nemocných s komplikovanou anamnézou, dokonce i u pacientů s přítomností neutralizujících protilátek proti léčivu. Naše poznatky naznačují možnost optimalizace terapeutických režimů a zlepšení klinických výsledků u pacientů s obtížně zvladatelnou CN. Zobecnění závěrů malé pilotní studie však není možné a k potvrzení našich výsledků a rozšíření znalostí o podání subkutánního infliximabu v léčbě CN budou potřebné další rozsáhlé studie. Tyto výzkumy by měly také zahrnovat sledování bezpečnosti a snášenlivosti tohoto terapeutického přístupu.
ORCID autorů
K. Černá ORCID 0000-0003-1593-5899,
D. Ďuricová ORCID 0000-0002-6090-3522,
M. Lukáš ORCID 0000-0003-3946-3953,
V. Hrubá ORCID 0000-0001-5218-0363,
K. Kaštylová ORCID 0000-0002-8024-1626,
K. Mitrová ORCID 0000-0002-1836-3745,
K. Kubíčková ORCID 0000-0003-1257-9171,
Š. Peterka ORCID 0000-0002-6458-4565,
M. Kolář ORCID 0000-0001-9501-0604,
G. Vojtěchová ORCID 0000-0002-7911-470X,
M. Lukáš ORCID 0000-0002-1463-3840.
Doručeno/Submitted: 7. 8. 2023
Přijato/Accepted: 9. 9. 2023
MUDr. Karin Černá
Klinické a výzkumné centrum pro střevní záněty
Klinické centrum ISCARE a. s.
1. LF UK Českomoravská 2510/19
190 00 Praha 9
cernak@iscare.cz
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Knight DM, Trinh H, Le J et al. Construction and initial characterization of a mouse-human chimeric anti-TNF antibody. Mol Immunol 1993; 30(16): 1443–1453. doi: 10.1016/ 0161-5890(93)90106- l.
2. Schnitzler F, Fidder H, Ferrante M et al. Long-term outcome of treatment with infliximab in 614 patients with Crohn’s disease: results from a single-centre cohort. Gut 2009; 58(4): 492–450. doi: 10.1136/gut.2008.155812.
3. Assa A, Hartman C, Weiss B et al. Long-term outcome of tumor necrosis factor alpha antagonist’s treatment in pediatric Crohn’s disease. J Crohns Colitis 2013; 7(5): 369–376. doi: 10.1016/j.crohns.2012.03.006.
4. Tighe D, McNamara D. Clinical impact of immunomonitoring in the treatment of inflammatory bowel disease. World J Gastroenterol 2017; 23(3): 414–425: doi: 10.3748/wjg.v23.i3. 414.
5. Albshesh A, Taylor J, Savarino EV et al. Effectiveness of Third-Class Biologic Treatment in Crohn’s Disease: A Multi-Center Retrospective Cohort Study. J Clin Med 2021; 10(13): 2914. doi: 10.3390/jcm10132914.
6. Little RD, Ward MG, Wright E et al. Therapeutic Drug Monitoring of Subcutaneous Infliximab in Inflammatory Bowel Disease-Understanding Pharmacokinetics and Exposure Response Relationships in a New Era of Subcutaneous Biologics. J Clin Med 2022; 11(20): 6173. doi: 10.3390/jcm11206173.
7. Kucharzik T, Wilkens R, D‘Agostino MA et al. STARDUST Intestinal Ultrasound study group. Early Ultrasound Response and Progressive Transmural Remission After Treatment with Ustekinumab in Crohn’s Disease. Clin Gastroenterol Hepatol 2023; 21(1): 153–163.e12. doi: 10.1016/j.cgh.2022.05.055.
8. Daperno M, D’Haens G, Van Assche G et al. Development and validation of a new, simplified endoscopic activity score for Crohn’s disease: the SES-CD. Gastrointest Endosc 2004; 60(4): 505–512. doi: 10.1016/s0016-5107(04)01878-4.
9. Malissen B, Tamoutounour S, Henri S. The origins and functions of dendritic cells and macrophages in the skin. Nat Rev Immunol 2014; 14(6): 417–428. doi: 10.1038/nri3683.
10. Kim H, Alten R, Cummings F et al. Innovative approaches to biologic development on the trail of CT-P13: Biosimilars, value-added medicines, and biobetters. MAbs 2021; 13(1): 1868078. doi: 10.1080/19420862.2020.1868078.
11. Bar-Yoseph H, Pressman S, Blatt A et al. Infliximab-Tumor Necrosis Factor Complexes Elicit Formation of Anti-Drug Antibodies. Gastroenterology 2019; 157(5): 1338–1351.e8. doi: 10.1053/j.gastro.2019.08.009.
12. Schreiber S, Jang BI, Borzan V et al. Novel Formulation of CT-P13 (Infliximab Biosimilar) for Subcutaneous Administration: Initial Results from a Phase I Open-Label Randomized Controlled Trial in Patients with Active Crohn’s Disease. Gastroenterology 2018; 154: 1371. doi: 10.1016/S0016-5085(18)34477-9.
13. Smith PJ, Critchley L, Storey D et al. Efficacy and Safety of Elective Switching from Intravenous to Subcutaneous Infliximab (Ct-P13): A Multi-Centre Cohort Study. J Crohn’s Colitis 2022; 16(9): 1436–1446. doi: 10.1093/ecco-jcc/jjac053.
14. Husman J, Matthes K, Gilger M et al. Subcutaneous infliximab in IBD patients with previous immunogenic failure of intravenous infliximab. J Crohns Colitis 2023; 17(Suppl): i920.
15. D‘Haens G, Reinisch W, Schreiber S et al. Comparison of combination subcutaneous infliximab and an immunomodulator versus subcutaneous infliximab monotherapy: post-hoc analysis of a randomised clinical trial (UEG Week 2021). 2021 [online]. Dostupné z: https: //programme.ueg.eu/week2021/#/details/presenta- tions/1284.
16. Kennedy NA, Heap GA, Green HD et al. UK Inflammatory Bowel Disease Pharmacogenetics Study Group. Predictors of anti-TNF treatment failure in anti-TNF-naive patients with active luminal Crohn’s disease: a prospective, multicentre, cohort study. Lancet Gastroenterol Hepatol 2019; 4(5): 341–353. doi: 10.1016/S2468-1253(19)30012-3.
17. Lionetti P, Bronzini F, Salvestrini C et al. Response to infliximab is related to disease duration in paediatric Crohn‘s disease. Aliment Pharmacol Ther 2003; 18(4): 425–431. doi: 10.1046/j.1365-2036.2003.01672.x.
18. Juillerat P, Sokol H, Froehlich F et al. Factors associated with durable response to infliximab in Crohn’s disease 5 years and beyond: a multicenter international cohort. Inflamm Bowel Dis 2015; 21(1): 60–70. doi: 10.1097/MIB. 0000000000000225.