Obezita a dětská ledvina
Zlatko Marinov1, Cecília Marinová2
+ Pracoviště
Souhrn
Chronické onemocnění ledvin a nealkoholická statóza jater jsou celosvětovými problémy veřejného zdraví. Vedle diabetu se řadí obezita k jejich hlavním rizikovým faktorům. Běžná obezita je chronické metabolické onemocnění, které spouští řetězení dalších civilizačních onemocnění. Tuková tkáň je největším endokrinním orgánem v těle a při jejím nadměrném zmnožení dochází k pozvolným, ale rozsáhlým kardiometabolickým změnám podmíněným inzulinorezistencí, prozánětlivým stavem a endoteliální dysfunkcí s nevratnou centrální dysregulací energetické homeostázy. Renální a hepatální následky běžné obezity, přestože se rozvíjejí v dospělosti, mohou mít svůj původ v dětské nadváze.
Klíčová slova
chronické onemocnění ledvin, dětská obezita, kardiometabolické riziko, nealkoholická steatóza jater, programováníÚvod
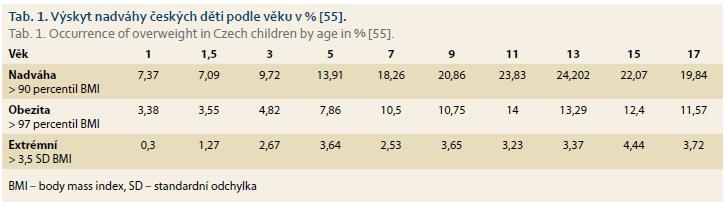
Výskyt dětské nadváhy překonal nejpesimističtější předpoklady z 80. let 20. století. Celosvětově trpí podle Světové zdravotnické organizace (WHO) obezitou více než 42 milionů dětí mladších 5 let. V Evropské unii (EU) žije přes 3 miliony obézních dětí a předpokládá se, že u 400 tisíc dětí je každý rok obezita nově diagnostikována. Za čtvrtstoletí epidemie obezity v ČR došlo ke dvojnásobnému nárůstu nadváhy v rámci celého populačního spektra a podle průzkumu antropometrických údajů u dětí v ČR v roce 2016 [1] k zpětinásobení počtu obézních dětí. Nadváhou (> 90 percentil body mass indexu (BMI)) v dětství trpí každé čtvrté dítě, obezitou (> 97 percentil BMI) každé sedmé a extrémní obezitou (nad 3,5 směrodatné odchylky BMI) čtyři ze sta dětí.
Nejrozšířenější běžná dětská obezita je charakterizována pozvolným nástupem a k jejímu rozvoji musí být splněna podmínka proobezitogenního genomu a podmínka neadekvátně zvýšeného příjmu potravy k energetickému výdeji v rámci obezitogenního prostředí. V ČR je okolo 154 tisíc dětí do 16 let s běžnou obezitou, z toho 85 tisíc dětí s morbidní (> 3 směrodatné odchylky BMI) a 34 tisíc s monstrózní obezitou (rozvoj ektopické tukové tkáně). Výskyt nadváhy českých dětí v jednotlivých věkových kategoriích v roce 2011 je uveden v tab. 1. Následky způsobené dětskou obezitou jsou v počátku reverzibilní, a proto se časné stanovení a léčba stávají významnou klinickou výzvou. Na jedné straně se v pediatrické praxi, na rozdíl od nealkoholické jaterní steatózy (NAFLD – non-alcoholic fatty liver disease), s nefrologickými následky dětské obezity běžně nesetkáváme, na druhé straně, o co diskrétnější v dětství, o to s výraznějšími projevy nefropatií a nealkoholické jaterní fibrózy (NASH – non-alcoholic steatohepatitis) se budeme setkávat u chronicky obézních pacientů v dospělosti. NAFLD je nejčastější celosvětovou hepatopatií a NASH se stává hlavním podkladem transplantačního programu jater [2]. Chronické onemocnění jater a ledvin na podkladě dětské obezity mají shodné patofyziologické mechanizmy a vzájemně se nejen doprovází, ale i potencují.
Etiologie dětské obezity
V dětské populaci se v současné době vyskytuje běžná obezita ve více než 99 % případů. Výskyt dětské obezity na podkladě jiných onemocnění je ojedinělý. S poklesem výdeje energie při snížení bazálního metabolizmu se setkáváme při hypotyreóze. Patologicky zvýšená chuť k jídlu je při nadbytku kortizolu u Cushingova syndromu nebo při podávání kortikoidů. Patologicky odchylné tělesné složení vlivem úbytku svalové hmoty a nadbytku tukové tkáně pozorujeme při deficitu růstového hormonu, při poškození ventromediálního hypothalamu v důsledku nádoru oblasti III. mozkové komory a po neurochirurgických operacích. Vrozená primární hypothalamická dysregulace na podkladě mendelovské dědičnosti je u mikrodelece 16p11.2, Praderova-Williho syndromu, Bardetova-Biedlova syndromu, Cohenova, Alströmova, fragilního X a syndromu WAGR, Albrigtovy hereditární osteodystrofie a u mutace SIMi. Sekundární hypothalamická dysregulace je při léčbě některými psychofarmaky a u syndromu polycystických ovarií. Narušení hypothalamické signalizace na molekulární úrovni se vyskytuje u mutací genu pro leptin, leptinový receptor, POMC, prohormon-konvertázu 1, MC3-R nebo genu pro MC4-R.
Poškození ledvin při renálním programování
Na vzniku jak běžné obezity, tak onemocnění ledvin se mohou podílet vzájemné vstupní podmínky [3], které se následně potencují v bludném kruhu. Koexistence celé řady iniciálních faktorů, které jsou shrnuty v tab. 2, začíná prakticky od početí a je klíčová v raném dětském věku. Obezita matek při koncepci negativně ovlivňuje programming energetické rovnováhy plodu [4]. Rizikové faktory pro vznik obezity v následujícím životě u novorozenců malých vzhledem ke gestačnímu věku nebo předčasně narozených jsou zároveň rizikovými faktory pro nízký počet a objem nefronů a pro progresi onemocnění ledvin [5].
Nefrogeneze je ukončena v 34.–36. týdnu těhotenství. Oproti buněčné proliferaci většiny orgánů se vytváří 60 % nefronů v průběhu 3. trimestru těhotenství a jejich tvorba se ukončuje v 36. týdnu těhotenství. V postnatálním období dochází k funkčnímu zrání, zapojení renin-angiotensinového systému a zvětšení velikosti glomerulů a délky tubulů. K funkční maturaci tubulární reabsorbce sodíku a vody dochází v 18. měsíci. V období 25 měsíců pre-, peri-a postnatálně jsou ledviny senzitivní k epigenetickému programování. Prvotně epigenetické změny vedou ke strukturální modifikaci tkání, která má trvalý vliv na funkci orgánů [6].
Prenatální faktory
Koncept vývojového programování chronických nemocí předpokládá, že podněty v intrauterinních a časných postnatálních podmínkách trvale mění strukturu a funkci orgánových systémů a způsobují predispozici k rozvoji onemocnění v pozdějším životě [7]. V roce 1989 Barker formuloval inverzní vztah mezi nízkou porodní hmotností a zvýšenou mírou úmrtnosti na ischemickou chorobu srdeční. Následně se potvrdilo zvýšené riziko pro rozvoj hypertenze, diabetes mellitus 2. typu a kardiovaskulárního a chronického onemocnění ledvin [8]. Ve washingtonské analýze byl dokumentován výskyt 1,267 ‰ chronického selhání ledvin s 2,88× vyšším rizikem pro novorozence s nízkou porodní hmotností, 1,54× pro matky s gestačním diabetem, 1,26× pro mateřskou obezitu a 1,24× vyšší pro matky s nadváhou oproti novorozencům s normální porodní hmotností [9]. Nízká porodní hmotnost s gestačním diabetem byla spojena se zvýšeným rizikem obstrukční uropatie a renální dysplazie nebo aplazie.
Porodní hmotnost
Novorozenci s nízkou porodní hmotností jsou jedním z nejvíce prostudovaných suboptimálních prenatálních vlivů, které jsou citlivé na programování počtu nefronů, tubulární resorpce sodíku a aferentního sympatického nervového zásobení [10]. Před čtvrtstoletím Brenner představil, že vrozené snížení počtu nefronů by mohlo vysvětlovat, proč jsou někteří jedinci náchylnější k hypertenzi a renálnímu selhání. Nízký počet nefronů způsobuje pokles filtrační plochy a vede k následné retenci soli, zvýšení krevního tlaku a snižuje renální adaptivní kapacitu ledvin [11]. Tato teorie objasňuje propojení mezi zvýšeným výskytem hypertenze a vysokou frekvencí onemocnění ledvin u nízké porodní hmotnosti. Jednotka směrodatné odchylky snížení porodní hmotnosti proti normě zvyšuje průměrně systolický tlak o 1,3 mm Hg a jednotka směrodatné odchylky zvýšení tělesné hmotnosti v raném dětství zvyšuje systolický tlak o 1,6 mm Hg [12]. Nízký energetický příjem matky, deficit vitaminu A, železa, ligace děložní tepny, gestační diabetes a glukokortikoidy vedou k intrauterinní růstové retardaci s poklesem počtu nefronů o 20–50 % [13]. Vztah mezi porodní hmotností a počtem nefronů není ale vždy lineární a nelze odhadovat jejich počet pouze na základě porodní hmotnosti [14].
Vysoká porodní hmotnost, expozice mateřskému diabetu a urychlené postnatální přibývání na hmotnosti jsou rizikové faktory pro vznik dětské obezity, které mohou být v pozdějším věku spojeny s proteinurií a onemocněním ledvin [11]. Populační studie prokázaly vztah ve tvaru U mezi porodní hmotností a rizikem chronického onemocnění ledvin. Vysoká porodní hmotnost je pro renální programování a riziko konečného stadia renálního onemocnění stejně významná jako nízká [15]. Vysoká porodní hmotnost představuje riziko vzniku metabolického syndromu a konečného stadia renálního onemocnění způsobeného v průběhu života diabetickou nefropatií [16].
Postnatální faktory
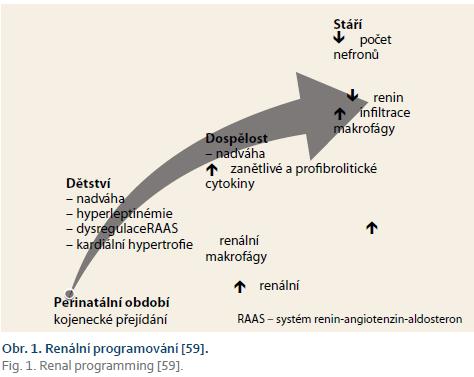
Hyperalimentace v postnatálním období má za následek časné změny genové exprese, modifikaci regulace energetické homeostázy v hypothalamu a cirkulující koncentrace hormonů, které mění metabolizmus a tkáňovou strukturu. Obezita v raném věku má okamžité a trvalé účinky na metabolizmus a funkční strukturu ledvin, slinivky břišní a srdce, které jsou shrnuty v obr. 1. Oproti tomu je omezení kalorií v postnatálním období spojeno se zpomalením patologických změn a projevů stárnutí v ledvinách a srdci [17]. Podmínky vztahující se ke vzorcům raného růstu se na buněčné úrovni spojují s mechanizmy předčasného stárnutí u oxidačního stresu, při kterém dochází ke zkrácení telomer. Významně jsou oxidačnímu stresu vystaveni novorozenci malí vzhledem ke gestačnímu věku s následným urychlením růstu. V experimentálních modelech je rychlý přírůstek postnatální hmotnosti u nízké porodní hmotnosti spojen se zkrácením telomer a zvýšenou apoptózou v ledvinách, srdci a aortě. Předčasné stárnutí ledvin může být zároveň důsledkem progredující hyperfiltrace sníženého počtu nefronů, doprovázeného rychlým nárůstem tělesného objemu [11].
Kojenecká strava s vysokým obsahem bílkovin urychluje růstový spurt a stimuluje renální hypertrofii i u zdravých donošených kojenců [18]. Vysoký příjem bílkovin indukuje zvýšenou sekreci inzulinu a IGF-1, které vedou k buněčné hyperplazii a k poklesu lipolýzy a hypertrofii tukových buněk. Objem ledviny kojenců krmených vysokým obsahem bílkovin je ve věku 6 měsíců o 10 % vyšší než u kojených s normální hmotností [19]. Renální účinek vysokého příjmu bílkovin souvisí s glomerulární hyperfiltrací na úrovni jednotlivých nefronů [14]. Výživa v raném věku se tak stává rozhodujícím faktorem pro dlouhodobé zdraví ledvin a kardiovaskulárního systému.
Poškození ledvin u dětské obezity
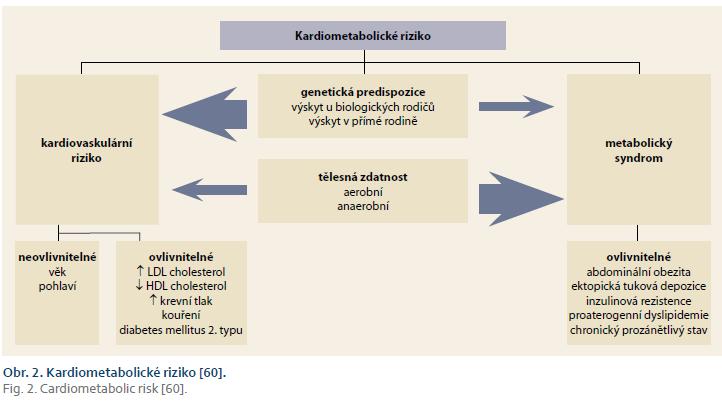
Tuková tkáň je největším endokrinním orgánem v těle a při jejím nadměrném zmnožení dochází k pozvolným, ale rozsáhlým a trvalým metabolickým změnám. Z pohledu chronických metabolických následků je nejaktivnější ektopická viscerální tuková tkáň, která se nejvýznamněji podílí na rozvoji relativního hyperkortikalizmu, hyperestrogenizmu, inzulinové rezistence a hyperkoagulace. Tento chronický stav je v řádu desetiletí potencován prolongovaným selháním ß-buněk pankreatu, proaterogenním a proimunosupresivním stavem. Komplexní metabolické změny jsou postupem času nevratné a jsou základním kamenem rozvoje metabolického syndromu. Metabolický syndrom je charakterizován absolutní inzulinovou rezistencí, endoteliální dysfunkcí a dyslipidemií. Inzulinová rezistence vede k rozvoji časného diabetes mellitus 2. typu, který urychluje aterosklerózu. Dyslipidemie, vedle podpory aterogeneze, vede k chronickému steatotickému zánětu jater. Obezita je stěžejním podkladem metabolického syndromu, který potencuje kardiovaskulární riziko v kardiometabolické riziko, jehož vztahy jsou shrnuty v obr. 2. V EU je přes 20 tisíc obézních dětí, které mají diabetes mellitus 2. typu, 400 tisíc dětí s inzulinovou rezistencí, přes 1 milion obézních dětí má známky kardiovaskulárního onemocnění vč. hypertenze a hypercholesterolemie a má tři nebo více známek metabolického syndromu. Více než 1,4 milionu má rané stadium jaterního poškození a předpokládá se u nich i rozvoj nefropatií [20].
Většina studií, které sledovaly vztah mezi obezitou a onemocněním ledvin, byla provedena u dospělých a v dětské populaci pouze v omezené formě. Přesto se přichází na stále více vztahů, které prokazují, že dětská obezita zvyšuje riziko onemocnění ledvin a že porucha funkce ledvin může začít dlouho před výskytem hypertenze nebo diabetu. Mnohé kardiovaskulární a renální následky běžné obezity, přestože se rozvíjejí v dospělosti, mají svůj původ v dětské nadváze [21].
Obézní děti mají větší ledviny s odpovídajícím zvýšením průtoku krve [22]. Obezita je spojena s glomerulární hyperfiltrací a v důsledku dilatace aferentních arteriol s hyperperfuzí, které na počátku maskují patologický pokles funkce ledvin. Patofyziologické mechanizmy u obezity vedou k sekundární formě fokální segmentální glomerulosklerózy [23].
Tuková tkáň jako největší endokrinní orgán vylučuje mnoho faktorů, souhrnně nazývané adipokininy, které mají významné prozánětlivé účinky. Adipocyty jsou stěžejními producenty leptinu a adiponektinu.
Leptin je primárním markerem tukových zásob centrální regulace energetické homeostázy. Kaskádové mechanizmy leptinu přímo i nepřímo ovlivňují ledviny. U obezity dochází k selektivní neurorezistenci leptinu v orexigenních centrech hypotalamu, ale jeho renální aktivita je plně zachována. Hyperleptinemie vede ke zvýšení uvolňování reninu a následnému rozvoji hypertenze. Leptin v glomerulárních endoteliálních buňkách stimuluje buněčnou proliferaci a produkci kolagenu IV. typu, které vedou k renální fibróze. U dětských obézních pacientů s chronickým onemocněním ledvin byly dokumentovány nadprůměrné hodnoty leptinu u 80 % a supranormální u 45 % případů [24].
Komplementárním hormonem leptinu je adiponektin, který se primárně zapojuje do regulace metabolizmu glukózy, zvyšuje inzulinovou senzitivitu, oxidaci mastných kyselin a má protizánětlivé účinky. Hladina adiponektinu inverzně koreluje s albuminurií. Deficit adiponektinu přispívá k poškození glomerulární permeability a dysfunkci podocytů. Nízká hladina adiponektinu je nezávislým prediktorem kardiovaskulárního rizika jak u dospělé, tak dětské obezity [25]. Úloha adiponektinu však stále není u renální a kardiální protekce objasněna a u dětí spíše s rozporuplnými nálezy [26].
Inzulinová rezistence
Jedním z nejvýznamnějších následků obezity je inzulinová rezistence. Obézní děti se shodným BMI mohou mít odlišné riziko komplikací na podkladě míry inzulinorezistence [27]. Následky obezity v cílových orgánech vč. ledvin jsou v dospělosti pravděpodobnější u těch, kterým se v dětství inzulinorezistence rozvinula [28]. Inzulin je prozánětlivý hormon a inzulinová rezistence potencuje chronický zánět a naopak. Hyperinzulinemie ovlivňuje krevní tlak a koncentraci lipoproteinů s následkem hypertenze a dyslipidemie. Přítomnost těchto faktorů sehrává klíčovou roli v patogenezi sekundární formy fokální segmentální glomerulosklerózy, která se pojí s obezitou [29].
Spouštěčem albuminurie a mikro-albuminurie není samotná obezita, ale její metabolické následky. Mikroalbuminurie je běžným nálezem u morbidně obézních dětí [30]. Je známkou glomerulární a tubulární dysfunkce. Hnací silou mikroalbuminurie je inzulinová rezistence a mírné abnormality v metabolizmu glukózy. Poměr vylučování albuminu ku kreatininu souvisí primárně s hyperinzulinemií a inzulinorezistencí [31]. Mikroalbuminurie je spojena s extrémní obezitou a urychlením růstu tělesné hmotnosti, kterému se ledviny nestíhají přizpůsobit [32].
Diabetes
Selhání ledvin způsobené diabetem je v dětství neobvyklé, ale expozice hyperglykemiím přispívají k dlouhodobým komplikacím již od dětství [33]. V dětství doposud převažuje výskyt diabetes mellitus 1. typu, ale zahraniční dětská centra informují o rapidním nárůstu případů diabetes mellitus 2. typu, který tvoří v USA jednu třetinu nově diagnostikovaných případů cukrovky ve věku 10–19 let [34]. Zhoršená tolerance glukózy a inzulinová rezistence jsou mezistupně v jeho vývoji. Morbidní obezita je nejvýznamnějším rizikovým faktorem pro rozvoj diabetes mellitus 2. typu již v mládí a zvyšující se výskyt nadváhy úzce souvisí s jeho nárůstem u dětí a dospívajících [35].
Standardem monitoringu dětských diabetiků je screening glomerulární filtrace a albuminurie. Pozitivní nález vyžaduje nefrologické vyhodnocení [36]. Diagnózu onemocnění ledvin u dětí s diabetem nelze spolehlivě určit klinickým a laboratorním nálezem a pro upřesnění je nezbytná renální biopsie k vyloučení imunonefropatie nebo glomerulosklerózy, které jsou pro ně typičtější [37].
Hypertenze
Hodnoty krevního tlaku se u dětí v posledním desetiletí zvýšily souběžně s růstem obezity. Prevalence hypertenze se u školních dětí progresivně zvyšuje s percentilem směrodatné odchylky BMI [38]. Riziko hypertenze se zvyšuje v celém rozsahu, ale není definováno jednoduchým prahovým efektem. Obézní dítě ve věku 15–19 let má 2,5–3,7× větší pravděpodobnost rozvoje hypertenze se zvýšením systolického tlaku o 0,8 mm Hg na nárůst jednotky BMI u chlapců a o 1,2 mm Hg u dívek [39,40]. Ve Framingham Off-spring Study bylo pozorováno riziko hypertenze v souvislosti s nadváhou u 78 % chlapců a 65 % dívek [41].
Prevalence vysokého normálního krevního tlaku se zvyšuje po celé dětství a u dospívajících v důsledku přibývání na hmotnosti [42]. Na rozvoji vysokého krevního tlaku se v dětství podílí inzulinová rezistence [27], která ovlivňuje renální reabsorpci sodíku a hyperaktivitu sympatického nervového systému, vč. zvýšení hladiny katecholaminů, zvýšení srdeční frekvence a variability krevního tlaku [39].
Vysoký normální krevní tlak má u obézní dětské populace stejný klinický význam jako hypertenze u běžné populace a je považovaná za rovnocenný rizikový faktor, protože i mírné zvýšení krevního tlaku vystavuje pacienta zvýšenému riziku [42]. Ledvina je příčinou i obětí hypertenze. V přítomnosti inzulinorezistence a dyslipidemie ve spojení s vyšším krevním tlakem může přispívat k poškození ledvin s postupnou ztrátou nefronů [43], které zpětně podmiňuje zvýšení krevního tlaku [44].
Dyslipidemie
Dyslipidemie přispívá k progresi aterosklerózy a onemocnění ledvin. Morbidně obézní děti mají nepříznivý profil lipidů a lipoproteinů s vyšším kardiovaskulárním rizikem [45]. Významně vyšší hladinu LDL cholesterolu a triglyceridů a nižší koncentrace HDL cholesterolu mají zejména v období puberty [46]. Polovina obézních dětí ve věku 8–12 let má zvýšené koncentrace celkového cholesterolu v porovnání s pětinou neobézních [47]. V Bogalusa Heart Study korelovaly hodnoty celkového cholesterolu u mladých dospělých s hodnotami před jejich 20. rokem [48]. Přibližně u poloviny dětí a dospívajících, kteří měli koncentraci celkového cholesterolu a LDL cholesterolu v krvi > 75 percentil, se přenesla dyslipidemie do dospělosti. Objevují se údaje o účinnosti léčby hyperlipidemie u dětských pacientů, ale zatím nejsou k dispozici žádné údaje o vlivu léčby statiny na rozvoj vaskulopatie nebo zlepšení přežití u dětí s chronickým onemocněním ledvin.
Klíčovou úlohu v dyslipidemii sehrává enterohepatální metabolizmus a nealkoholická jaterní steatóza, která je v pediatrii v rozvinutých zemích nejrozšířenější příčinou onemocnění jater a doprovází epidemii dětské obezity. NAFLD je spojena se sníženou glomerulární filtrací a mikroalbuminurií nezávisle na antropometrických a klinických proměnných [49]. U morbidně obézních adolescentů se vyskytuje v 80 % případů [50]. Klinický obraz NAFLD bývá němý, bez výraznějších subjektivních obtíží. Při vyšetření se setkáváme s elevací alaninaminotransferázy, dyslipidemií a inzulinovou rezistencí doprovázených echografickým obrazem jaterní steatózy. Klinické jednotky hepatopatie lze v současné době ověřovat pouze jaterní biopsií, k jejíž indikaci nejčastěji vedou chronicky zvýšené aminotransferázy s dominancí gama-glutamyltransferázy a pozitivní protilátky proti hladké svalovině.
Mikrobion
V těsné koexistenci s jaterní tkání kooperuje mikrobiální střevní flóra, která má rovnocenný metabolický význam, ale oproti jaternímu metabolizmu s pasivní aktivitou. Mikrobiota se významně účastní metabolických pochodů na úrovni energetické homeostázy, toxikologie a hormonální modifikace trávicího traktu. Zdrojem mikrobioty novorozence je během průchodu porodním kanálem jeho matka. Následně se modifikuje jen mírně dle vnějších podmínek. Na unikátní lidské mikrobiotě se na jednotlivých úrovních v odlišných ekologických společenstvech podílejí specifické mikroorganizmy.
Stejně negativně jak soudobá civilizace zasahuje do makroekosystémů, tak významně negativně zasahuje i do mikroekosystémů trávicího traktu. Obezita je spojena v distální části střeva s redukcí gramnegativních Bacteroides a proporcionálním navýšením grampozitivních Fermicutes. Omezení tuků a sacharidů ve stravě nevede jen ke snížení hmotnosti, ale i v řádu týdnů k úpravě mikrobiálních poměrů ve střevě.
Potenciál metabolické aktivity střevní mikrobioty je shodný s metabolickým potenciálem jaterní tkáně. Mikrobiota se v hostitelském organizmu účastní na úrovní příjmu a ukládání zásob energetické homeostázy. Může ovlivňovat inzulinovou rezistenci, glukózový a lipidový metabolizmus, ukládání tuků a následně tělesnou hmotnost. Při zvýšeném příjmu tuků vedou fermentační procesy mikrobioty ke zvýšené oxidaci mastných kyselin. Protektivní cholin může konvertovat na hepatotoxické mataaminové formy, které podporují jaterní steatózu. Lipoperoxidace žlučových kyselin vede k zásahu do energetického tukového metabolizmu a ukládání triglyceridů. Hyperperoxidace podporuje inzulinovou rezistenci a chronickou zánětlivou reakci indukovanou nízkou hladinovou lokální endotoxemií. Otázkou nezůstává nejen proliferativní potenciál mikrobioty na specifické buňky trávicího traktu a pseudohormonální aktivita produktů a fermentace mikrobioty na jaterní buňky, ale i celá řada zatím neprobádaných a netušených vazeb unikátního ekospolečenství, které se přímo podílí na rozvoji NAFLD, inzulinové rezistence, dyslipidemie a nepřímo i na poškození ledvin.
Kyslíkové radikály
Oxidační stres a oxid dusnatý představují významné spojení mezi obezitou, kardiovaskulárním a metabolickým onemocněním a onemocněním ledvin. Oxidační stres se zvyšuje s nadváhou prepubertálních dětí a koreluje se stupněm kardiometabolického rizika a funkcí ledvin [51]. Markerem oxidačního stresu jsou izoprostany, které sehrávají stěžejní roli při patogenezi vaskulární dysfunkce. Na ateroskleróze se podílejí vazokonstrikcí, agregací krevních destiček a zvýšením adherence neutrofilů a monocytů na endoteliální výstelku cév. Zvýšený oxidační stres u obézních dětí může být příčinou poškození arteriální stěny i v nepřítomnosti hypertenze [52]. Morbidně obézní dětí mají ztluštěnou intimu medii karotid a akcentovanou rychlost pulzové vlny [53]. Syntetáza oxidu dusnatého (NO syntetáza) je v pozitivní korelaci s kyselinou močovou a produkty peroxidační xanthinoxidázy. Jsou indukovány současně a potencují systémový prozánětlivý stav. Vysoké množství NO a peroxydusitanu vytvořené při prozánětlivých podmínkách inhibuje endoteliální NO syntetázu. Hypercholesterolemie, inzulinová rezistence, diabetes, arteriální hypertenze, oxidační stres a hyperleptinemie způsobují u obezity pokles syntézy NO v ledvinách a přispívají k vazokonstrikčnímu poškození ledvin [54].
Závěr
Dětská nadváha přestupuje v 80 % do dospělosti. Tito jedinci se budou řadit k chronicky obézním dospělým se závažnými zdravotními následky, které se rozvinou již v produktivním věku. Na podkladě časného diabetes mellitus 2. typu se předpokládá manifestace nefropatií, retinopatií a angiopatií dolních končetin, na podkladě steatohepatitidy rozvoj cirhózy, na základě prozánětlivého stavu posun nádorových onemocnění, iktů a infarktů myokardu do raného produktivního věku. Na jedné straně dojde ke snížením ekonomického a společenského uplatnění chronicky obézních a na druhé ke zvyšování zdravotnických a celospolečenských nákladů.
Patofyziologické mechanizmy spojené s obezitou, které vedou k rozvoji nefropatií od dětského věku, se při epigenetickém programování týkají pětiny a u dětské obezity desetiny dětské populace. Naplnění katastrofické vize následků dětské nadváhy jsou velkou výzvou, protože záleží bez nadsázky na všech, jestli se podaří zvrátit současné negativní trendy. Snaha převedení morbidní obezity do metabolicky neaktivní formy je nákladná, zdlouhavá a s nejistými dlouhodobými výsledky. Normalizovat hmotnost při rozvoji morbidní obezity, kdy dochází k přeprogramování centrální energetické homeostázy, není současnými prostředky možná. Obezita se tak stává celoživotní a nevyléčitelnou chronickou nemocí. Jedinou účelnou léčbou dětské obezity je a bude pouze její prevence. Každý jedinec by měl dostat šanci uplatnit se ve zdravém životním stylu, který je nutné budovat od nejútlejšího věku, a ne získat pocit selhání v současném vysoce toxickém obezitogenním prostředí.
Přijato/Accepted: 5. 12. 2019
MUDr. Zlatko Marinov
Dětská obezitologická ambulance
FN Motol
V Úvalu 84
150 06 Praha
zlatko.marinov@fnmotol.cz

Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Procházka B, Kratěnová J, Žejglicová K et al. Aktuální výskyt rizikových faktorů ischemické choroby srdeční u dětí v ČR v roce 2016. Čes-slov Pediat 2018; 73 (8): 501–508.
2. Iqbal U, Perumpail BJ, Akhtar D et al. The epidemiology, risk profiling and diagnostic challenges of nonalcoholic fatty liver disease. Medicines (Basel) 2019; 6 (1): E41. doi: 10.3390/medicines6010041.
3. de Jong PE, Verhave JC, Pinto-Sietsma SJ et al. Obesity and target organ damage: the kidney. Int J Obes Relat Metab Disord 2002; 26: S21–S24. doi: 10.1038/sj.ijo.0802213
4. Marinov Z, Střítecká H, Riedlová J at al. Programování energetické homeostázy. DMEV 2015; 18 (2): 69–74.
5. Abitbol CL, Chandar J, Rodriguez MM et al. Obesity and preterm birth: additive risks in the progression of kidney disease in children. Pediatr Nephrol 2009; 24 (7): 1363–1370. doi: 10.1007/s00467-009-1120-2.
6. O’Sullivan L, Combes AN, Moritz KM. Epigenetics and developmental programming of adult onset diseases. Pediatr Nephrol 2012; 27 (12): 2175–2182. doi: 10.1007/s00467-012-2108-x.
7. Leontovyčová J, Janda J. Nízká porodní hmotnost a další rizikové faktory pro pozdější onemocnění u dětí a dospělých (prenatální a postnatální programming). Čes-slov Pediat 2018; 73 (3): 166–172.
8. Hanson M, Gluckman P. Developmental origins of noncommunicable disease: population and public health implications. Am J Clin Nutr 2011; 94 (Suppl 6): S1754–S1758. doi: 10.3945/ajcn.110.001206.
9. Plagemann A, Harder T, Rake A et al. Perinatal elevation of hypothalamic insulin, acquired malformation of hypothalamic galaninergic neurons, and syndrome x-like alterations in adulthood of neonatally overfed rats. Brain Res 1999; 836 (1–2): 146–155. doi: 10.1016/s0006-8993 (99) 01662-5.
10. Kett MM, Denton KM. Renal programming: cause for concern? Am J Physiol Regul Integr Comp Physiol 2011; 300 (4): 791–803. doi: 10.1152/ajpregu.00791.2010.
11. Luyckx VA, Bertram JF, Brenner BM et al. Effect of fetal and child health on kidney development and long-term risk of hypertension and kidney disease. Lancet 2013; 382 (9888): 273–283. doi: 10.1016/S0140-6736 (13) 60311-6.
12. Andersen LG, Angquist L, Eriksson JG et al. Birth weight, childhood body mass index and risk of coronary heart disease in adults: combined historical cohort studies. PLoS One 2010; 5 (11): e14126. doi: 10.1371/journal.pone.0014126.
13. Lelièvre-Pégorier M, Merlet-Bénichou C. The number of nephrons in the mammalian kidney: environmental influences play a determining role. Exp Nephrol 2000; 8 (2): 63–65. doi: 10.1159/000020649.
14. Boubred F, Saint-Faust M, Buffat C et al. Developmental origins of chronic renal disease: an integrative hypothesis. Int J Nephrol 2013: 346067. doi: 10.1155/2013/346067.
15. Vikse BE, Irgens LM, Leivestad T et al. Low birth weight increases risk for end-stage renal disease. J Am Soc Nephrol 2008; 19 (1): 151–157. doi: 10.1681/ASN.2007020252.
16. Stene LC, Magnus P, Lie RT et al. Birth weight and childhood onset type 1 diabetes: population based cohort study. BMJ 2001; 322 (7291): 889–892. doi: 10.1136/bmj.322.7291.889.
17. Krishnamurthy J, Torrice C, Ramsey MR et al. Ink4a/Arf expression is a biomarker of aging. J Clin Invest 2004; 114 (9): 1299–1307. doi: 10.1172/JCI22475.
18. Agostoni C, Turck D. Is cow’s milk harmful to a child’s health? J Pediatr Gastroenterol Nur 2011; 53 (6): 594–600. doi: 10.1097/MPG.0b013e318235b23e.
19. Escribano J, Luque V, Ferre N et al. Increased protein intake augments kidney volume and function in healthy infants. Kidney Int 2011; 79 (7): 783–790. doi: 10.1038/ki.2010.499.
20. Lobstein T, Jackson-Leach R. Estimated burden of paediatric obesity and co-morbidities in Europe. Part 2. Numbers of children with indicators of obesity-related disease. Int J Pediatr Obes 2006; 1 (1): 33–41. doi: 10.1080/17477160600586689.
21. Srivastava T. Nondiabetic consequences of obesity on kidney. Pediatr Nephrol 2006; 21 (4): 463–470. doi: 10.1007/s00467-006-0027-4.
22. Pantoja-Zuzuárregui JR, Mallios R, Murphy J. The effect of obesity on kidney length in a healthy pediatric population. Pediatr Nephrol 2009; 24 (10): 2023–2027. doi: 10.1007/s00467-009-1202-1.
23. Gunta SS, Mak RH. Is obesity a risk factor for chronic kidney disease in children? Pediatr Nephrol 2013; 28 (10): 1949–1956. doi: 10.1007/s00467-012-2353-z.
24. Daschner M, Tönshoff B, Blum WF et al. Inappropriate elevation of serum leptin levels in children with chronic renal failure. European Study Group for Nutritional Treatment of Chronic Renal Failure in Childhood. J Am Soc Nephrol 1998; 9 (6): 1074–1079.
25. Mitsnefes M, Kartal J, Khoury P et al. Adiponectin in children with chronic kidney disease: role of adiposity and kidney dysfunction. Clin J Am Soc Nephrol 2007; 2 (1): 46–50. doi: 10.2215/CJN.02790806.
26. Yoshinaga M, Sameshima K, Tanaka Y et al. Adipokines and the prediction of the accumulation of cardiovascular risk factors or the presence of metabolic syndrome in elementary school children. Circ J 2008; 72 (11): 1874–1878. doi: 10.1253/circj.cj-08-0180.
27. Chiarelli F, Marcovecchio ML. Insulin resistance and obesity in childhood. Eur J Endocrinol 2008; 159 (Suppl 1): S67–S74. doi: 10.1530/EJE-08-0245.
28. Jolliffe CJ, Janssen I. Vascular risks and management of obesity in children and adolescents. Vasc Health Risk Manag 2006; 2 (2): 171–187. doi: 10.2147/vhrm.2006.2.2.171.
29. Teplan V, Lukáš M, Beňo P et al. Obezita a ledviny. Gastroent Hepatol 2017; 71 (6): 510–516. doi: 10.14735/amgh2017510.
30. Burgert TS, Dziura J, Yeckel C et al. Micro-albuminuria in pediatric obesity: prevalence and relation to other cardiovascular risk factors. Int J Obes (Lond) 2006; 30 (2): 273–280. doi: 10.1038/sj.ijo.0803136.
31. Verhulst SL, Van Hoeck K, Schrauwen N et al. Sleep-disordered breathing and proteinuria in overweight and obese children and adolescents. Horm Res 2008; 70 (4): 224–229. doi: 10.1159/000151594.
32. Ferris M, Hogan SL, Chin H et al. Obesity, albuminuria, and urinalysis findings in US young adults from the Add Health Wave III Study. Clin J Am Soc Nephrol 2007; 2 (6): 1207–1214. doi: 10.2215/CJN.00540107.
33. Lane PH. Pediatric aspects of diabetic kidney disease. Adv Chronic Kidney Dis 2005; 12 (2): 230–235. doi: 10.1053/j.ackd.2005.01.005.
34. Pinhas-Hamiel O, Dolan LM, Daniels SR et al. Increased incidence of non-insulin-dependent diabetes mellitus among adolescents. J Pediatr 1996; 128 (5): 608–615. 10.1016/s0022-3476 (96) 80124-7.
35. Hannon TS, Rao G, Arslanian SA. Childhood obesity and type 2 diabetes mellitus. Pediatrics 2005; 116 (2): 473–480. 10.1542/peds.2004-2536.
36. Edelstein SL, Knowler WC, Bain RP et al. Predictors of progression from impaired glucose tolerance to NIDDM: an analysis of six prospective studies. Diabetes 1997; 46 (4): 701–710. doi: 10.2337/diab.46.4.701.
37. Sellers EA, Blydt-Hansen TD, Dean HJ et al. Macroalbuminuria and renal pathology in First Nation youth with type 2 diabetes. Diabetes Care 2009; 32 (5): 786–790. doi: 10.2337/dc08-1828.
38. Muntner P, He J, Cutler JA et al. Trends in blood pressure among children and adolescents. JAMA 2004; 291 (17): 2107–2113. doi: 10.1001/jama.291.17.2107.
39. Sorof J, Daniels S. Obesity hypertension in children: a problem of epidemic proportions. Hypertension 2002; 40 (4): 441–447. doi: 10.1161/01.hyp.0000032940.33466.12.
40. Lee WW. An overview of pediatric obesity. Pediatr Diabetes 2007; 8 (Suppl 9): S76–S87. doi: 10.1111/j.1399-5448.2007.00337.x.
41. Garrison RJ, Kannel WB, Stokes J 3rd et al. Incidence and precursors of hypertension in young adults: the Framingham Offspring Study. Prev Med 1987; 16 (2): 235–251. doi: 10.1016/0091-7435 (87) 90087-9.
42. Falkner B, DeLoach S. Refining the blood pressure phenotype in children: when does target organ damage begin? Hypertension 2009; 53 (6): 905–906. doi: 10.1161/HYPERTENSION AHA.109.130070.
43. Bakris GL, Ritz E. The message for World Kidney Day 2009: hypertension and kidney disease – a marriage that should be prevented. Pediatr Nephrol 2009; 24 (3): 427–430. doi: 10.1007/s00467-008-1112-7.
44. El-Atat FA, Stas SN, McFarlane SI et al. The relationship between hyperinsulinemia, hypertension and progressive renal disease. J Am Soc Nephrol 2004; 15 (11): 2816–2827. doi: 10.1097/01.ASN.0000133698.80390.37.
45. Glowinska B, Urban M, Koput A et al. New atherosclerosis risk factors in obese, hypertensive and diabetic children and adolescents. Atherosclerosis 2003; 167 (2): 275–286. doi: 10.1016/s0021-9150 (03) 00003-0.
46. Nicklas TA, von Duvillard SP, Berenson GS. Tracking of serum lipids and lipoproteins from childhood to dyslipidemia in adults: the Bogalusa Heart Study. Int J Sports Med 2002; 23 (Suppl 1): S39–S43. doi: 10.1055/s-2002-28460.
47. Friedland O, Nemet D, Gorodnitsky N et al. Obesity and lipid profiles in children and adolescents. J Pediatr Endocrinol Metab 2002; 15 (7): 1011–1016. doi: 10.1515/jpem.2002.15.7. 1011.
48. Webber LS, Harsha DW, Phillips GT et al. Cardiovascular risk factors in Hispanic, white, and black children: the Brooks County and Bogalusa Heart studies. Am J Epidemiol 1991; 133 (7): 704–714. doi: 10.1093/oxfordjournals.aje.a115945.
49. Pacifico L, Bonci E, Andreoli GM et al. The impact of nonalcoholic fatty liver disease on renal function in children with overweight/obesity. Int J Mol Sci 2016; 17 (8). doi: 10.3390/ijms17081218.
50. Feldstein AE, Patton-Ku D, Boutelle KN. Obesity, nutrition, and liver disease in children. Clin Liver Dis 2014; 18 (1): 219–231. doi: 10.1016/j.cld.2013.09.003.
51. Correia-Costa L, Sousa T, Morato M at al. Oxidative stress and nitric oxide are increased in obese children and correlate with cardiometabolic risk and renal function. Br J Nutr 2016; 116: 805–815. doi: 10.1017/S0007114516002804.
52. Meyer AA, Kundt G, Steiner M et al. Impaired flow-mediated vasodilation, carotid artery intima-media thickening, and elevated endothelial plasma markers in obese children: the impact of cardiovascular risk factors. Pediatrics 2006; 117 (5): 1560–1567. doi: 10.1542/peds.2005-2140.
53. Giannini C, de Giorgis T, Scarinci A et al. Obese related effects of inflammatory markers and insulin resistance on increased carotid intima media thickness in pre-pubertal children. Atherosclerosis 2008; 197 (1): 448–456. doi: 10.1016/j.atherosclerosis.2007.06. 023.
54. Pacher P, Beckman JS, Liaudet L. Nitric oxide and peroxynitrite in health and disease. Physiol Rev 2007; 87 (1): 315–424. doi: 10.1152/physrev.00029.2006.
55. Marinov Z. Nadváha a běžná obezita v dětském věku – zdravotní výzva 21. století. Lékařské listy 2014; 9: 21–24.
56. Ong KK, Ahmed ML, Emmett PM et al. Association between postnatal catch-up growth and obesity in childhood: prospective cohort study. BMJ 2000; 320 (7240): 967–971. doi: 10.1136/bmj.320.7240.967.
57. Druet C, Stettler N, Sharp S et al. Prediction of childhood obesity by infancy weight gain: an individual-level meta-analysis. Paediatr Perinat Epidemiol 2012; 26 (1): 19–26. doi: 10.1111/j.1365-3016.2011.01213.x.
58. Weng SF, Redsell SA, Swift JA et al. Systematic review and meta-analyses of risk factors for childhood overweight identifiable during infancy. Arch Dis Child 2012; 97 (12): 1019–1026. doi: 10.1136/archdischild-2012-302263.
59. Yim HE, Yoo KH. Early life obesity and chronic kidney disease in later life. Pediatr Nephrol 2015; 30 (8): 1255–1263. doi: 10.1007/s00467-014-2922-4.
60. Marinov Z, Pastucha D. Komplexní metabolické změny u obézních dětí. Pediatr praxi 2012: 13 (1): 12–15.