Duodenálne stenty, nechirurgické riešenie poruchy evakuácie žalúdka pri malígnych ochoreniach
Ján Ušák Orcid.org 1, Filip Závada Orcid.org 2, Rastislav Husťak3,4,5, Andrej Klepanec6, Igor Keher7, Silvia Hojerová8, Marián Streško9, Vanda Ušáková10, Jan Martínek Orcid.org 11,12
+ Pracoviště
Souhrn
Úvod: Zavedenie samoexpandibilného metalického stentu do duodena je paliatívny výkon určený pre pacientov s malígnymi stenózami v mieste pylorického kanála alebo duodena, u ktorých je prítomná obštrukcia s evakuačnou poruchou žalúdka a nie sú vhodní na operačné riešenie. Východisko: Karcinóm pankreasu a žalúdka sú ochorenia často diagnostikované v pokročilom štádiu, keď býva iniciálne potrebné vytvoriť podmienky pre najlepšiu podpornú liečbu. Ciele: Retrospektívne sme sledovali celkové prežívanie pacientov, ktorým bol zavedený duodenálny stent na našom pracovisku v období rokov 2013–2017 pre evakuačnú poruchu žalúdka, z dôvodu malígnej infiltrácie výtokovej časti žalúdka alebo duodena. Umožnilo sa tak obnovenie príjmu potravy a prepustenie pacientov z nemocničnej starostlivosti. Priemerný vek pacientov bol 69,5 roka. Bolo implatnovaných 26 stentov 20 pacientom, prevažne sa jednalo o pacientov s karcinómom pankreasu a žalúdka s evakuačnou poruchou žalúdka s nízkym výkonnostným stavom, ktorých nebolo možné operovať. Priemerná dĺžka prežívania po zavedení stentu bola 114,6 dňa a 65 % pacientov bolo možné prepustiť z nemocničnej starostlivosti. Záver: Správna indikácia a postup pri zavedení samoexpandibilného metalického stentu do duodena môžu efektívne riešiť evakuačnú poruchu žalúdka, zlepšujú kvalitu života, často limitovanú medicínsky neriešiteľným malígnym nádorovým ochorením.
Klíčová slova
duodenální stent, evakuační porucha žaludku, podpůrná léčba, samoexpandibilní metalický stentÚvod
Evakuačná porucha žalúdka (GOO – gastric outlet obstruction) predstavuje závažný medicínsky problém, ktorý vyžaduje riešenie na zabezpečenie vitálnych potrieb organizmu. V našich podmienkach je najčastejšou príčinou obštrukcie s následnou GOO lokálne pokročilý karcinóm pankreasu, v ázijských krajinách je to karcinóm žalúdka [1].
Klinicky sa u pacientov najčastejšie vyskytuje pokles hmotnosti (často závažný), ikterus (pri nádoroch pankreasu), zvracanie a intolerancia potravy, zápach úst z natrávenej potravy. Bolesti môžu a nemusia byť prítomné.
Možnosti riešenia sú chirurgické (derivačné operácie), endoskopické alebo rádiologické (zavedenie samoexpandibilného metalického stentu – SEMS). Hlavnou indikáciou na zavedenie duodenálneho stentu je obštrukcia odchodu potravy zo žalúdka z malígnej príčiny. Cieľom je obnovenie duodenálneho lúmenu u symptomatických pacientov, u ktorých je pomerne krátke očakávanie prežívania (2–6 mesiacov) [2]. Zo zavedenia stentu najviac profitujú pacienti s nižším výkonnostným stavom (podľa Eastern Coopertive Oncology Group – ECOG) [3,4].
Naopak, zavedenie stentu nie je indikované u pacientov bez GOO. U pacientov v dobrom výkonnostnom stave (ECOG 0–2) sa preferuje chirurgické riešenie, nakoľko má z dlhodobého hľadiska lepšie výsledky (tab. 1).
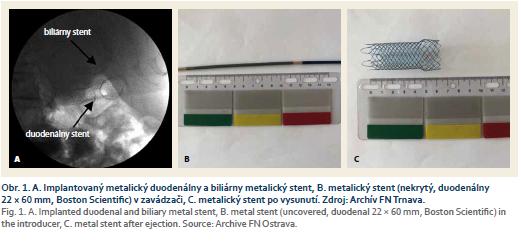
Dostupné sú duodenálne SEMS kryté (covered), nekryté (uncovered), v skúšaní sú čiastočne kryté (partially co-vered). Vo všeobecnosti sa akceptuje, že kryté stenty majú lepšie vlastnosti vo vzťahu k prerastaniu malígnym ochorením, ale častejšie migrujú a sú menej flexibilné. Preto niektoré pracoviská používajú pri malígnej príčine poruchy evakuácie žalúdka nekryté stenty, u ktorých sa predpokladá výhoda, že ostávajú voľné žlčové cesty, či už bez, alebo so zavedeným biliárnym stentom (obr. 1A). Ukazuje sa však, že výsledky použitia krytých a nekrytých stentov sú podobné a rozdiely medzi nimi nie sú štatisticky významné [5]. Na našom pracovisku sa používajú Wallflex duodenálne stenty priemeru 22 mm, dĺžky 60–90–120 mm, kryté alebo nekryté (Boston Scientific). K výkonu slúžia rôzne endoskopy, podľa miesta obštrukcie a od vzdialenosti stenózy (obštrukcie) od rezákov. Ak je prekážka transpyloricky, používa sa terapeutický gastroskop, v oblasti D2 duodena duodenoskop a v oblasti distálneho duodena kolonoskop (s výhodou detský, ak je dostupný). Výber endoskopu záleží od lokálnych zvyklostí a možností. Na našom pracovisku stenty zavádzame v intravenóznej sedácii propofolom.
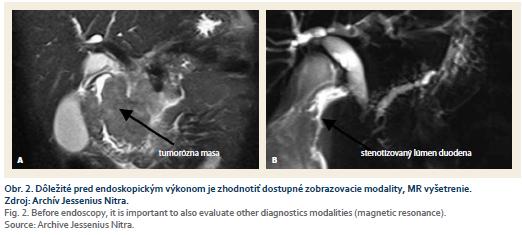
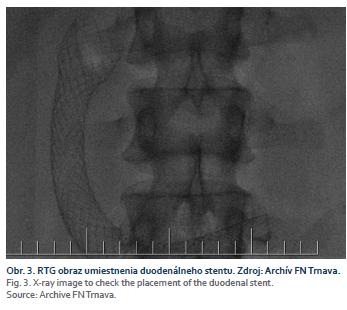
Pokiaľ je možné, je dobré oboznámiť sa s anatomickými pomermi CT vyšetrením alebo magnetickou rezonanciou, i keď to nie je podmienkou (obr. 2 a 3). Pred výkonom je potrebné odsať žalúdkový obsah. Po zavedení duodenoskopu je dobré fixovať jeho polohu ak sa dá tak, že endoskop sa oprie slučkou o steny žalúdka a vytvorí „loop”. Kanylou sa tvrdý vodič (napr. Amplatz Super Stiff™ Guidewire) zavedie tak, aby sa distálnym koncom bezpečne dostal až za pozíciu Treitzovho ligamenta s dostatočnou rezervou pre vyvolanie pnutia pri zavádzaní stentu. V prípade tesnej stenózy je potrebné, aby vodič bol hydrofilný. Pozícia vodiča sa kontroluje aplikovaním kontrastu (napr. Ultravist) do stenózy, napr. kanylou.
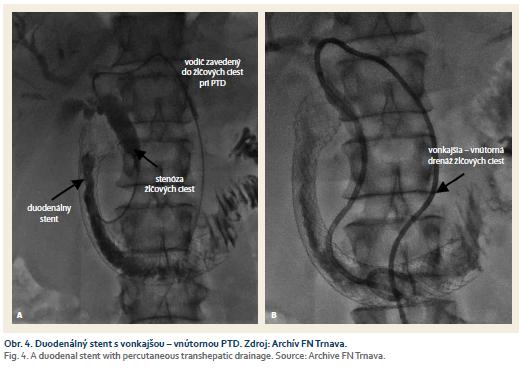
Voľba dĺžky stentu záleží na dĺžke stenózy (obr. 4A). Niekedy je potrebné použiť dva stenty na preklenutie dlhej stenózy alebo býva potrebné stentovať žlčové cesty, či už plastovými alebo výhodnejšie metalickými stentami. Prístup môže byť transpapilárny (endoskopickou retrográdnou cholangiopankreatikografiou) alebo transhepatálny (perkutánnou transhepatálnou drenážou – PTD). U karcinómu pankreasu býva často potrebné pred zavedením duodenálneho stentu zaistiť drenáž žlčových ciest, ideálne SEMS. Ak je prítomná duodenálna stenóza, môže byť už zavedenie biliárneho stentu duodenoskopom technicky nerealizovateľné a je nutné realizovať PTD (obr. 4B). Niektoré pracoviská pripúšťajú miernu balónovú preddilatáciu malígnej stenózy pred zavedením duodenálneho SEMS.
Pri odhadnutí dĺžky stentu je potrebné zohľadniť fakt, že pri „otváraní” stentu dochádza k jeho skráteniu až o 30 % (obr. 1B a 1C). Odporúča sa odhadnúť dĺžku stenózy a prirátať 4 cm. Vo všeobecnosti platí, že dlhší stent je vhodnejší [6]. Ak je to možné, snažíme sa, aby bol proximálny koniec transpyloricky (nie v bulbe duodena) a distálny nebol zalomený oproti duodenálnemu ohybu (poranenie steny duodena, resp. prekážka pri prechode potravy stentom). Samotný stent sa otvára pomaly, za neustálej kontroly polohy rentgenom, v jej proximálnej časti (pred pylorom) endoskopicky. Pri rýchlom otváraní sa môže stať, že stent nemá správnu polohu (ktorá sa mení jeho skrátením pri otváraní), alebo v záverečnej fáze „vyskočí” z púzdra a úplne stratíme správnu polohu. Na záver po jeho zavedení sa kontroluje poloha a priechodnosť aplikáciou kontrastu do stentu.
Pri potrebe zavedenia druhého stentu sa postupuje rovnako. Je potrebné, aby bol koniec prvého stentu transpyloricky (v bulbe môže spôsobiť perforáciu alebo nekrózu steny) a druhý sa zavádza do „stentu”, ak je jeho dĺžka nedostatočná alebo rozsah stenózy prekračuje možnosti stentu.
Európska spoločnosť pre gastrointestinálnu endoskopiu nemá vypracované všeobecné odporúčania na implantáciu duodenálnych SEMS. Dostupné sú odporúčania radiologickej spoločnosti Cardiovascular and Interventional Radiological Society of Europe [7]. Podľa týchto odporúčaní sú indikáciou na implantáciu duodenálneho stentu nasledovné stavy:
1. Neresekabilné alebo neliečiteľné malígne ochorenia spôsobujúce gastrointestinálnu obštrukciu:
a) Intrinsické alebo extrinsické tumory oblasti žalúdka alebo duodena. Kuratívna resekcia nie je možná u 40 % pacientov.
b) Extrinsické gastroduodenálne obštrukcie pri karcinómoch pankreasu, cholangiocelulárnych karcinómoch, malígnej lymfadenoaptii, pri lokalizovaných intraperitoneálnych metastázach alebo lymfóme. Kuratívna resekcia nie je možná u 80–95 % pankreatických karcinómoch.
2. Rekurencia nádoru v aferentnej alebo eferentnej kľučke po gastrojejunostómii po paliatívnom chirurgickom zákroku pre hornú gastrointestinálnu malignitu.
3. U pacientov s reziduálnou malignitou alebo u tých, ktorým zlyhala opakovaná dilatácia.
4. Povlečené stenty na liečbu malígnych fistúl žalúdka a duodena do priľahlých orgánov.
5. Benígne striktúry sekundárne po chronickej vredovej chorobe, keď operácia nie je možná a opakovaná balónová dilatácia zlyhala.
Za kontraindikácie sa považuje [7]:
Absolútne – 1. klinické a radiologické príznaky voľnej perforácie do dutiny brušnej s peritonitídou; 2. súbežná obštrukcia tenkého čreva, ktorá nie je v dosahu stentu.
Relatívne – 1. dokumentovaná karcinomatóza peritonea; 2. abnormálna koagulácia, procedúra sa môže realizovať po podaní zmrazenej plazmy.
Výsledky
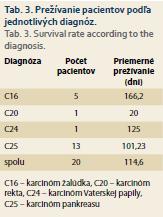
Retrospektívne sme zhodnotili efekt liečby duodenálnymi stentami u paliatívnych pacientov s GOO v dôsledku malígnej infiltrácie pylorickej a duodenálnej oblasti, zavedených na Endoskopickom pracovisku FN Trnava od roku 2013 do konca roka 2017. Celkovo bolo zavedených 26 duodenálnych SEMS u 20 pacientov (tab. 2). Výkony boli realizované u symptomatických pacientov s GOO, s vysoko pravdepodobnou (podľa zobrazovacích metód) alebo histologicky preukázanou malignitou, u ktorých performans status neumožňoval v danej chvíli chirurgické riešenie. Hlavné diagnózy, pre ktoré bol stent implantovaný, boli pokročilé karcinómy pankreasu (13 pacientov; 65 %), karcinóm žalúdka (5 pacientov; 25 %), karcinomatóza brušnej dutiny pri karcinóme rekta (1 pacient, 10 %) a karcinóm Vaterskej papily (1 pacient; 10 %). Vzhľadom na to, že išlo o paliatívnu liečbu, hlavný sledovaný cieľ bolo prežívanie pacientov (tab. 3).
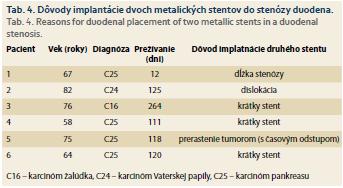
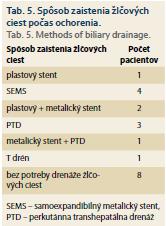
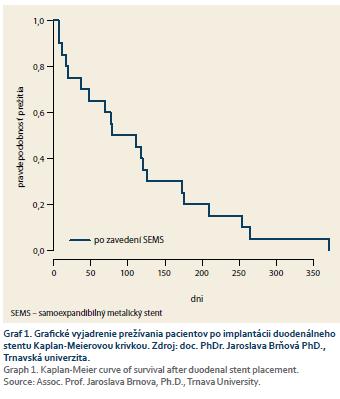
U šiestich pacientov boli zavedené dva metalické stenty, 1× z dôvodu dislokácie pri zavedení, 1× z dôvodu prerastenia malígnymi štruktúrami, 3× z dôvodu iniciálne nesprávne odhadnutej veľkosti stentu a 1× z dôvodu dĺžky stenózy, ktorá prekračovala dĺžku stentu pri jeho správnej polohe vyústenia nad pylorickým kanálom (tab. 4). Celkovo sa 4× stenty zaviedli v jednom sedení (dĺžka stenózy, krátky stent) a 2× ve dvoch nezávislých sedeniach (prípad dislokácie a prerastania). Vekový priemer pacientov bol 69,85 roka, z toho najmladší pacient mal 37 rokov a najstarší 93 rokov. Celkovo bolo 11 žien a 9 mužov. Z duodenálnych stentov sme aplikovali Wallflex uncovered (nekryté), priemeru 22 mm, dĺžky 60–120 mm (Boston Scientific). V šiestich prípadoch boli zavedené stenty dva, u väčšiny pacientov s nádorom pankreasu bolo zavedenie duodenálneho stentu nasledované zavedením biliárneho stentu, alebo perkutánnej duodenobiliárnej drenáže (tab. 5). Priemerné prežívanie pacientov bolo 114,6 dňa, najkratší čas prežívania po zavedení stentu bol 7 dní (pri fatálnej progresii základného ochorenia) a najdlhšie prežívanie bolo 370 dní. Graficky vyjadrené Kaplan-Meierovou krivkou v grafe 1. Z našich pacientov 5 (25 %) neprežili mesiac (progresia a komplikácia základného ochorenia) a ďalší 2 (10 %) neprežili viac ako 2 mesiace. U ostávajúcich 13 pacientov (65 %) bolo prežívanie dlhšie ako 2 mesiace a boli prepustení do domáceho liečenia za účelom ďalšej, prevažne podpornej liečby v rámci základného ochorenia.
U pacientov so zavedenými stentami bolo histologicky potvrdených 8 malígnych ochorení a u 12 pacientov nebola histológia dostupná. Malígne ochorenie bolo popísané na CT vyšetrení abdomenu a klinický priebeh bol natoľko závažný, že endoskopickú liečbu sme volili k zabezpečeniu základných vitálnych potrieb a v rámci najlepšej možnej podpornej liečby.
Celkovo 17 pacientov bolo prepustených z nemocničnej do domácej starostlivosti, prekladaných do hospicu alebo do zariadení sociálnej starostlivosti. U 3 pacientov bol priebeh natoľko závažný, že zomreli ešte počas pobytu v nemocnici. Počas insercie duodenálnych stentov sa v našom súbore nevyskytli bezprostredné periprocedurálne komplikácie. Obnova pasáže sa sledovala hneď na druhý postprocedurálny deň a pacienti boli ponechaní len na definovej strave, aby sa predchádzalo možnej dysfunkcii stentu z dôvodu impaktácie tuhej stravy samotnom stente.
Záver
Duodenálne stenty predstavujú efek-tívne paliatívne riešenie GOO u pacientov s malígnymi ochoreniami v pylore a duodene. Zavádzanie je endoskopicko-rádiologický postup, často s potrebou súčasného drénovania žlčových ciest. Nami používané SEMS (Wallflex, Boston Scientific) predstavujú účelne riešenie malígnych stenóz spôsobujúcich GOO a môžu prispieť k predĺženiu života a zlepšeniu kvality života pacienta a zároveň skráteniu dĺžky pobytu v nemocnici na lôžku. Predstavujú možnosť humánneho riešenia u pacientov, u ktorých prekážka v hornej časti gastrointestinálneho traktu neumožňuje prijímať potravu v tuhej ani tekutej forme a nie sú vhodní na operačné riešenie. Správna indikácia a postup pri zavedení stentu môžu efektívne zlepšiť kvalitu života, často limitovanú medicínsky neriešiteľným malígnym nádorovým ochorením. V našej skupine pacientov 65 % bolo prepustených do ambulantnej starostlivosti a priemerná dĺžka prežívania bola 114,6 dňa. U väčšiny našich pacientov s karcinómom pankreasu (92,3 %) bolo potrebné zaviesť súbežne alebo pred zavedením duodenálneho stentu i biliárnu drenáž. Periproceduálne sa závažnejšie komplikácie nevyskytli.
Zavádzanie duodenálnych SEMS je pomerne jednoduchá a pritom vysoko účinná endoskopická a rádiologická metóda riešenia GOO u paliatívnych pacientov.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Doručeno: 25. 1. 2018
Přijato: 21. 5. 2018
MUDr. Ján Ušák, Ph.D.
Gastroenterologická a endoskopická ambulancia
Interná klinika FZaSP TU a FN Trnava
A. Žarnova 11
917 75 Trnava
jan.usak@gmail.com


Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Yusuke N, Tetsuhide I, Keijiro U et al. Effectiveness of endoscopic duodenal stenting for the management of patients with unresectable pancreatic cancer. Gastroenterol Hepatol Endosc 2017; 2 (1): 1–5. doi: 10.15761/GHE.1000133.
2. Shone DN, Nikoomanesh P, Smith-Meek MM et al. Malignancy is the most common cause of gastric outlet obstruction in the era of H2 blockers. Am J Gastroenterol 1995; 90 (10): 1769–1970.
3. Jeurnink SM, Steyerberg EW, van Hooft JE et al. Surgical gastrojejunostomy or endoscopic stent placement for the palliation of malignant gastric outlet obstruction (SUSTENT study): a multicenter randomized trial. Gastrointest Endosc 2010; 71 (3): 490–499. doi: 10.1016/j.gie.2009.09.042.
4. van Hooft JE, Dijkgraaf MG, Timmer R et al. Independent predictors of survival in patients with incurable malignant gastric outlet obstruction: a multicenter prospective observational study. Scand J Gastroenterol 2010; 45 (10): 1217–1222. doi: 10.3109/00365521.2010.487916.
5. Oken M, Creech R, Tormey D et al. Toxicity and response criteria of the Eastern Cooperative Oncology Group. Am J Clin Oncol 1982; 5: 649–655.
6. Karnofsky DA, Burchenal JH. The clinical evaluation of chemotherapeutic agents in cancer. In: MacLeod CM (ed). Evaluation of chemotherapeutic agents. New York: Columbia University Press 1949: 191–205.
7. Hamada T, Hakuta R, Takahara N et al. Covered versus uncovered metal stents for malignant gastric outlet obstruction: Systematic review and meta-analysis. Dig Endosc 2017; 29 (3): 259–271. doi: 10.1111/den.12786.
8. Reppicci A. Duodenal stenting: tips and trics. Presented at: United European Gastroenterology Week 2017. October 28th – November 1st 2017.
9. Sabharwal T, Irani FG, Adam A. Quality assurance guidelines for placement of gastroduodenal stents. Cardiovasc Intervent Radiol 2007; 30 (1): 1–5.