Abstrakt
Nová doporučení odrážejí nárůst poznatků, které byly publikovány od vydání předchozího českého doporučeného postupu v září 2017. Základem pro napsání tohoto doporučeného postupu byla doporučení Evropské asociace pro studium jater (EASL) z května 2025. Podle kvalifikovaných odhadů je celosvětově chronicky infikováno virem hepatitidy B (HBV) 254 milionů lidí. Česká republika patří mezi státy s nízkou prevalencí infekce HBV. Infekce HBV může vyvolat závažná, život ohrožující poškození jater – fulminantní hepatitidu, jaterní cirhózu a hepatocelulární karcinom (HCC). Hlavním cílem léčby je prodloužit délku života a zlepšit jeho kvalitu zabráněním progrese chronické hepatitidy do jaterní cirhózy, dekompenzace cirhózy a vzniku HCC. Předpokladem dosažení tohoto cíle je trvalá suprese replikace HBV. Dalšími cíli léčby jsou prevence vertikálního přenosu infekce z matky na novorozence, zábrana reaktivace infekce HBV, léčba extrahepatálních manifestací (EHM) HBV a snížení pravděpodobnosti mezilidského přenosu HBV. Obecně jsou možné dvě strategie léčby chronické hepatitidy B – léčba nukleos (t) idovými analogy (NA) nebo pegylovaným interferonem alfa. V současnosti je naprostá většina pacientů v České republice a v celé Evropě léčena NA. Entekavir (ETV), tenofovir disoproxil fumarát (TDF) nebo tenofovir alafenamid (TAF) by měly být používány jako NA první linie léčby. Hlavní výhodou léčby vysoce účinnými NA s vysokou genetickou bariérou pro vznik rezistence je predikovatelně vysoká a dlouhodobá antivirová účinnost vedoucí k dosažení nedetekovatelné HBV DNA v séru u naprosté většiny adherentních pacientů a příznivý bezpečnostní profil těchto léků. Těmito NA může být léčen každý pacient s chronickou hepatitidou B a představují jedinou možnost léčby u pacientů s dekompenzovanou jaterní cirhózou, po transplantaci jater, s EHM infekce HBV, závažnou akutní hepatitidou B nebo exacerbací chronické hepatitidy B. Při rozhodování mezi ETV, TDF a TAF je potřeba zhodnotit komorbidity (především renální insuficienci a redukci kostní denzity) a další faktory (ženy v produktivním věku, gravidní, vyšší věk).
Preambule
Níže uvedená doporučení pro gnostiku a terapii infekce virem hepatitidy B (HBV) byla vytvořena členy pracovních skupin pro virové hepatitidy České hepatologické společnosti (ČHS) České lékařské společnosti Jana Evangelisty Purkyně (ČLS JEP) a Společnosti infekčního lékařství (SIL) ČLS JEP. Nová doporučení odrážejí nárůst poznatků, které byly publikovány od vydání předchozího doporučeného postupu ČHS a SIL v září 2017 [1,2]. Základem pro napsání tohoto doporučeného postupu byla doporučení Evropské asociace pro studium jater (EASL) z května 2025 [3]. Maximální možné dodržování odborných doporučení je podmínkou dosažení efektivní péče o nemocné s virovou hepatitidou B v celostátním měřítku. Předkládaný dokument je oporou při jednání obou odborných společností se státními orgány a s plátci zdravotní péče.
Epidemiologie HBV
Podle kvalifikovaných odhadů Světové zdravotnické organizace (WHO) žilo v roce 2022 celosvětově 254 milionů lidí chronicky infikovaných HBV. Roční incidence se odhaduje na 1,2 milionů nových infekcí HBV. Ročně umírá asi 1,08 milionů osob na důsledky infekce HBV, především na jaterní cirhózu a hepatocelulární karcinom (HCC). Předpokládá se, že mortalita spojená s infekcí HBV bude nadále narůstat z 858 tisíc v roce 2015 na 1,149 milionů v roce 2030. Konkrétně u úmrtí na HCC se předpokládá v uvedených létech nárůst z 664 tisíc na 857 tisíc a u dekompenzované cirhózy z 296 tisíc na 403 tisíc [4]. Hlavním problémem je nízká úroveň testování a špatná dostupnost léčby chronické hepatitidy B v řadě chudších zemí světa. Podle modelu vytvořeného v roce 2022 Polaris Observatory Collaborators, což je mezinárodní epidemiologická iniciativa, byla infekce dignostikována jen u 36 milionů osob s infekcí HBV a jen 6,8 milionů z 83,3 milionů k léčbě indikovaných bylo dosud léčeno [5].
Regionálně jsou obrovské rozdíly v prevalenci infekce HBV – jako nízká prevalence se bere pozitivita povrchového antigenu (HBsAg – hepatitis B surface antigen) u méně než 2 % populace, střední prevalence je 2–8 % a vysoká více než 8 % chronicky infikovaných HBV. Česká republika patří mezi státy s nízkou prevalencí infekce HBV. Podle posledních celostátních sérologických přehledů z roku 2001 bylo 0,56 % našich občanů chronicky infikováno HBV [6]. Novější výsledky z celé České republiky nejsou k dispozici. V roce 2013 byla provedena obdobná studie jen ve dvou krajích České republiky a zjištěná prevalence byla jen 0,064 % [7]. V posledních letech je u nás hlášeno méně než 50 případů akutní hepatitidy B ročně, výkyvy jsou jen minimální a lze pozorovat trvalý trend k poklesu případů tohoto závažného onemocnění. Je to důsledek dlouhodobé vakcinace významné části naší populace proti HBV. V důsledku migrace obyvatelstva došlo v posledních 4 letech k nárůstu počtu hlášených případů chronické hepatitidy B v České republice – 127 případů v roce 2021, 244 v roce 2022, 380 v roce 2023 a 429 v roce 2024. Předběžná data za rok 2025 ukazují na pokračování tohoto vzestupného trendu – 218 případů do konce června 2025 [8].
Virus hepatitidy B je prokazatelný ve většině tělesných tekutin, proto má velkou roli v šíření infekce přenos transkutánní a permukosální. V tomto směru je HBV přibližně stokrát více infekční než virus lidského imunodeficitu (HIV – human immunodeficiency virus) a desetkrát více než virus hepatitidy C (HCV). Celosvětově se infekce HBV přenáší nejčastěji sexuálním stykem. V endemických oblastech (jižní a jihovýchodní Asie, subsaharská Afrika) má velký význam vertikální cesta přenosu infekce z matky na novorozence. K tomuto přenosu dochází nejčastěji v průběhu porodu a při kojení. Pokud je matka vysoce viremická, může se HBV přenést v posledním trimestru gravidity i transplacentárně. Stále existuje řada zemí, kde se rutinně netestují dárci krve na přítomnost infekce HBV, a v těchto méně rozvinutých státech světa představuje transfuze krve a krevních derivátů reálné riziko infikování HBV. Významným rizikovým faktorem pro přenos infekce HBV je sdílení injekčního instrumentaria mezi injekčními uživateli drog, i když výskyt infekce HBV není v této rizikové skupině tak častý, jako je tomu u infekce HCV [9].
Infekce novorozenců a malých dětí jsou v současné době v České republice naprosto výjimečné díky screeningu všech těhotných žen na přítomnost HBsAg a následné pasivní a aktivní imunizaci novorozenců HBsAg pozitivních matek. Navíc od roku 2001 je v naší republice prováděna plošná vakcinace dětí proti HBV – nyní od 9. týdne věku.
Přirozený průběh a klinický obraz HBV infekce
Infekce HBV je spojena s velmi heterogenním spektrem jaterních onemocnění. Akutní hepatitida B je převážně benigní onemocnění končící ve většině případů spontánním uzdravením, v 0,1–1 % případů probíhá onemocnění fulminantně s vysokou mortalitou.
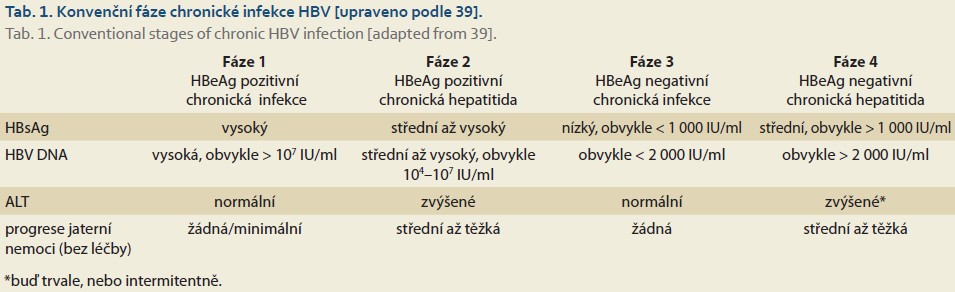
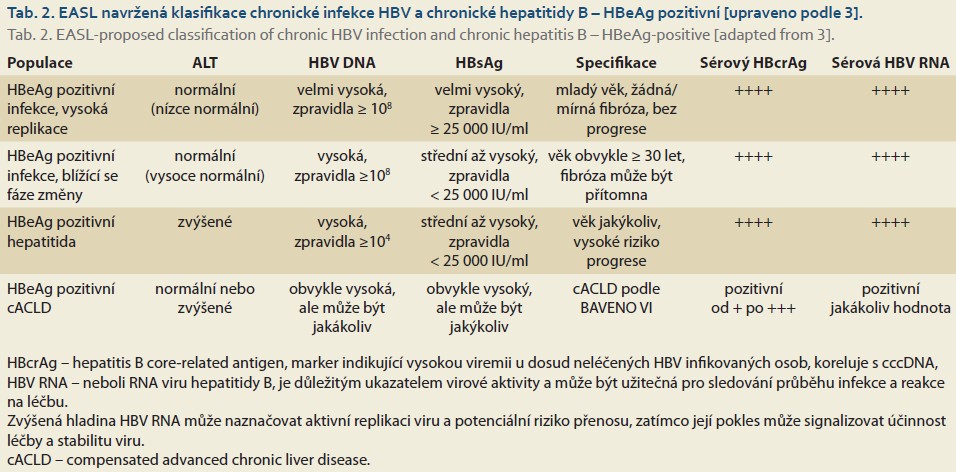
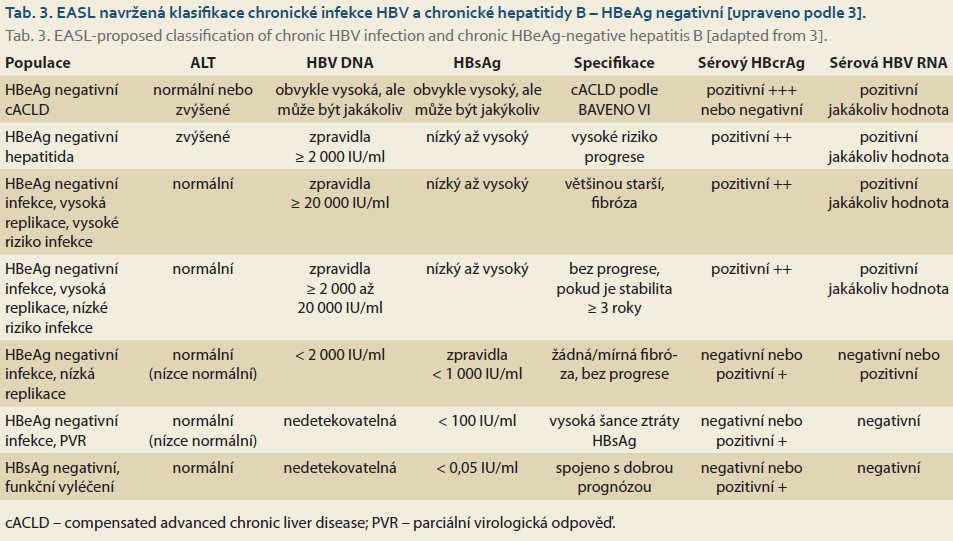
Chronická infekce HBV je označení pro infekci trvající déle než 6 měsíců. Jde o dynamický proces, který odráží interakce mezi virovou replikací a hostitelskou imunitní odpovědí. Ne všichni pacienti chronicky infikovaní HBV mají chronickou hepatitidu B. Přirozený vývoj chronické infekce HBV se schematicky dělí do čtyř fází, a to podle přítomnosti sekrečního antigenu (HBeAg – hepatitis B „e“ antigen), sérové koncentrace HBV DNA (nukleové kyseliny HBV), sérové aktivity ALT (alaninaminotransferázy) a pravděpodobné progrese jaterního zánětu bez antivirové léčby (tab. 1). Současná nomenklatura je založena na popisu dvou základních charakteristik chronicity – infekce vs. hepatitida. Chronická infekce HBV je vysoce heterogenním onemocněním, které nelze často zcela zařadit do čtyř tradičních fází. Proto vznikly termíny jako „šedá zóna (grey zone) “ nebo „intermediární fáze (intermete phase) “, které byly použity ve studiích, aby popsaly populaci pacientů, která se zcela nedá zařadit do klasických kategorií [10–12]. EASL si je vědoma, že pro klinickou praxi je nezbytná jednoduchá a praktická nomenklatura chronické infekce HBV, ale v klinickém výzkumu je potřebná přesnější klasifikace jednotlivých fází infekce HBV, aby byla podchycena složitá dynamika tohoto procesu. Proto bylo navrženo 11 odlišných kategorií pacientů založených na různých virových markerech, zánětlivé aktivitě, stadiu choroby a riziku progrese (tab. 2, 3) [3].
Screening a iniciální vyšetření pacienta s chronickou infekcí HBV
Iniciální screening infekce HBV spočívá v detekci HBsAg a protilátek anti-HBc. Když HBV infikuje hepatocyty, uvolňuje se do krevního oběhu velké množství HBsAg, což umožňuje detekci infekce HBV již v počátečních stadiích. Pro detekci HBsAg se většinou používají vysoce senzitivní enzymatické imunoeseje s dolním limitem detekce < 0,05 IU/ml (někdy i < 0,005 IU/ml). Přesto může docházet k falešné negativitě HBsAg během časných fází infekce HBV. Toto okno, kdy je HBsAg negativní a HBV DNA pozitivní, může trvat i několik týdnů. Nízké koncentrace HBsAg mohou být i u imunosuprimovaných pacientů [13].
Vstupní vyšetření pacienta s nově diagnostikovanou chronickou infekcí HBV musí zahrnovat kompletní anamnézu, fyzikální vyšetření, stanovení aktivity a pokročilosti jaterního onemocnění a sérologických markerů infekce HBV. Sexuálním partnerům a osobám žijícím ve společné domácnosti infikovaných by mělo být doporučeno testování sérologických markerů infekce HBV (HBsAg, anti-HBc celkové a třídy IgM, anti-HBs). V případě negativity těchto sérologických ukazatelů by měli být očkováni proti HBV.
Kvantitativní vyšetření HBV DNA v séru je nezbytné pro stanovení diagnózy, fáze chronické infekce HBV, rozhodnutí léčit a monitorování efektu léčby. K průkazu HBV DNA v séru se používá vysoce senzitivní polymerázová řetězová reakce (PCR). Výsledky získané touto metodou jsou udávány v mezinárodních jednotkách na mililitr (IU/ml). Dolní detekční limit této metody je 10–15 IU/ml [14].
Stanovení HBeAg a anti-HBe je zásadní pro určení fáze chronické infekce HBV.
U všech nově diagnostikovaných HBsAg pozitivních osob by měla být provedena abdominální sonografie, stanovení pokročilosti jaterního procesu neinvazivními metodami měření tuhosti jater (LSM – liver stiffness measurement), a to elastografií tranzientní (VCTE – vibration-controlled transient elastography), nebo ultrazvukovou (SWE – shear wave elastography) a (ARFI – acoustic ration force impulse imaging) i krevními testy (APRI – AST-platelet ratio index, FIB-4 – Fibrosis-4, FibroTest) [15].
Konference Baveno VI zavedla termín „compensated advanced chronic liver disease – cACLD“, pro pacienty s pokročilou jaterní fibrózou nebo časnou cirhózou, kteří jsou asymptomatičtí, ale jsou v riziku rozvoje klinicky signifikantní portální hypertenze (CSPH) a progrese jaterní choroby. Tuhost jater < 10 kPa je bezpečnou hranicí pro vyloučení cACLD a tuhost> 15 kPa je velmi podezřelá pro cACLD. U osob s tuhostí jater < 20 kPa a počtem trombocytů > 150 000 je nízká pravděpodobnost vzniku vysoce rizikových varixů a krvácení z nich, proto není nutné provádět preventivní gastrofibroskopické vyšetření [16,17]. Hraniční hodnoty VCTE-LSM jsou uvedeny v tab. 4.

Jaterní biopsie má místo v případě gnostických nejasností – různé výsledky neinvazivního vyšetření a přítomnost jaterních komorbidit.
Kvantitativní stanovení sérové koncentrace HBsAg nemůže nahradit kvantifikaci HBV DNA, ale přináší další důležité informace týkající se určení fáze chronické infekce HBV a zejména posouzení rizika ukončení léčby před vymizením HBsAg [18]. Význam kvantifikace HBsAg je patrný z tab. 5.

Významu nabývá stanovení dvou nových biomarkerů HBcrAg a HBV RNA, které umožňují posoudit intrahepatální pool kovalentně vázané cirkulární DNA (cccDNA – covalently closed circular DNA). Trvalá perzistence cccDNA v jádrech hepatocytů je podkladem pro reaktivaci a rekurenci infekce HBV u imunokompromitovaných osob nebo při imunosuprimující léčbě. Přímý průkaz cccDNA je možný jen v biopticky získaném vzorku jaterní tkáně, proto má posouzení následujících sérologických parametrů velký praktický význam. HBcrAg – hepatitis B core-related antigen, je marker indikující vysokou viremii u dosud neléčených HBV infikovaných osob, jeho kvantifikovaná hodnota v krvi dobře koreluje s úrovní cccDNA v hepatocytech. HBV RNA – neboli ribonukleová kyselina viru hepatitidy B, je důležitým ukazatelem virové aktivity a může být užitečná pro sledování průběhu infekce a reakce na léčbu. Zvýšená hladina HBV RNA může naznačovat aktivní replikaci viru a potenciální riziko přenosu, zatímco její pokles může signalizovat účinnost léčby a stabilitu viru [19–21].
Komorbidity musí být systematicky potvrzeny či vyloučeny, včetně alkoholového, autoimunitního a metabolického poškození jater, koinfekce s virem hepatitidy D (HDV), hepatitidy C (HCV) a HIV.
Testování přítomnosti protilátek proti viru hepatitidy A (HAV) by mělo být provedeno a pacienti s negativitou protilátek anti-HAV třídy IgG by měli být očkováni proti HAV.
Cíle léčby chronické infekce virem hepatitidy B
Hlavním cílem léčby je prodloužit délku života a zlepšit jeho kvalitu zabráněním progrese chronické hepatitidy do jaterní cirhózy, dekompenzace cirhózy, jaterního selhání a vzniku HCC a prodloužení délky života [3].
Protože dosažení hlavních cílů léčby lze posoudit až po mnoha letech, jsou definovány i jiné cíle, které umožňují posoudit úspěšnost léčby již dříve:
- Navození dlouhodobé suprese koncentrace HBV DNA v séru, ideálně pod dolním limitem citlivosti PCR (10–15 IU/ml), je hlavním úkolem současných terapeutických strategií.
- Ideální výsledek léčby představuje setrvalé vymizení HBsAg s/bez sérokonverze do anti-HBs. Jde o indikátor hluboké suprese replikace HBV a exprese virových proteinů.
- Normalizace ALT je doplňkovým cílem.
Dalšími cíli antivirové léčby jsou:
- U HBeAg pozitivních pacientů se za uspokojivý výsledek léčby považuje ztráta HBeAg s/bez dosažení sérokonverze HBeAg/anti-HBe v kombinaci s poklesem HBV DNA < 2 000 IU/ml, což často představuje částečnou imunitní kontrolu chronické infekce HBV.
- Pokles stupně jaterní fibrózy.
- Zlepšení extrahepatálních manifestací (EHM) infekce HBV.
- Zvýšení kvality života.
- Prevence přenosu infekce HBV.
- Prevence reaktivace a rekurence HBV.
Měnící se cíle léčby chronické infekce HBV nukleos(t)idovými analogy
Ani mnohaletá léčba nukleos(t)idovými analogy (NA) nevede u naprosté většiny osob s chronickou infekcí HBV k dosažení všech současných cílů léčby. Proto je snaha zavádět do praxe místo maximalistického cíle kompletního vyléčení s eradikací všech známek infekce HBV z jater včetně cccDNA a integrované HBV DNA, realističtější cíl označovaný jako funkční vyléčení (setrvalá ztráta HBsAg, ideálně s pozitivitou anti-HBs, nedetekovatelná HBV DNA). To souvisí s narůstající snahou ukončovat léčbu chronické infekce HBV dříve než po dosažení kompletního vyléčení, které je při v současnosti dostupné léčbě nereálné.
Význam suprese HBV DNA
- Koncentrace HBV DNA ≥ 2 000 IU/ml je spojena se zvýšeným rizikem vzniku jaterní cirhózy a HCC [22,23].
- Vztah mezi sérovou koncentrací HBV DNA a rizikem vzniku HCC není lineární.
- Signifikantně vyšší riziko HCC je při HBV DNA > 200 000 IU/ml, a to při srovnání s rizikem při koncentracích HBV DNA mezi 2 000 IU/ml a 200 000 IU/ml.
- Naopak velmi nízké riziko HCC je při HBV DNA < 2 000 IU/ml [24,25].
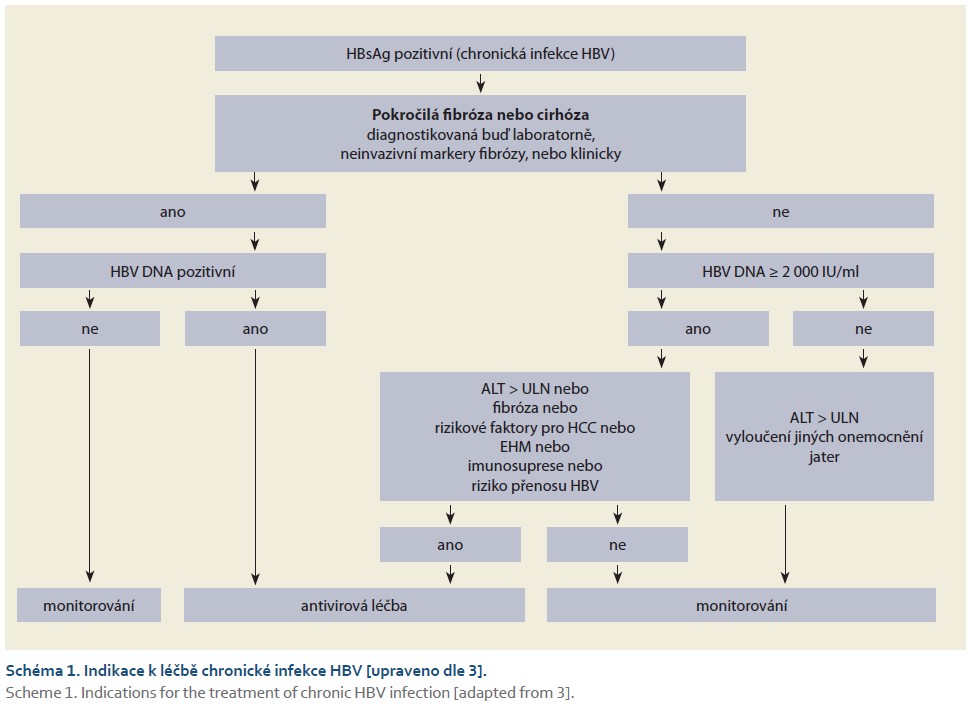
Obecné indikace k léčbě chronické hepatitidy B
- Principiálně všichni HBsAg pozitivní pacienti s prokazatelnou HBV DNA jsou kandidáty antivirové léčby. Indikace pro léčbu je primárně založena na posouzení koncentrace HBV DNA, aktivity ALT, sta fibrózy a rizika progrese jaterní nemoci a vzniku HCC.
- Všichni pacienti s HBeAg pozitivní i HBeAg negativní chronickou hepatitidou B, definovanou koncentrací HBV DNA v séru > 2 000 IU/ml, ALT > horní hranice normy (ULN – upper limit of normal) a/nebo minimálně středně těžkým zánětlivě-nekrotickým procesem nebo fibrózou, by měli být léčeni.
- Pacienti s jaterní cirhózou nebo pokročilou jaterní fibrózou (METAVIR skóre ≥ 3 v jaterní histologii nebo LSM > 8 kPa) by měli být léčeni, pokud lze u nich detekovat HBV DNA v séru (jakákoliv koncentrace), a to bez ohledu na aktivitu ALT.
- Pacienti s trvale nízkou HBV DNA (< 2 000 IU/ml) a trvale zvýšenou aktivitou ALT (> ULN) by měli být léčeni. Je však nutné určit, zda elevace ALT není způsobena jinou jaterní chorobou.
- Osoby s HBeAg pozitivní nebo HBeAg negativní chronickou infekcí HBV vyžadují individuální posouzení k určení indikací k antivirové léčbě [3].
Monitorování neléčených pacientů
Pacienty, kteří nejsou kandidáty okamžité antivirové léčby, je třeba monitorovat po stránce aktivity ALT, výše HBV DNA v séru a stupně fibrózy (neinvazivními metodami):
- Osoby s nově diagnostikovanou pozitivitou HBsAg by měly být monitorovány během prvního roku od stanovení diagnózy, nebo do zahájení antivirové léčby, a to vyšetřením HBV DNA a ALT každých 3–6 měsíců. Po této iniciální fázi je možné prodloužit intervaly mezi jednotlivými kontrolami na 6–12 měsíců v závislosti na fázi onemocnění.
- Kvantitativní testování HBsAg by mělo být prováděno každých 12 měsíců. Pokud není možnost kvantitativního testování HBsAg, je minimálním požadavkem provádění kvalitativní detekci HBsAg.
- HBeAg pozitivní pacienti by měli být testováni na přítomnost HBeAg a anti-HBe každých 12 měsíců a při každé signifikantní změně aktivity ALT.
- Frekvence provádění neinvazivních metod posuzujících progresi jaterní fibrózy závisí na fázi choroby a přítomnosti komorbidit (individuální posouzení potřeby) [3].
Léčba pacientů s HBeAg pozitivní chronickou infekcí HBV
A) U mladých pacientů (< 30 let věku), HBeAg pozitivních, s perzistentně normální aktivitou ALT, bez signifikantní fibrózy, bez rodinné anamnézy HCC a bez imunosuprimující terapie:
- Současné klinické důkazy nepodporují nutnost okamžité antivirové léčby.
- Na druhé straně má taková časná léčba potencionální benefity v redukci integrace HBV DNA a klonální expanze s ohledem na vysokou viremii u těchto osob.
B) Léčba je indikována u HBeAg pozitivní chronické infekce:
- Při zvýšeném riziku vzniku HCC.
- U osob imunokompromitovaných nebo na imunosupresivní terapii k prevenci vzniku hepatitidy.
- U vybraných osob se zvýšeným rizikem přenosu infekce na jiného člověka.
- U těhotných žen s HBV DNA ≥ 200 000 IU/ml k zábraně vertikálního přenosu [3].
Léčba pacientů s HBeAg negativní chronickou infekcí HBV
Absence HBeAg je zpravidla spojena s nižší koncentrací HBV DNA a z toho plynoucím asi 10krát nižším rizikem přenosu infekce HBV, i když riziko tohoto přenosu z člověka na člověka nelze zcela vyloučit. Proto je v některých zemích světa indikována léčba z epidemiologických důvodů u zdravotníků, aby u nich koncentrace HBV DNA byla udržována < 2 000 IU/ml nebo dokonce < 200 IU/ml, pokud vykonávají invazivní zákroky [26,27]. V České republice není tato povinnost legislativně stanovena, ale nelze předpokládat, že by to představovalo signifikantní problém – dlouhodobá vakcinace zdravotníků již před nástupem na lékařské fakulty nebo do zdravotních škol, plošná vakcinace dětí od roku 2001, která se týkala i současných mladých lékařů a sester, velmi malé zastoupení cizinců z endemických oblastí HBV mezi našimi zdravotníky.
A) Pacienti s HBeAg negativní chronickou infekcí (HBV DNA trvale < 2 000 IU/ml, perzistující normální aktivitou ALT, bez známek jaterní fibrózy) mají nízké riziko progrese nemoci a přenosu infekce HBV na jinou osobu, proto obvykle nevyžadují okamžitou antivirovou terapii.
B) Léčba je indikována u HBeAg negativní chronické infekce:
- Při zvýšeném riziku vzniku HCC.
- U osob imunokompromitovaných nebo na imunosupresivní terapii k prevenci vzniku hepatitidy.
- U vybraných osob se zvýšeným rizikem přenosu infekce na jiného člověka.
- U těhotných žen s HBV DNA ≥ 200 000 IU/ml k zábraně vertikálního přenosu [3].
Strategie léčby chronické hepatitidy B
Obecně jsou možné dvě strategie léčby chronické hepatitidy B – léčba NA nebo pegylovaným interferonem-α (PEG-IFN). V České republice se léčba PEG-IFN prakticky vůbec nepoužívá, protože není dostatek vhodných pacientů pro tuto léčbu, která má řadu závažných nežádoucích účinků a množství kontraindikací. Proto se jí v následujícím textu nebudeme blíže věnovat. V Doporučeném postupu EASL z roku 2025 je jí věnována dostatečná pozornost [3].
Hlavní výhodou léčby vysoce účinnými NA s vysokou genetickou bariérou pro vznik rezistence (ETV – entekavir, TDF – tenofovir disoproxil fumarát, TAF – tenofovir alafenamid) je predikovatelně vysoká a dlouhodobá antivirová účinnost vedoucí k dosažení nedetekovatelné HBV DNA v séru u naprosté většiny adherentních pacientů a příznivý bezpečnostní profil těchto léků. Těmito NA může být léčen každý pacient s chronickou hepatitidou B a představují jedinou možnost léčby u pacientů s dekompenzovanou jaterní cirhózou, po transplantaci jater, s EHM, akutní hepatitidou B nebo závažnou exacerbací chronické hepatitidy B. K prevenci vzniku reaktivace HBV při imunosupresi a prevenci přenosu HBV od pacientů s vysokou viremií, kteří nesplňují typická indikační kritéria pro léčbu, lze použít jen NA.
- ETV, TDF nebo TAF by měly být používány jako NA první linie léčby.
- Při rozhodování mezi ETV, TDF a TAF je potřeba zhodnotit komorbidity (především renální insuficienci a redukci kostní denzity) a další faktory (ženy ve fertilním věku, gravidní, vyšší věk) (tab. 6).
- Suprese HBV DNA je při léčbě ETV, TDF nebo TAF srovnatelná – dle výsledků klinických studií 90–100 % po 1–10 letech léčby [3].
Obecný algoritmus léčby chronické infekce HBV je patrný ze schématu 1.

Definice odpovědi na antivirovou léčbu
- Kompletní virologická odpověď (CVR) – HBV DNA nedetekovatelná při užití senzitivní eseje (< 20 IU/ml).
- Částečná (parciální) virologická odpověď (PVR) – viremie neklesá plynule a zůstává > 2 000 IU/ml.
- Virologická non-response (VNR) – pokles HBV DNA < 1 log10 za 6 měsíců léčby.
- Virologická rezistence (VR) – vzestup HBV DNA ≥ log10 od nejvyšší hodnoty (nadir) [3].
Monitorování pacientů léčených ETV, TDF nebo TAF
- Během léčby je nutné monitorovat HBV DNA a ALT každých 3–6 měsíců do dosažení virologické odpovědi, potom lze při léčbě ETV, TDF nebo TAF interval prodloužit na 6–12 měsíců.
- Detekování HBsAg každých 12 měsíců, nejlépe kvantitativně.
- U HBeAg pozitivních stanovení HBeAg/anti-HBe každých 12 měsíců.
- Ledvinné funkce posoudit před léčbou a pravidelně během léčby.
- Změna TDF na TAF nebo ETV při poklesu glomerulární filtrace (GF), objevení tubulopatie, hypofosfatemie a osteoporózy.
- Neinvazivní měření fibrózy každých 12–24 měsíců [3].
U HIV i HBV pozitivních pacientů prokázalo mnoho studií vyšší hladiny lipidů při léčbě TAF než TDF. Data z reálné praxe ukázala, že náhrada TDF režimem s TAF (bez jiných změn medikace) vedla k postupnému vzestupu hladiny LDL-cholesterolu, trvajícímu déle než 9 měsíců, zatímco hladina TGL stoupala 9–16 měsíců, než se stabilizovala. Dobře dokumentované je i přibývání na váze po náhradě TAF za TDF a může se podílet na změně lipidového spektra. U pacientů s chronickou infekcí HBV byly předchozí diabetes mellitus a hypertenze identifikovány jako rizikové faktory pro zhoršení lipidového spektra při léčbě TAF. Několik studií naopak prokázalo, že TDF má mírný vliv na pokles hladiny lipidů. Tyto skutečnosti je třeba vzít do úvahy při uvažované změně TDF za TAF, zejména u pacientů s preexistujícími metabolickými rizikovými faktory a monitorovat hladiny lipidů u léčených TAF [28–32].
Reakce v případě parciální virologické odpovědi (PVR), virologické non-response (VNR) nebo vzniku rezistence (VR) během léčby NA
- V případě PVR nebo VNR je prvním krokem kontrola adherence.
- Pokud je adherence v pořádku, je na místě testování rezistence HBV.
- Reakce v případě prokázané PVR, VNR nebo VR:
a) přechod z nukleosidového analoga (LAM – lamivudin, ETV) na TAF nebo TDF;
b) přechod z TDF nebo TAF na ETV nebo kombinaci ETV s TDF nebo TAF. - V případě perzistence nízké viremie (< 2 000 IU/ml) nebo objevení krátkodobého vzestupu HBV DNA („blip“) během léčby TDF, TAF nebo ETV není nutné okamžitě měnit léčbu, pokud nejde o pokročilou fibrózu a rezistence byla vyloučena – vysvětlením může být špatná adherence nebo snížená absorpce ze střeva.
- U pacientů s jaterní cirhózou je cílem dosáhnout nedetekovatelnou HBV DNA, ideálně do 12 měsíců léčby NA. Pokud se to nezdaří, je na místě změna léčby [3].
Rezistence vzniklá při léčbě ETV, TDF nebo TAF je velmi vzácná. Tato NA mají vysokou genetickou bariéru proti vzniku rezistence i při dlouhodobé léčbě. Proto je jejich použití při terapii první linie tak důležité, protože vznik rezistence se klinicky zpravidla projevuje jako reaktivace hepatitidy B, což je zejména u cirhotiků a pacientů s pokročilou jaterní fibrózou spojeno s vyšší morbiditou a mortalitou [33].
Genotypová rezistence k ETV je u dosud neléčených pacientů vzácná – 1,2 % během 5 let léčby. U pacientů v minulosti léčených LAM je mnohem vyšší pravděpodobnost rychlého vzniku rezistence – 6 % po 1 roce, více než 50 % po 5 letech. Proto se nemá ETV používat při léčbě pacientů s prokázanou rezistencí na LAM vůbec a po předchozí léčbě LAM se používá dvojnásobná dávka ETV, tedy 1 mg denně [34,35].
Pravděpodobnost vzniku rezistence k TDF nebo TAF je mimořádně nízká – po 5 letech léčby nebyla prokázána ani u jednoho z tenofovirových preparátů [36,37].
Kdy může být léčba NA ukončena?
Obecné možnosti ukončení léčby NA
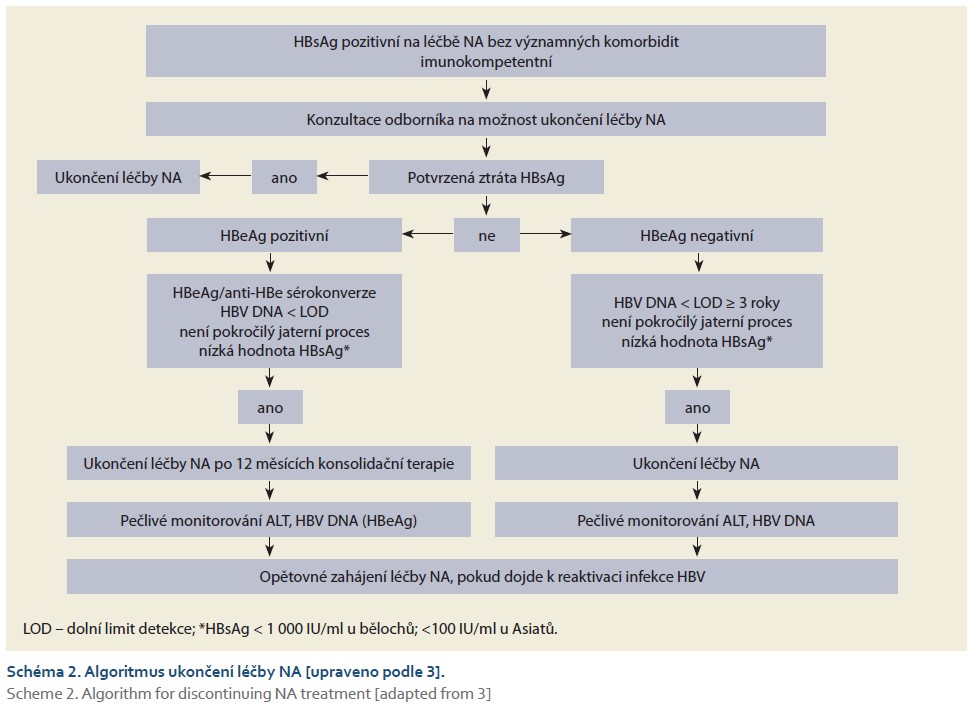
Obecný algoritmus ukončení léčby chronické infekce HBV je patrný ze schématu 2.
- Ukončení léčby NA je velmi nesnadné a zodpovědné rozhodnutí, které si vyžaduje velké zkušenosti lékaře, který antivirovou léčbu indikuje a ukončuje.
- Předem je nutné posoudit stav HBeAg, hladinu HBsAg, délku trvání suprese HBV DNA, stupeň jaterní fibrózy, komorbidity, preference a porozumění pacienta možným důsledkům ukončení léčby.
- Po konfirmované ztrátě HBsAg (s/bez anti-HBs sérokonverze) a při absenci rizikových faktorů lze léčbu NA ukončit.
- Kvantifikace HBsAg je důležitá při rozhodování o ukončení léčby NA – jako nízká hodnota HBsAg se bere u bělochů < 1 000 IU/ml, u Asiatů < 100 IU/ml (robustnější data jsou od HBeAg negativních pacientů).
- U původně HBeAg pozitivních osob bez známek pokročilého jaterního procesu lze léčbu NA ukončit 12 měsíců po konfirmované sérokonverzi HBeAg/anti-HBe a negativitě HBV DNA – pečlivá monitorace je po ukončení léčby nutná.
- U vybraných HBeAg negativních pacientů bez pokročilého jaterního procesu může být léčba ukončena před ztrátou HBsAg, pokud je HBV DNA nedetekovatelná 3–4 roky, hladina HBsAg je nízká – pečlivá monitorace je po ukončení léčby nutná.
- Kromě posouzení hodnoty HBsAg kvantifikovaně, může znalost koncentrace HBcrAg a HBV RNA pomoci v rozhodnutí o ukončení léčby – pokud jsou tato vyšetření dostupná [3].
Ukončení léčby NA po ztrátě HBsAg
- Ztráta HBsAg je při v současnosti dostupné léčbě NA velmi vzácná (většinou ročně kolem 1 %).
- Pokud dojde k negativizaci HBsAg, může to být ukazatel efektivní kontroly infekce HBV, který je spojen s nejlepší dlouhodobou prognózou.
- Po ztrátě HBsAg je možnost séroreverze (opětovné pozitivity HBsAg) vzhledem k přetrvávající perzistenci cccDNA v játrech.
- Pokud je ztráta HBsAg opakovaně potvrzena při vyšetřeních 6 měsíců od sebe, je riziko séroreverze velmi nízké.
- Po ztrátě HBsAg se jen u menší počtu léčených NA objevují protilátky anti-HBs, proto se kritéria pro ukončení léčby NA řídí primárně ztrátou HBsAg.
- Monitorování po ukončení léčby: první rok HBV DNA a ALT každé 3 měsíce, potom každých 6–12 měsíců i vzhledem k surveillance HCC.
- U pacientů s kompenzovanou jaterní cirhózou je možné léčbu ukončit jen po konfirmované sérokonverzi HBsAg/anti-HBs nebo po 12 měsících konsolidační terapie po ztrátě HBsAg.
- Hlavním problémem je fakt, že event. séroreverze HBsAg spojená se vzestupem HBV DNA může vést s jaterní dekompenzaci.
- U pacientů s dekompenzovanou cirhózou je možné léčbu ukončit jen po konfirmované sérokonverzi HBsAg/anti-HBs, podle některých autorů by se léčba neměla nikdy ukončovat [3].
Ukončení léčby NA před ztrátou HBsAg u HBeAg pozitivních
- U původně HBeAg pozitivních osob bez známek pokročilého jaterního procesu lze léčbu NA ukončit 12 měsíců po konfirmované sérokonverzi HBeAg/anti-HBe a negativitě HBV DNA – pečlivá monitorace je po ukončení léčby nutná.
- Většina dat je však od asijských pacientů, tak není úplně jasné, zda to platí i pro kavkazskou populaci.
- Heterogenní data ukazují, že nižší hodnota HBsAg v době vysazení NA zvyšuje pravděpodobnost setrvalé odpovědi (u Kavkazanů < 1 000 IU/ml, u Asiatů < 100 IU/ml – robustnější data jsou od HBeAg negativních osob).
- Ukončení léčby NA osob s přetrvávající HBeAg pozitivitou se nedoporučuje ani při dlouhodobé HBV DNA negativitě [3].
Ukončení léčby NA před ztrátou HBsAg u HBeAg negativních
- U vybraných HBeAg negativních pacientů bez pokročilého jaterního procesu může být léčba ukončena před ztrátou HBsAg, pokud je HBV DNA nedetekovatelná 3–4 roky a hladina HBsAg je nízká – pečlivá monitorace je po ukončení léčby nutná.
- V případě pokročilého jaterního onemocnění by neměla být léčba NA ukončena před vymizením HBsAg, ideálně po HBsAg/anti-HBs sérokonverzi [3].
Riziko vzniku HCC u osob s chronickou infekcí HBV
Rizikové faktory spojené se vznikem HCC u osob s chronickou infekcí HBV můžeme rozdělit na virové, hostitelské a vlivy zevního prostředí (tab. 7–10). Doporučení pro zařazení do programu surveillance HCC jsou v tab. 11.
- Jaterní cirhóza je nejvýznamnějším rizikovým faktorem HCC, i po virové supresi a event. ztrátě HBsAg riziko vzniku HCC trvá.
- Abdominální sonografie by se měla dělat každých 6 měsíců u všech rizikových pacientů – důležité je provedení zkušeným sonografistou.
- Jiné zobrazovací metody (kontrastní CT – computerová tomografie, MR – magnetická rezonance) jsou indikovány, pokud výsledek sonografie není spolehlivý.
- Onkomarkery (např. AFP – alfa1-fetoprotein) lze současně použít se zobrazovacím vyšetřením, může se tím zvýšit senzitivita průkazu časných stadií HCC, ale 10–20 % případů HCC není spojeno s elevací AFP [3].





Léčba infekce u osob s HCC
- HBsAg pozitivní pacienti s HCC mají být léčeni NA bez ohledu na výši HBV DNA.
- TDF se považuje za preferovaný lék pro terciální profylaxi po kurativní terapii HCC (resekci, lokoablativní terapii, transplantaci jater) – signifikantně nižší riziko rekurence tumoru a přežívání ve srovnání s ETV (pro použití TAF v této indikaci zatím není dostatek dat).
- Léčba NA je indikovaná i u pacientů s původně neresekovatelným HCC – zpomalení progrese tumoru, zlepšené přežívání [3].
Měla by být akutní infekce HBV antivirově léčena?
Je velmi vysoká pravděpodobnost ztráty HBsAg (> 95 %) během akutní fáze infekce HBV, proto je nepravděpodobné, že by antivirová léčba ještě zvýšila procento ztráty HBsAg a nebylo to ani dosud v literatuře dokumentováno [39].
- Antivirová léčba NA je indikována jen při poruše syntetických funkcí jater a je vhodná spolupráce s transplantačním centrem k správnému načasování transplantace jater, pokud je nezbytná
- Délka léčby NA je do ztráty HBsAg.
- Nejvíce zkušeností je s LAM, ale recentní data ukazují, že ETV, TDF nebo TAF jsou minimálně stejně účinné a bezpečné [3].
Dostupná data neprokázala, že by antivirová léčba těžkých případů akutní hepatitidy B (INR < 1,5) měla nějaký benefit na lepší přežívání nebo snížení potřeby transplantace jater [40]. Proto obecně se nyní antivirová léčba akutní hepatitidy B nedoporučuje [41]. Je i možný nepříznivý vliv časné léčby NA na potlačení HBV-specifické imunitní odpovědi a snížené pravděpodobnosti ztráty HBsAg, i když v této otázce zatím není konsenzus [40,42].
Léčba HBsAg pozitivních těhotných žen
Podle americké klasifikace US FDA Pharmaceutical Pregnancy Categories, která rozlišuje pět kategorií léků (A, B, C, D, X) podle možného ovlivnění těhotenství, patří tenofovir a telbivudin (TBV) do kategorie B, což znamená, že i když nebyly ve studiích na zvířatech popsány žádné nežádoucí účinky na plod, kontrolované lidské studie chybí, což je pochopitelné. LAM, ADV, ETV jsou zařazeny do kategorie C – v animálních studiích byly popsány nežádoucí účinky na plod. Existuje však dostatek klinických dat z klinických studií a velkých registrů těhotných, které podporují názor, že LAM, TBV i TDV a TAF jsou v těhotenství bezpečné. Dokonce i při jejich podávání v prvním trimestru gravidity nebylo popsáno zvýšené riziko fetálních malformací. Nejvíce informací o bezpečnosti NA pochází od HIV pozitivních žen léčených léky účinnými současně proti infekci HIV i HBV. Vzhledem k účinnosti a odolnosti vůči vzniku rezistence jsou TDF a TAF léky první volby během těhotenství a jako zábrana vertikálního přenosu infekce HBV [43–49].
A) Již zavedená léčba TDF nebo TAF pokračuje i v těhotenství, léčba ETV nebo ADV (pravděpodobně i LAM) by se měla změnit na TDF nebo TAF.
B) Indikace pro zahájení antivirové léčby během těhotenství:
- chronická hepatitida B s obecnými doporučeními léčit;
- HBV DNA≥ 200 000 IU/ml – zábrana vertikálního přenosu.
C) Léčba TDF nebo TAF, jako zábrana vertikálního přenosu, by měla být ideálně zahájena před začátkem posledního trimestru gravidity.
D) Tato léčba má pokračovat i po porodu k utlumení virové replikace.
E) Ženy léčené TDF nebo TAF mohou kojit.
K transplacentárnímu přenosu HBV může dojít u vysoce viremických matek navzdory pasivní a aktivní imunizaci novorozence. Toto riziko stoupá až k 30 %, pokud HBV DNA u těhotné ženy překročí 6–8 log10 IU/ml [50,51]. Toto riziko může být sníženo co nejrychlejší redukcí viremie < 200 000 IU/ml léčbou NA (přednostně tenofovirem) [43,44]. Antivirovou léčbu lze zahájit v jakémkoliv stadiu gravidity, a to včetně prvního trimestru. Nejvíce informací je ale ze studií, kdy léčba NA začínala mezi 28. a 32. týdnem gravidity [43,44,51].
Dosud nebyl popsán případ, kdyby došlo k přenosu infekce HBV od matky s viremií < 200 000 IU/ml, pokud byl novorozenec řádně pasivně a aktivně imunizován. Proto antivirová léčba není u gravidních žen s HBV DNA < 200 000 IU/ml indikována, pokud je zajištěna imunizace novorozence [43,51].
Rozhodnutí o pokračování léčby NA po porodu závisí na řadě faktorů. Pokud žena plánuje další graviditu, má chronickou hepatitidu nebo fibrózu nebo zájem pokračovat v antivirové léčbě, měla by léčba NA pokračovat. Pokud byla léčba nasazena jako prevence vertikálního přenosu a nejsou přítomny obecné indikace pro léčbu infekce HBV, může být léčba NA ukončena brzy po porodu (podle čínských doporučení za 1–3 měsíce). Je však nutné potom monitorování HBV DNA a ALT. Přesná délka podávání NA po porodu z preventivních důvodů nebyla zatím jasně stanovena. Pravděpodobně ukončení podávání NA hned po porodu signifikantně nezvyšuje riziko virologického relapsu u matky, oproti pokračování podávání 4–8 týdnů po porodu [52].
Koncentrace TAF, TDF i LAM je v mateřském mléce velmi nízká, takže expozice novorozence TDF během kojení je nižší než in utero. Podle jiné studie nebyl TAF v mateřském mléce prokázán vůbec a TDF ve velmi nízké koncentraci v mléce i pupečníkové krvi. Podle současných poznatků je možné kojit i při léčbě matky TAF nebo TDF [53–56].
Otázka snížení nebezpečí vertikálního přenosu infekce HBV císařským řezem není dosud jednoznačně vyřešena. Rutinně není sekce indikována, pokud je zajištěná řádná pasivní a aktivní imunizace novorozence co nejdříve po narození. Pokud je HBV DNA u matky v době porodu ≥ 200 000 IU/ml, může být provedení císařského řezu zváženo po rozhovoru s pacientkou, ve které jsou jí podrobně vysvětleny všechny argumenty pro a proti takovému řešení [57–61].
Léčba pacientů s dekompenzovanou jaterní cirhózou a acute-on-chronic liver failure (ACLF)
- Nemocní s dekompenzovanou jaterní cirhózou nebo ACLF a detekovatelnou HBV DNA v séru (bez ohledu na její výši) vyžadují urgentní zahájení antivirové léčby ETV, TDF nebo TAF ve specializovaných centrech s napojením na transplantační jednotky [3].
Terapie NA je vysoce účinná a bezpečná u pacientů s dekompenzovanou CIH a vede ke klinickému zlepšení – redukci rizika HCC, snížení skóre MELD a Child-Pughova skóre. Často dochází vlivem léčby ke stabilizaci stavu – více než 80 % nemocných přežívá bez potřeby transplantace jater a až u třetiny původně dekompenzovaných cirhotiků se stav kompenzuje [62,63]. Rovněž u pacientů s ACLF (akutní selhání jater nasedající na chronické jaterní onemocnění) se vlivem léčby NA zlepšuje přežívání, jaterní funkce a virologická odpověď [64–66].
U pacientů s jaterní cirhózou kompenzovanou i dekompenzovanou je cílem dosáhnout nedetekovatelnou HBV DNA, ideálně do 12 měsíců léčby NA. Při použití ETV, TDF nebo TAF je dosažení tohoto cíle velmi pravděpodobné. V minulosti byla doporučována dávka ETV u pacientů s dekompenzovanou cirhózou 1 mg denně, protože se předpokládalo, že část těchto pacientů je infikována mutantou HBV rezistentní na LAM. Novější práce považují denní dávku 0,5 mg za dostatečnou i u pacientů s dekompenzovanou cirhózou [63].
Obecně udávaným možným nežádoucím účinkem léčby NA u pacientů s dekompenzovanou cirhózou je vznik laktátové acidózy. Z tohoto důvodu je nutné pečlivé monitorování především nemocných s MELD > 22 a poškozenou funkcí ledvin.
Léčba HBV/HDV koinfekce
Kompletní doporučení pro léčbu chronické hepatitidy D jsou obsažena v EASL Clinical Practice Guidelines on Hepatitis D [67] z roku 2023 a v DP ČHS a SIL z téhož roku [68,69].
- Léčba NA by měla být podávána kompenzovaným i dekompenzovaným cirhotikům.
- Pacienti bez jaterní cirhózy s HBV DNA ≥ 2 000 IU/ml by měli být léčeni NA [3].
Podle nových poznatků zveřejněných od vydání výše vydaných doporučených postupů pro léčbu HDV léčba bulevirtidem (BLV) nezhoršuje jaterní funkce u pacientů s jaterní cirhózou a portální hypertenzí. V některých případech pokročilé, ale ne dekompenzované cirhózy, bylo pozorováno zlepšení jaterních funkcí při léčbě BLV. Největším rizikem je rebound HDV RNA po vysazení léčby BLV, a to zejména u dekompenzovaných pacientů, což může způsobit další zhoršení jaterních funkcí [70,71]. Užití BLV u nemocných s dekompenzovaným jaterním onemocněním je v současnosti stále off-label.
Léčba HBV/HIV koinfekce
Odhadem asi 3 miliony lidí jsou celosvětově koinfikovány HBV/HIV [72]. Je prokázáno zvýšené riziko progrese jaterní fibrózy a vývoje HCC při této koinfekci – riziko HCC vzrůstá časově dependentně již od HBV DNA ≥ 200 IU/ml [73].
- HBsAg pozitivní osoby s infekcí HIV by měly být léčeny NA bez ohledu na výši HBV DNA a ALT.
- Součástí antiretrovirové terapie (ART) by měl být TAF nebo TDF, pokud jsou tyto léky kontraindikovány nebo nedostupné, je možnost podávat ETV současně s plně supresivní ART.
- Monitorování léčby a event. její úprava se řídí stejnými pravidly jako léčba monoinfikovaných HBV s ohledem na současnou infekci HIV.
- ART obsahující TAF nebo TDF by neměla být ukončena vzhledem k nebezpečí virologického a biochemického relapsu po skončení léčby NA [3].
Léčba HBV/HCV koinfekce
Studie prokázaly, že koinfekce HBV/HCV zhoršuje prognózu jaterní choroby ve srovnání s HBV nebo HCV monoinfekcí, a to včetně signifikantně častějšího výskytu HCC [74,75].
- Chronická infekce se u pacientů HBsAg pozitivních léčí přímo působícími virostatiky (DAA) – účinnosti léčby infekce HCV i HBV jsou vysoké a srovnatelné s monoinfekcemi.
- Všichni HBsAg pozitivní pacienti s jaterní cirhózou by měli dostat NA během léčby DAA jako zábranu reaktivace HBV, a to i HBV DNA negativní.
- Profylaktické podávání NA je nutné během léčby hepatitidy C pomocí DAA, i když pacient nesplňuje podmínky pro léčbu chronické infekce HBV – např. HBV DNA < 2 000 IU/ml, normální ALT, absence pokročilé fibrózy/cirhózy [3].
K reaktivaci HBV dochází během léčby DAA nebo krátce po jejím skončení. Vzácně vzniká během reaktivace HBV závažný vzestup aktivity hepatitidy (flare), někdy jaterní selhání vyžadující transplantaci jater. Riziko reaktivace HBV kolísá mezi 5,9 a 24 %, flares jsou méně časté – 2–9 %. Vyšší vstupní hodnota HBsAg a HBV DNA zvyšuje nebezpečí reaktivace HBV, zatímco profylaxe NA signifikantně snižuje toto riziko – to je důležité zejména u cirhotiků. Délka profylaktického podávání NA má být nejméně 12 týdnů po skončení léčby DAA. U osob HBsAg negativních a anti-HBc pozitivních je riziko reaktivace HBV během léčby DAA nízké – 0,16–2 %, často je reaktivace přechodná a většinou není provázena vznikem „flare“ hepatitidy a séroreverzí HBsAg – proto není doporučována rutinní profylaxe NA u těchto osob s výjimkou cirhotiků [76–78].
Jaké jsou možnosti antivirové léčby dětí a adolescentů?
Pro léčbu dětí a adolescentů lze použít:
- interferon (IFN) α-2b je schválen Evropskou lékovou agenturou (EMA) a americkou FDA pro děti ve věku 1 rok a starší.
- PEG-IFNα-2a pro děti ve věku 3 let a starší.
- LAM pro děti tříleté a starší.
- ETV pro děti dvouleté a starší.
- TDF je schválen EMA pro děti dvouleté a starší, FDA pro 12leté a starší.
- TAF je schválen EMA pro děti ve věku 12 let a starší a bez ohledu na věk při hmotnosti vyšší než 35 let [3].
Profylaxe reaktivace a rekurence infekce HBV
Souhrn doporučení pro profylaxi reaktivace a rekurence infekce HBV při imunosupresivní (IS) terapii je v tab. 11–14.
- Před podáním IS léčby je vždy nutné testování přítomnosti markerů HBV (HBsAg, anti-HBc, HBV DNA).
- HBsAg pozitivní osoby začínající IS léčbu by měly podstoupit stejná vyšetření jako všechny jiné HBsAg pozitivní osoby.
- HBsAg negativní a anti-HBc pozitivní osoby by měly být před zahájením IS léčby testovány na HBV DNA.
- HBsAg pozitivní pacienti ve vysokém a středním riziku reaktivace by měli dostat profylaktickou léčbu NA.
- HBsAg pozitivní osoby v nízkém riziku reaktivace nemusí ihned dostávat profylaxi NA, ale HBV DNA u nich musí být monitorována nejméně každé 3 měsíce.
- HBsAg negativní, anti-HBc pozitivní a HBV DNA pozitivní osoby – postupuje se jako u HBsAg pozitivních osob.
- HBsAg negativní, anti-HBc pozitivní a HBV DNA negativní osoby by měly dostat profylakticky NA, pokud jsou v důsledku IS léčby ve vysokém riziku reaktivace infekce HBV.
- HBsAg negativní, anti-HBc pozitivní a HBV DNA negativní osoby, které jsou z důvodu IS léčby ve střední nebo nízkém riziku reaktivace, nemusí ihned dostávat profylaxi NA, ale HBsAg a/nebo HBV DNA u nich musí být monitorovány každé 3 měsíce [3].



Následující doporučení se týkají všech osob, které vyžadují profylaktické podávání NA.
- Obecně by se pro profylaxi reaktivace infekce HBV měly používat ETV, TDF nebo TAF.
- Délka profylaktického podávání NA není jasně stanovena, ale měla by trvat nejméně 6–12 měsíců po skončení IS terapie.
- V případě IS terapie, která vede k depleci B-buněk, by profylaxe NA měla trvat minimálně 18 měsíců po skončení IS terapie.
- V ideálním případě by ukončení profylaktického podávání NA mělo splňovat obecná kritéria pro ukončení léčby NA. To platí zejména, pokud je HBV DNA pozitivní před zahájením profylaxe NA.
Replikace HBV sama o sobě nevede k destrukci infikovaných hepatocytů, virus není ve většině případů cytopatogenní. Imunosupresivní léčba sice sníží imunitní reakci namířenou proti infikovaným hepatocytům, na druhou stranu oslabí imunitní kontrolu replikace viru. Zvyšuje se podíl infikovaných hepatocytů, replikace HBV výrazně stoupá a dosáhne úrovně, kdy již vede k přímému poškození infikovaných hepatocytů, a HBV se tím stává cytopatogenní. Klinickým korelátem popsaných pochodů je rozvoj fibrotizující cholestatické hepatitidy, což je závažné život ohrožující onemocnění, během několika týdnů vede bez účinné léčby u většiny případů k selhání jater. Stav, kdy imunosupresivní léčba vede k výraznému nárůstu replikace HBV a vzplanutí hepatitidy u dosud inaktivního nosiče HBsAg, se označuje jako reaktivace chronické hepatitidy B. Rekurencí se rozumí stav, kdy se pacient, který prodělal hepatitidu B a vymizel u něj HBsAg ze séra, stane znovu HBsAg pozitivním a replikace HBV rychle roste. Virová nukleová kyselina totiž perzistuje trvale v hepatocytech ve formě tzv. cccDNA (covalently closed circular DNA), a to i u pacientů, kteří se stali HBsAg negativními. K úplné eliminaci HBV nikdy nedojde. Stav dříve nazývaný eliminací viru je jen účinnou imunitní kontrolou replikace s poklesem viremie pod hranici detekce. Ztráta imunitní kontroly replikace viru vlivem imunosupresivní léčby tak vede k rekurenci hepatitidy B. V Doporučeném postupu EASL z roku 2025 [3] se používá jen termín reaktivace a s termínem rekurence se nepracuje. Jako reaktivace se podle EASL označuje stav charakterizovaný buď opětovnou pozitivitou HBV DNA (> 100 IU/ml), nebo séroreverzí (pozitivitou HBsAg po přechodné negativitě), nebo nejméně 10násobným vzestupem hladiny HBV DNA od vstupní hodnoty. Českým autorům se jeví dělení na reaktivaci a rekurenci jako účelné. Rovněž se domníváme, že pokud není možné adekvátně monitorovat replikaci při IS léčbě, má být profylaxe podána, a to především u HBsAg pozitivních jedinců, i když je podle doporučení EASL riziko reaktivace relativně malé. Reaktivace a rekurence infekce HBV jsou potencionálně život ohrožující situace, a proto jejich profylaxi považujeme za prioritní, zejména v průběhu IS léčby nebo po jejím skončení. Riziko jejich vzniku se kvantifikuje do 3 úrovní: vysoké (> 10 %), střední (1–10 %) a nízké (< 1 %). K reaktivaci dochází u 15–50 % inaktivních HBsAg pozitivních osob podstupujících IS terapii, po transplantaci kostní dřeně může být riziko reaktivace vyšší než 75 % [79]. Riziko vzniku rekurence infekce HBV během IS terapie je obecně nižší, ale může v některých případech přesáhnout 10 %, zejména při léčbě vedoucí k depleci B-buněk [80,81].
Během profylaxe se kontrolují ALT a HBV DNA každých 3–6 měsíců a nejméně 12 měsíců po skončení profylaxe NA. K významné části reaktivací dochází až po vysazení NA.
Hlavním virologickým projevem rekurence je znovuobjevení HBsAg v séru (séroreverze), provázené konstantně exacerbací hepatitidy (flare). Naproti tomu opětovná pozitivita sérové HBV DNA je provázena séroreverzí a exacerbací hepatitidy jen asi v polovině případů. V případě rekurence infekce HBV, charakterizované detekovatelností sérové HBV DNA nebo séroreverzí HBsAg, je nezbytné okamžité zahájení léčby NA (ETV, TDF nebo TAF), a to nejlépe ještě před vzestupem aktivity ALT. Séroreverze HBsAg může vést k těžké, dokonce fulminantní, akutní hepatitidě [3].
Prevence rekurence infekce HBV po transplantaci jater a jiných orgánů
Zdrojem infekce HBV při rekurenci po transplantaci jater (TJ) může být buď příjemce, pokud je graft od anti-HBc negativního dárce a není dostatečná profylaxe rekurence, nebo dárce, pokud je graft od anti-HBc pozitivního dárce a obsahuje cccDNA. I v případě infekce od anti-HBc pozitivního dárce se používá termín rekurence HBV, protože dochází k reaktivaci infekce HBV. Hepatitida v důsledku rekurence HBV je většinou závažná a vede často ke ztrátě orgánu (pokud není léčena). Obzvláště rychle progredující forma se označuje jako fibrotizující cholestatická hepatitida B [82].
Rekurence HBV je charakterizována pozitivitou HBsAg a/nebo pozitivitou HBV DNA a může mít tyto formy:
- pozitivita HBsAg i HBV DNA – nejčastější;
- negativita HBsAg a pozitivita HBV DNA – vzácná situace vzniklá v důsledku vytvoření „escape“ mutací v genu pro HBsAg [83].
- Standardní doporučenou profylaxí k zábraně rekurence infekce HBV po TJ je kombinace ETV, TDV nebo TAF a hyperimunního imunoglobulinu proti HBV (HBIG).
- Přednost má podávání TAF nebo ETV, protože v důsledku léčby kalcineuronovými inhibitory a kortikosteroidy je vyšší riziko renální insuficience a snížení kostní denzity, které by TDF mohl prohlubovat.
- HBIG se začíná podávat během anhepatální fáze TJ a dávkování po TJ se řídí podle koncentrace anti-HBs – cílová koncentrace je ≥ 50–100 IU/l.
- Podávání HBIG lze ukončit po TJ, pokud je dobrá adherence pacienta s léčbou NA a je nízké riziko rekurence.
- Doporučení na vysazení HBIG se různí. Většinou se shodují, že pokud je kombinovanou profylaxí dosaženo dlouhodobé HBsAg negativity, anti-HBs pozitivity a HBV DNA negativity, je možné profylaxi HBIG ukončit a pokračovat v NA.
- Vysazení HBIG se nedoporučuje při vysoké viremii v době TJ (> 100 000 IU/ml) a průkazu HCC před TJ.
- V případě séroreverze po TJ se skončí podávání HBIG a pokračuje se v podávání NA [3].
O profylaxi infekce HBV bez HBIG (HBIG-free profylaxe), tedy „pouze“ podáváním účinných NA, je možné uvažovat, pokud je nízké riziko rekurence HBV – HBV DNA je v době TJ negativní a není přítomna HDV nebo HIV koinfekce, ani HCC. Předpokladem možnosti uplatnění této strategie je účinná léčba příjemce NA před TJ. Při HBIG-free profylaxi dochází po TJ častěji k HBsAg pozitivitě než při kombinované profylaxi, ale není jasné, zda jde o inkompletní eliminaci HBsAg nebo opravdovou rekurenci infekce HBV. HBsAg pozitivita je často přechodná a zdá se, že její klinický význam je minimální [84].
Zábrana reinfekce HBV je po TJ pro konečná sta infekce HDV kruciální, protože infekce HDV při IS je velmi agresivní a není dostatek robustních dat o použití BLV v této indikaci. Proto je kombinovaná profylaxe NA a HBIG v této indikaci nutná. Zlatým standardem je doživotní podávání NA a HBIG, minimální doba této profylaxe je 24 měsíců po TJ [67].
Většina pacientů s infekcí HIV je HIV RNA a HBV DNA negativní v době TJ, takže doporučení pro profylaxi jsou principiálně stejná jako při HBV monoinfekci. Je důležité, aby ART obsahovala TAF nebo TDF. Zatím není dostatek dat pro vysazení HBIG nebo HBIG-free režim hned po TJ [85,86].
Pacient s chronickou infekcí HBV a HCC má po TJ vyšší riziko rekurence HBV (2–35 %) než bez HCC (1,9–9,7 %). Riziko je obzvláště zvýšeno při pokročilém HCC [87]. Rekurence HBV po TJ je významně asociována s rekurencí HCC v játrech a/nebo extrahepatálních lokalizacích. Rekurence HCC po TJ byla pozorována u 10–15 % HBsAg-pozitivních pacientů. Pozitivita HBV DNA nebo HBsAg u příjemce jater tedy vyvolá důvodné podezření na rekurenci HCC [88]. V současnosti se nedoporučení ukončení profylaxe HBIG ani HBIG-free režim hned po TJ u těchto pacientů.
V tab. 15 jsou uvedena všechna opatření, která je nutno provést v případě transplantace orgánu od anti-HBc pozitivního dárce příjemci, který je HBsAg negativní [3].

Transplantace jater od HBsAg pozitivního dárce je výjimečným řešením nedostatku vhodných dárců – taková játra se transplantují především HBsAg pozitivním příjemcům [89]. Všichni příjemci jater musí dostávat profylakticky ETV, TDF nebo TAF, profylaxe HBIG není potřebná, protože dárcovská játra jsou již infikována HBV a reinfekci nelze předejít. Pacient s chronickou hepatitidou D by neměl dostat játra od HBsAg pozitivního dárce.
Transplantace jiných orgánů od HBsAg pozitivního dárce je výjimečným řešením nedostatku vhodných dárců – takové orgány se transplantují především HBsAg pozitivním příjemcům, v případě HBsAg negativního příjemce je vhodná jeho aktivní a pasivní imunizace proti HBV před TJ. Příjemci jiných orgánů musí dostat profylakticky ETV, TDF nebo TAF a HBIG (pokud příjemce nemá hladinu anti-HBs >100 IU/ml) [90]. V případě transplantace kostní dřeně nebo solidního orgánu od živého dárce by měl být dárce před transplantací léčen co nejdříve účinnými NA [91].
Vakcinace proti HBV
Vakcíny proti HBV byly zpočátku derivovány z plazmy (časná 80. léta), potom nahrazeny řadou vakcín 2. generace produkovaných genetickým inženýrstvím modifikovanými savčími nebo kvasinkovými buňkami. Jejich zavedení do praxe zcela zásadně omezilo přenos infekce HBV (včetně vertikálního, nozokomiálního a profesionálního), výskyt akutních i chronických forem infekce HBV [92]. Konvenční rekombinantní vakcíny 2. generace obsahující S antigen vedou k robustní imunogenicitě u mladých, zdravých osob – vakcinace se skládá ze tří dávek. Účinnost těchto vakcín klesá u osob starších a s komorbiditami – protektivní hodnotu protilátek anti-HBs (≥ 10 IU/ml) dosáhne po 3 dávkách vakcíny < 75 % vakcinovaných. Obezita, kouření, mužské pohlaví, IS stav a chronické choroby (jaterní cirhóza, chronické renální nemoci a betes mellitus) jsou spojeny se sníženou účinností vakcinace [93,94]. Těhotné ženy mohou být vakcinovány proti HBV, i když indikace musí být pečlivě zvážena jako u všech vakcinací v těhotenství [95].
Vakcíny 3. generace mají vyšší účinnost zejména v podskupinách vakcinovaných, které odpovídají suboptimálně na konvenční vakcinaci 2. generací vakcín [96].
Univerzální vakcinace v dětském věku je doporučena co nejdříve, nejpozději před pubertou. V České republice je od roku 2001 prováděna plošná vakcinace dětí proti HBV – nyní od 9. týdne věku.
- Řádně vakcinované osoby, které jsou zdravé a mladší 40 let, není třeba testovat na hladinu anti-HBs, protektivní titr anti-HBs (> 10 IU/l) dosáhne ≥ 95 % dětí a ≥ 90 % zdravých dospělých.
- Titr anti-HBs může poklesnou < 10 IU/l během 4–10 let asi u 10–50 % zdravých osob, tyto osoby jsou však i nadále chráněny proti HBV díky robustní imunitní paměti, která přetrvává i po poklesu anti-HBs.
- Revakcinace osob, které ztratily protektivní hladinu anti-HBs, vede k významnému vzestupu titru anti-HBs během 3–7 dní.
- Tato „anamnestická“ imunitní odpověď je detekovatelná u více než 70 % vakcinovaných až 35 let po skončení základní vakcinace.
- Podle Doporučení EASL z roku 2025 by za protektivní titr anti-HBs by měla být považována hodnota ≥ 100 IU/ml, a to zejména u osob se zvýšeným rizikem těžké infekce, jako jsou osoby imunosuprimované [3].
Kombinace aktivní imunizace (vakcinace) a pasivní imunizace má zásadní význam v zábraně přenosu infekce z matky na novorozence, ke kterému jinak dochází především v období porodu a při kojení, pokud nebyl novorozenec řádně imunizován.
- Novorozenci od HBsAg pozitivních matek by měli dostat 1. dávku vakcíny co nejdříve po narození (nejpozději do 12 hodin věku, ale nejlépe během 1. hodiny života) v kombinaci s pasivní imunizací hyperimunním imunoglobulinem proti HBV (HBIG).
- Kombinace vakcinace a pasivní imunizace vede k séroprotekci u 95 % zdravých donošených novorozenců.
- Selhání tohoto přístupu je většinou spojeno s HBeAg pozitivitou nebo vysokou hodnotou HBV DNA u matky.
- Novorozenci s porodní vahou < 2 000 g mají sníženou odpověď na vakcinaci a doporučuje se u nich očkovat 4 dávkami vakcíny.
- Postvakcinační testování (anti-HBs, HBsAg) se provádí obvykle mezi 9. a 12. měsícem života – v případě anti-HBs < 10 IU/l se přidává 4. dávka vakcíny a testuje se 1–2 měsíce po ní, pokud jsou stále anti-HBs < 10 IU/l přidávají se 5. a 6. dávka vakcíny a testuje se 1–2 měsíce po 6. dávce [3].
Vakcinace osob imunosuprimovaných nebo imunodeficientních má být dvojnásobnou dávkou standardní vakcíny 2. generace nebo vakcínou 3. generace. Pacienti na hemolýze odpovídají lépe na dvojnásobnou dávku vakcíny 2. generace nebo na vakcínu 3. generace [97]. To platí i pro chronické alkoholiky [98]. Imunokompetentní HIV pozitivní osoby se očkují stejně jako zdraví jedinci, při nízké hodnotě CD4+ se podávají dvojnásobné dávky konvenční vakcíny [99]. Při očkování cirhotiků se doporučuje dvojnásobná dávka konvenční vakcíny, ale i 6 dávek vakcíny může mít suboptimální odpověď [100]. Vakcína 3. generace může být v této indikaci účinnější [101].
Séroprotektivní koncentrace anti-HBs byla stanovena ≥ 10 IU/l, ale u rizikových osob, jako jsou imunosuprimovaní se za optimální efekt vakcinace považuje koncentrace anti-HBs ≥ 100 IU/l naměřená 1–2 měsíce po poslední dávce vakcíny – to ukazuje na dlouhodobou, možná celoživotní ochranu proti HBV. Osoby s titrem anti-HBs ≥ 100 IU/l naměřeným 1–2 měsíce po poslední dávce vakcíny není třeba dále testovat s výjimkou imunosuprimovaných osob, kde by testování mělo být každých 1–10 let v závislosti na míře rizika – v případě poklesu anti-HBs < 100 IU/l je na místě booster dávka vakcíny. Rizikové osoby s anti-HBs mezi 10 a 100 IU/l 1–2 měsíce po poslední dávce vakcíny by měly dostat 4. dávku vakcíny s následnou kontrolou hladiny anti-HBs za 1–2 měsíce. Osoby s titrem anti-HBs < 10 IU/l naměřeným 1–2 měsíce po poslední dávce vakcíny se doporučuje kompletně revakcinovat 3 dávkami vakcíny, možná ve dvojnásobné jednotlivé dávce, s následnou kontrolou anti-HBs za 1–2 měsíce po skončení druhé vakcinace. Před revakcinací je vhodné zkontrolovat, zda neprobíhá infekce HBV (HBsAg, anti-HBc) [3]. Intradermální vakcinace non-responderů, i když se zdá být imunologicky výhodná, zatím neprokázala lepší efekt u imunokompromitovaných [102].
Způsob dispenzarizace pacientů s infekcí virem hepatitidy B
V České republice je ze zákona nařízena povinná izolace nemocných s akutní hepatitidou na infekčních klinikách či odděleních. Dále jsou pacienti nejméně 12 měsíců kontrolováni v jaterních poradnách při těchto pracovištích. Pokud infekce přejde do chronicity, je nutná dlouhodobá, event. celoživotní dispenzarizace v jaterních poradnách infekčních, gastroenterologických nebo interních pracovišť. V případě vzniku HCC na gastroenterologii a onkologii. Oprávnění poskytovat antivirovou léčbu chronické hepatitidy B mají pouze pracoviště garantovaná Českou hepatologickou společností a Společností infekčního lékařství České lékařské společnosti J. E. Purkyně.
Tento doporučený postup byl schválen výbory SIL ČLS JEP a ČHS ČLS JEP v září 2025.
Korespondenční autor
prof. MUDr. Petr Husa, CSc.
Klinika infekčních chorob
LF MU a FN Brno
Jihlavská 20
625 00 Brno
husa.petr@fnbrno.cz
Literatura
1. Husa P, Šperl J, Urbánek P et al. Doporučený postup gnostiky a léčby chronické hepatitidy B. Gastroent Hepatol 2014; 68(6): 514–526. doi: 10.14735/amgh2014514.
2. Husa P, Šperl J, Urbánek P et al. Diagnosis and therapy of chronic hepatitis B: Czech national guidelines. Klin Mikrobiol Infect Lek 2014; 20(4): 121–132.
3. European Association for the Study of the Liver. EASL Clinical Practice Guidelines on the management of hepatitis B virus infection. J Hepatol 2025; 83(2): 502–583. doi: 10.1016/j.jhep.2025.03.018
4. WHO. Global hepatitis report 2024: action for accession low- and middle-income countries. 2024 [online]. Dostupné z: https: //www.who.int/publications/i/item/9789240091672.
5. Polaris Observatory Collaborators. Global prevalence, cascade of care, and prophylaxis coverage of hepatitis B in 2022: a modelling study. Lancet Gastroenterol Hepatol 2023; 8(10): 879–907. doi: 10.1016/S2468-1253(23)00197-8.
6. Němeček V, Částková J, Fritz P et al. The 2001 serological survey in the Czech Republic – viral hepatitis. Cent Eur J Public Health 2003; 47(Suppl 1): S54–S61.
7. Bílková Fránková H, Kloudová A, Zelená H et al. Víceúčelový sérologický přehled (spalničky, příušnice, pertusse, virová hepatitida B) SP 2013, ČR: závěrečná zpráva, příloha č. 1. Zprávy CEM (SZÚ Praha) 2014; 23: 1–152. 2015 [online]. Dostupné z: http: //www.zuusti.cz/wp-content/uploads/2015/04/SP-2013-vnitřek-do-TISKU.pdf.
8. ISIN. Epidemiologická databáze Státního zdravotního ústavu Praha. 2025 [online]. Dostupné z: http: //www.szu.cz/publikace/data/infekce-v-cr.
9. Husa P, Urbánek P. Virová hepatitida B. In: Urbánek P, Brůha R (eds). Hepatologie. Praha: Grada Publishing: 2022: 343–355.
10. Huang DQ, Tran A, Yeh M-L et al. Antiviral therapy substantially reduces HCC risk in patients with chronic hepatitis B infection in the indeterminate phase. Hepatology 2023; 78(5): 1558–1568. doi: 10.1097/HEP.0000 000000000459.
11. Lai JC, Wong GL, Tse YK et al. Histological severity, clinical outcomes and impact of antiviral treatment in indeterminate phase of chronic hepatitis B: a systematic review and meta-analysis. J Hepatol 2025; 82(6): 992–1003. doi: 10.1016/j.jhep.2024.11.018.
12. Yapali S, Talaat N, Fontana RJ et al. Outcomes of patients with chronic hepatitis B who do not meet criteria for antiviral treatment at presentation. Clin Gastroenterol Hepatol 2015; 13(1): 193.e1–201.e1. doi: 10.1016/j.cgh.2014.07.019.
13. Pronier C, Candotti D, Boizeau L et al. The contribution of more sensitive hepatitis B surface antigen assays to detecting and monitoring hepatitis B infection. J Clin Virol 2020; 129: 104507. doi: 10.1016/j.jcv.2020.104507.
14. Fu MX, Simmonds P, Andreani J et al. Ultrasensitive PCR system for HBV DNA detection: risk stratification for occult hepatitis B virus infection in English blood donors. J Med Virol 2023; 95(10): e29144. doi: 10.1002/jmv.29144.
15. Duarte-Rojo A, Taouli B, Leung DH et al. Imaging-based noninvasive liver disease assessment for staging liver fibrosis in chronic liver disease: a systematic review supporting the AASLD Practice Guideline. Hepatology 2025; 81(2): 725–748. doi: 10.1097/HEP.0000000000000852.
16. de Franchis R, Baveno VI Faculty. Expanding consensus in portal hypertension: report of the Baveno VI Consensus Workshop: stratifying risk and individualizing care for portal hypertension. J Hepatol 2015; 63(3): 743–752. doi: 10.1016/j.jhep.2015.05.022.
17. Papatheodoridi M, Hiriart JB, Lupsor-Platon M et al. Refining the Baveno VI elastography criteria for the definition of compensated advanced chronic liver disease. J Hepatol 2021; 74(5): 1109–1116. doi: 10.1016/j.jhep.2020.11.050.
18. Cornberg M, Wong VW-S, Locarnini S et al. The role of quantitative hepatitis B surface antigen revisited. J Hepatol 2017; 66(2): 398–411. doi: 10.1016/j.jhep.2016.08.009.
19. Kramvis A, Chang KM, Dandri M et al. A roadmap for serum biomarkers for hepatitis B virus: current status and future outlook. Nat Rev Gastroenterol Hepatol 2022; 19(11): 727–745. doi: 10.1038/s41575-022-00649-z.
20. Yoshida K, Desbiolles A, Feldman SF et al. Hepatitis B core-related antigen to indicate high viral load: systematic review and meta-analysis of 10,397 individual participants. Clin Gastroenterol Hepatol 2021; 19(1): 46–60.e8. doi: 10.1016/j.cgh.2020.04.045.
21. Shimakawa Y, Ndow G, Kaneko A et al. Rapid point-of-care test for hepatitis B core-related antigen to gnosehigh viral load in resource-limited settings. Clin Gastroenterol Hepatol 2023; 21(7): 1943.e2–1946.e2. doi: 10.1016/ j.cgh.2022.05.026.
22. Chen CJ, Yang HI, Su J et al. Risk of hepatocellular carcinoma across a biological gradient of serum hepatitis B virus DNA level. J Am Med Assoc 2006; 295(1): 65–73. doi: 10.1001/jama.295.1.65.
23. Iloeje UH, Yang HI, Su J et al. Predicting cirrhosis risk based on the level of circulating hepatitis B viral load. Gastroenterology 2006; 130(3): 678–686. doi: 10.1053/j.gastro.2005.11.016.
24. Chen X, Wu F, Liu Y et al. The contribution of serum hepatitis B virus load in the carcinogenesis and prognosis of hepatocellular carcinoma: evidence from two meta-analyses. Oncotarget 2016; 7(31): 49299–49309. doi: 10.18632/oncotarget.10335.
25. Chen CJ, Yang HI, Iloeje UH et al. Hepatitis B virus DNA levels and outcomes in chronic hepatitis B. Hepatology 2009; 49(Suppl 5): S72–S84. doi: 10.1002/hep.22884.
26. Gerlich WH. Reduction of infectivity in chronic hepatitis B virus carriers among healthcare providers and pregnant women by antiviral therapy. Intervirology 2014; 57(3–4): 202–211. doi: 10.1159/000360949.
27. Incident Investigation Teams and Others. Transmission of hepatitis B to patients from four infected surgeons without hepatitis B e antigen. N Engl J Med 1997; 336(3): 178–184. doi: 10.1056/NEJM199701163360304.
28. Yoo JJ, Jung EA, Kim SG et al. Risk of dyslipidaemia in people living with HIV who are taking tenofovir alafenamide: a systematic review and meta-analysis. J Int AIDS Soc 2024; 27(9): e26358. doi: 10.1002/jia2.26358.
29. Lin S, Huang W, Liao Z et al. Comparison of lipid profile alterations in chronic hepatitis b patients receiving tenofovir alafenamideor tenofovir disoproxil fumarate. Sci Rep 2024; 14(1): 27369. doi: 10.1038/s41598-024-78656-0.
30. Hwang EG, Jung EA, Yoo JJ et al. Risk of dyslipidemia in chronic hepatitis B patients taking tenofovir alafenamide: a systematic review and meta-analysis. Hepatol Int 2023; 17(4): 860–869. doi: 10.1007/s12072-023-10528-7.
31. Mallon PWG, Brunet L, Fusco JS et al. Lipid changes after switch from TDF to TAF in the OPERA cohort: LDL cholesterol and triglycerides. Open Forum Infect Dis 2022; 9(1): ofab621. doi: 10.1093/ofid/ofab621.
32. Kanters S, Renaud F, Rangaraj A et al. Evidence synthesis evaluating body weight gain among people treating HIV with antiretroviral therapy-a systematic literature review and network meta-analysis. EClinicalMedicine 2022; 48: 101412. doi: 10.1016/j.eclinm.2022. 101412.
33. Zoutendijk R, Reijnders JG, Zoulim F et al. Virological response to entecavir is associated with a better clinical outcome in chronic hepatitis B patients with cirrhosis. Gut 2013; 62(5): 760–765. doi: 10.1136/gutjnl-2012-302024.
34. Zoulim F, Locarnini S. Hepatitis B virus resistance to nucleos (t) ide analogues. Gastroenterology 2009; 137(5): 1593–1608. doi: 10.1053/j.gastro.2009.08.063.
35. Sherman M, Yurdaydin C, Sollano J et al. Entecavir for treatment of lamivudine-refractory, HBeAg-positive chronic hepatitis B. Gastroenterology 2006; 130(7): 2039–2049. doi: 10.1053/j.gastro.2006.04.007.
36. Kitrinos KM, Corsa A, Liu Y et al. No detectable resistance to tenofovir disoproxil fumarate after 6 years of therapy in patients with chronic hepatitis B. Hepatology 2014; 59(2): 434–442. doi: 10.1002/hep.26686.
37. Chan HL, Buti M, Lim YS et al. Long-term treatment with tenofovir alafenamide for chronic hepatitis B results in high rates of viral suppression and favorable renal and bone safety. Am J Gastroenterol 2024; 119(3): 486–496. doi: 10.14309/ajg.0000000000002468.
38. European Association for the Study of the Liver. EASL Clinical Practice Guidelines: management of hepatocellular carcinoma. J Hepatol 2018; 69(1): 182–236. doi: 10.1016/j.jhep.2018.03.019.
39. European Association for the Study of the Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection. J Hepatol 2017; 67(2): 370–398. doi: 10.1016/j.jhep.2017.03.021.
40. Wiegand J, Wedemeyer H, Franke A et al. Treatment of severe, nonfulminant acute hepatitis B with lamivudine vs placebo: a prospective randomized double-blinded multicentre trial. J Viral Hepat 2014; 21(10): 744–750. doi: 10.1111/jvh.12210.
41. Mantzoukis K, Rodríguez-Perálvarez M, Buzzetti E et al. Pharmacological interventions for acute hepatitis B infection: an attempted network meta-analysis. Cochrane Database Syst Rev 2017; 3(3): CD011645. doi: 10.1002/14651858.CD011645.pub2.
42. Yu JW, Sun LJ, Zhao YH et al. The study of efficacy of lamivudine in patients with severe acute hepatitis B. Dig Dis Sci 2010; 55(3): 775–783. doi: 10.1007/s10620-009-1060-5.
43. Brown RS, McMahon BJ, Lok ASF et al. Antiviral therapy in chronic hepatitis B viral infection during pregnancy: a systematic review and meta-analysis. Hepatology 2016; 63(1): 319–333. doi: 10.1002/hep.28302.
44. Li W, Jia L, Zhao X et al. Efficacy and safety of tenofovir in preventing mother-to-infant transmission of hepatitis B virus: a meta-analysis based on 6 studies from China and 3 studies from other countries. BMC Gastroenterol 2018; 18(1): 121. doi: 10.1186/s12876-018-0847-2.
45. Shang J, Wen Q, Wang CC et al. Safety and efficacy of telbivudine for chronic hepatitis B during the entire pregnancy: long-term follow-up. J Viral Hepat 2017; 24(Suppl 1): 43–48. doi: 10.1111/jvh.12785.
46. Zeng QL, Yu ZJ, Ji F et al. Tenofovir alafenamide to prevent perinatal hepatitis B transmission: a multicenter, prospective, observational study. Clin Infect Dis 2021; 73(9): e3324–e3332. doi: 10.1093/cid/ciaa1939.
47. Ding Y, Cao L, Zhu L et al. Efficacy and safety of tenofovir alafenamide fumarate for preventing mother-to-child transmission of hepatitis B virus: a national cohort study. Aliment Pharmacol Ther 2020; 52(8): 1377–1386. doi: 10.1111/apt.16043.
48. Chen R, Zou J, Long L et al. Safety and efficacy of tenofovir alafenamide fumarate in early-middle pregnancy for mothers with chronic hepatitis B. Front Med (Lausanne) 2021; 8: 796901. doi: 10.3389/fmed.2021.796901.
49. Pan CQ, Zhu L, Yu AS et al. Tenofovir alafenamide versus tenofovir disoproxil fumarate for preventing vertical transmission in chronic hepatitis B mothers: a systematic review and meta-analysis. Clin Infect Dis 2024; 79(4): 953–964. doi: 10.1093/cid/ciae288.ciae288.
50. Wen WH, Chang MH, Zhao LL et al. Motherto-infant transmission of hepatitis B virus infection: significance of maternal viral load and strategies for intervention. J Hepatol 2013; 59(1): 24–30. doi: 10.1016/j.jhep.2013.02.015.
51. Pan CQ, Duan ZP, Bhamidimarri KR et al. Analgorithm for risk assessment and intervention of mother to child transmission of hepatitis B virus. Clin Gastroenterol Hepatol 2012; 10(5): 452–459. doi: 10.1016/j.cgh.2011.10.041.
52. You H, Wang F, Li T et al. Guidelines for the prevention and treatment of chronic hepatitis B (version 2022). J Clin Transl Hepatol 2023; 11(6): 1425–1442. doi: 10.14218/JCTH.2023.00320.
53. Ehrhardt S, Xie C, Guo N et al. Breastfeeding while taking lamivudine or tenofovir disoproxil fumarate: a review of the evidence. Clin Infect Dis 2015; 60(2): 275–278. doi: 10.1093/cid/ciu798.
54. Hu X, Wang L, Xu F. Guides concerning tenofovir exposure via breastfeeding: a comparison of drug dosages by developmental stage. Int J Infect Dis 2019; 87: 8–12. doi: 10.1016/j.ijid.2019.07.023.
55. Li S, Jin J, Jiang Y et al. Low levels of tenofovir in breast milk support breastfeeding in HBV-infected mothers treated with tenofovir disoproxil fumarate. Int J Antimicrob Agents 2023; 61(3): 106726. doi: 10.1016/j.ijantimicag.2023.106726.
56. Li B, Liu Z, Liu X et al. Efficacy and safety of tenofovir disoproxil fumarate and tenofovir alafenamide fumarate in preventing HBV vertical transmission of high maternal viral load. Hepatol Int 2021; 15(5): 1103–1108. doi: 10.1007/s12072-021-10235-1.
57. Pan YC, Jia ZF, Wang YQ et al. The role of caesarean section and nonbreastfeeding in preventing mother-to-childtransmission of hepatitis B virus in HBsAg-and HBeAg-positive mothers: results from a prospective cohort study and a meta-analysis. J Viral Hepat 2020; 27(10): 1032–1043. doi: 10.1111/jvh.13314.
58. Levy MT, Terrault NA. Caesarean section or non-breastfeeding for prevention of MTCT-beware of sending the wrong message. J Viral Hepat 2021; 28(3): 575–576. doi: 10.1111/jvh.13455.
59. Yang M, Qin Q, Fang Q et al. Cesarean section to prevent mother-to-child transmission of hepatitis B virus in China: a meta-analysis. BMC Pregnancy Childbirth 2017; 17(1): 303. doi: 10.1186/s12884-017-1487-1.
60. Chen HL, Cai JY, Song YP et al. Vaginal delivery and HBV mother to child transmission risk after immunoprophylaxis: a systematic review and a meta-analysis. Midwifery 2019; 74: 116–125. doi: 10.1016/j.midw.2019.03.024.
61. Pan CQ, Zou HB, Chen Y et al. Cesarean section reduces perinatal transmission of hepatitis B virus infection from hepatitis B surface antigen-positive women to their infants. Clin Gastroenterol Hepatol 2013; 11(10): 1349–1355. doi: 10.1016/j.cgh.2013.04.026.
62. Singal AK, Salameh H, Kuo YF et al. Meta-analysis: the impact of oral anti-viral agents on the incidence of hepatocellular carcinoma inchronic hepatitis B. Aliment Pharmacol Ther 2013; 38(2): 98–106. doi: 10.1111/apt.12344.
63. Shim JH, Lee HC, Kim KM et al. Efficacy of entecavir in treatment-naïve patients with hepatitis B virus-related decompensated cirrhosis. J Hepatol 2010; 52(2): 176–182. doi: 10.1016/j.jhep.2009.11.007.
64. Wang N, He S, Zheng Y et al. Efficacy and safety of tenofovir disoproxil fumarate versus entecavir in the treatment of acute-on-chronic liver failure with hepatitis B: a systematic review and meta-analysis. BMC Gastroenterol 2023; 23(1): 388. doi: 10.1186/s12876-023-03024-7.
65. Li J, Hu C, Chen Y et al. Short-term and long-term safety and efficacy of tenofovir alafenamide, tenofovir disoproxil fumarate and entecavir treatment of acute-on-chronic liver failure associated with hepatitis B. BMC Infect Dis 2021; 21(1): 567. doi: 10.1186/s12879-021-06237-x.
66. Peng W, Gu H, Cheng D et al. Tenofovir alafenamide versus entecavir for treating hepatitis B virus-related acute-onchronic liver failure: real-world study. Front Microbiol 2023; 14: 1185492. doi: 10.3389/fmicb.2023.1185492.
67. European Association for the Study of the Liver. EASL Clinical Practice Guidelines on hepatitis delta virus. J Hepatol 2023; 79(2): 433–460. doi: 10.1016/j.jhep.2023.05.00.
68. Husa P. Šperl J, Urbánek P et al. Doporučený postup gnostiky a léčby chronické hepatitidy D. Datum vydání doporučení. 2023. Vnitr Lek 2023; 69(8): 525–532. doi: 10.36290/vnl.2023.104.
69. Husa P, Šperl J, Urbánek P et al. Doporučený postup gnostiky a léčby chronické hepatitidy D. Klin Mikrobiol Inf Lek 2024; 29(Suppl 3): 1–9.
70. Degasperi E, Anolli MP, Uceda Renteria SC et al. Bulevirtide monotherapy for 48 weeks in patients with HDV-related compensated cirrhosis and clinically significant portal hypertension. J Hepatol 2022; 77(6): 1525–1531. doi: 10.1016/j.jhep.2022.07.016.
71. Dietz-Fricke C, Tacke F, Zöllner C et al. Treating hepatitis D with bulevirtide – real-world experience from 114 patients. JHEP Rep 2023; 5(4): 100686. doi: 10.1016/j.jhepr.2023.100686.
72. Leumi S, Bigna JJ, Amougou MA et al. Global burden of hepatitis B infection in people living with human immunodeficiency virus: a systematic review and meta-analysis. Clin Infect Dis 2020; 71(11): 2799–2806. doi: 10.1093/cid/ciz1170.
73. Kim HN, Newcomb CW, Carbonari DM et al. Risk of HCC with hepatitis B viremia among HIV/HBV-coinfected persons in North America. Hepatology 2021; 74(3): 1190–1202. doi: 10.1002/hep.31839.
74. Donato F, Boffetta P, Puoti M. A meta-analysis of epidemiological studies on the combined effect of hepatitis B and C virus infections in causing hepatocellular carcinoma. Int J Cancer 1998; 75(3): 347–354. doi: 10.1002/(SICI)1097-0215(19980130)75: 3< 347::aid-ijc4>3.0.co;2-2.
75. Shi J, Zhu L, Liu S et al. A meta-analysis of case-control studies on the combined effect of hepatitis B and C virus infections in causing hepatocellular carcinoma in China. Br J Cancer 2005; 92(3): 607–612. doi: 10.1038/sj.bjc.6602333.
76. Mücke MM, Backus LI, Mücke VT et al. Hepatitis B virus reactivation during direct-acting antiviral therapy for hepatitis C: a systematic review and meta-analysis. Lancet Gastroenterol Hepatol 2018; 3(3): 172–180. doi: 10.1016/S2468-1253(18)30002-5.
77. Serper M, Forde KA, Kaplan DE. Rare clinically significant hepatic events and hepatitis B reactivation occur more frequently following rather than during direct-acting antiviral therapy for chronic hepatitis C: data from a national US cohort. J Viral Hepat 2018; 25(2): 187–197. doi: 10.1111/jvh.12784.
78. Jaroszewicz J, Pawłowska M, Simon K et al. Low risk of HBV reactivation in a large European cohort of HCV/HBV coinfected patients treated with DAA. Expert Rev Anti Infect Ther 2020; 18(10): 1045–1054. doi: 10.1080/14787210.2020.1782189.
79. Papatheodoridis GV, Lekakis V, Voulgaris T et al. Hepatitis B virus reactivation associated with new classes of immunosuppressants and immunomodulators: a systematic review, meta-analysis, and expert opinion. J Hepatol 2022; 77(6): 1670–1689. doi: 10.1016/j.jhep.2022.07.003.
80. Cholongitas E, Haidich AB, Apostolidou-Kiouti F et al. Hepatitis B virus reactivation in HBsAg-negative, anti-HBc-positive patients receiving immunosuppressive therapy: a systematic review. Ann Gastroenterol 2018; 31(4): 480–490. doi: 10.20524/aog.2018.0266.
81. Mozessohn L, Chan KK, Feld JJ et al. Hepatitis B reactivation in HBsAg-negative/HBcAb-positive patients receiving rituximab for lymphoma: a meta-analysis. J Viral Hepat 2015; 22(10): 842–849. doi: 10.1111/jvh.12402.
82. Samuel D, Muller R, Alexander G et al. Liver transplantation in European patients with the hepatitis B surface antigen. N Engl J Med 1993; 329(25): 1842–1847. doi: 10.1056/NEJM 199312163292503.
83. Duvoux C, Belli LS, Fung J et al. 2020 position statement and recommendations of the European Liver and Intestine Transplantation Association (ELITA): management of hepatitis B virusrelated infection before and after liver transplantation. Aliment Pharmacol Ther 2021; 54(5): 583–605. doi: 10.1111/apt.16374.
84. Fung J, Wong T, Chok K et al. Long-term outcomes of entecavir monotherapy for chronic hepatitis B after liver transplantation: results up to 8 years. Hepatology 2017; 66(4): 1036–1044. doi: 10.1002/hep.29191.
85. Agüero F, Forner A, Manzardo C et al. Human immunodeficiency virus infection does not worsen prognosis of liver transplantation for hepatocellular carcinoma. Hepatology 2016; 63(2): 488–498. doi: 10.1002/hep.28321.
86. Jacob JS, Shaikh A, Goli K et al. Improved survival after liver transplantation for patients with human immunodeficiency virus (HIV) and HIV/hepatitis C virus coinfection in the integrase strand transfer inhibitor and direct-acting antiviral eras. Clin Infect Dis 2023; 76(4): 592–599. doi: 10.1093/cid/ciac821.
87. Faria LC, Gigou M, Roque-Afonso AM et al. Hepatocellular carcinoma is associated with an increased risk of hepatitis B virus recurrence after liver transplantation. Gastroenterology 2008; 134(7): 1890–1899. doi: 10.1053/ j.gastro.2008.02.064.
88. Saab S, Yeganeh M, Nguyen K et al. Recurrence of hepatocellular carcinoma and hepatitis B reinfection in hepatitis B surface antigen-positive patients after liver transplantation. Liver Transpl 2009; 15(11): 1525–1534. doi: 10.1002/lt.21882.
89. European Association for the Study of the Liver. EASL Clinical Practice Guidelines on liver transplantation. J Hepatol 2024; 81(6): 1040–1086. doi: 10.1016/j.jhep.2024.07.032.
90. Chancharoenthana W, Townamchai N, Pongpirul K et al. The outcomes of kidney transplantation in hepatitis B surface antigen (HBsAg) -negative recipients receiving graft from HBsAg-positive donors: a retrospective, propensity score-matched study. Am J Transplant 2014; 14(12): 2814–2820. doi: 10.1111/ajt.12921.
91. Hui CK, Lie A, Au WY et al. Effectiveness of prophylactic anti-HBV therapy in allogeneic hematopoietic stem cell transplantation with HBsAg positive donors. Am J Transplant 2005; 5(6): 1437–1445. doi: 10.1111/j.1600-6143. 2005.00887.x.
92. Wong GL, Hui VW, Yip TC et al. Universal HBV vaccination dramatically reduces the prevalence of HBV infection and incidence of hepatocellular carcinoma. Aliment Pharmacol Ther 2022; 56(5): 869–877. doi: 10.1111/apt.17120.
93. Fan W, Chen XF, Shen C et al. Hepatitis B vaccine response in obesity: a meta-analysis. Vaccine 2016; 34(40): 4835–4841. doi: 10.1016/j.vaccine.2016.08.027.
94. Aggeletopoulou I, Davoulou P, Konstantakis C et al. Response to hepatitis B vaccination in patients with livercirrhosis. Rev Med Virol 2017; 27(6). doi: 10.1002/rmv.1942.
95. Sheffield JS, Hickman A, Tang J et al. Efficacy of an accelerated hepatitis b vaccination program during pregnancy. Obstet Gynecol 2011; 117(5): 1130–1135. doi: 10.1097/AOG. 0b013e3182148efe.
96. A two-dose hepatitis B vaccine for adults (Heplisav-B). JAMA 2018; 319(8): 822–823. doi: 10.1001/jama.2018.1097.
97. Awad AM, Ntoso A, Connaire JJ et al. An open-label, single-arm study evaluating the immunogenicity and safety of the hepatitis B vaccine HepB-CpG (HEPLISAV-B®) in adults receiving hemolysis. Vaccine 2021; 39(25): 3346–3352. doi: 10.1016/j.vaccine.2021.05.003.
98. Rosman AS, Basu P, Galvin K et al. Efficacy of a high and accelerated dose of hepatitis B vaccine in alcoholic patients: a randomized clinical trial. Am J Med 1997; 103(3): 217–222. doi: 10.1016/s0002-9343(97)00132-0.
99. Gupta A, Fine SM, Vail RM et al. Prevention and management of hepatitis B virus infection in adults with HIV. Baltimore (MD): Johns Hopkins University 2022.
100. Rodríguez-Tajes S, Pocurull A, Lens S et al. Efficacy of an accelerated double-dose hepatitis B vaccine regimen in patients with cirrhosis. J Viral Hepat 2021; 28(7): 1019–1024. doi: 10.1111/jvh.13509.
101. Amjad W, Alukal J, Zhang T et al. Two-dose hepatitis B vaccine (Heplisav-B) results in better seroconversion than three-dose vaccine (Engerix-B) in chronic liver disease. Dig Dis Sci 2021; 66(6): 2101–2106. doi: 10.1007/s10620-020-06437-6.
102. David MC, Ha SH, Paynter S et al. A systematic review and metaanalysis of management options for adults who respond poorly to hepatitis B vaccination. Vaccine 2015; 33(48): 6564–6569. doi: 10.1016/j.vaccine.2015.09.051.