Abstrakt
Nedostatok darcovských orgánov predstavuje jeden z hlavných limitujúcich faktorov transplantácie pečene a významne prispieva k mortalite pacientov na čakacích listinách. Darcovstvo po smrti obehu (DCD – donation after circulatory death) sa v posledných desaťročiach stalo etablovanou súčasťou transplantačných programov v mnohých európskych krajinách a predstavuje významnú možnosť rozšírenia darcovského poolu. Historicky boli transplantácie z DCD darcov spojené s vyšším rizikom ischemicko-reperfúzneho poškodenia a biliárnych komplikácií. Zavedenie moderných techník strojovej perfúzie, najmä normotermickej regionálnej perfúzie (NRP) a ex vivo perfúzie (HOPE, NMP), však významne zlepšilo klinické výsledky a umožnilo dosahovať prežívanie štepu porovnateľné s transplantáciami od darcov po mozgovej smrti. Implementácia DCD programu by preto mohla významne rozšíriť darcovský pool na Slovensku, zvýšiť transplantačnú aktivitu a prispieť k zníženiu mortality pacientov na čakacej listine.
Úvod
Nedostatok orgánov na transplantáciu predstavuje dlhodobý a celosvetový problém, ktorý významne ovplyvňuje mortalitu pacientov na čakacích listinách. V oblasti transplantácie pečene (LT) je tento deficit obzvlášť výrazný, keďže ide o jedinú kauzálnu liečbu terminálnych štádií chronických ochorení pečene, jej akútneho zlyhania a niektorých onkologických gnóz. Európske transplantačné programy boli historicky založené predovšetkým na darcoch po smrti mozgu (DBD – donation after brain death). Postupne sa však ukázalo, že samotný DBD program nedokáže pokryť narastajúce potreby [1–3].
V Slovenskej republike bolo v období 27. 5. 2008 – 31. 12. 2025 realizovaných 543 LT, z toho 468 v Transplantačnom centre Banská Bystrica (TC BB) (archív TC BB). Program dosahuje stabilné 1-, 5- a 10-ročné prežívanie porovnateľné s európskymi centrami. Napriek tomu pretrváva významná mortalita na čakacej listine (WL – waiting list) – priemerná mortalita dosahuje 16 %. Priemerná čakacia doba na LT na Slovensku je 17,1 týždňa. Tieto údaje poukazujú na limitovaný darcovský pool ako hlavný systémový problém.
Donation after circulatory death (DCD), teda darcovstvo po smrti obehu, predstavuje významnú možnosť rozšírenia darcovského poolu a jednu z pôvodných foriem získavania orgánov na transplantáciu. V začiatkoch transplantačnej medicíny v 50. a 60. rokoch 20. storočia boli takmer všetky orgány získavané práve po zástave obehu, pretože koncept mozgovej smrti ešte nebol uznesene definovaný. Prvé úspešné transplantácie obličiek využívali práve orgány od darcov po cirkulačnej smrti.
V roku 1968 bola publikovaná Harvardská definícia mozgovej smrti, ktorá umožnila rozvoj DBD.V dôsledku toho sa využívanie DCD darcov na niekoľko desaťročí výrazne znížilo, keďže DBD poskytovalo v tom čase lepšie podmienky pre zachovanie orgánov a logistiku transplantácie.
Znovuobnovený záujem o DCD nastal v 90. rokoch 20. storočia ako reakcia na rastúci nedostatok darcovských orgánov. Dôležitým krokom bolo zavedenie Maastrichtskej klasifikácie v roku 1995, ktorá systematicky rozdelila DCD darcov do kategórií podľa okolností smrti. Táto klasifikácia sa stala základom pre klinickú prax a výskum v oblasti DCD [4–6].
Podľa prehľadovej práce Council of Europe sa DCD stal etablovanou súčasťou transplantačných programov vo viacerých európskych krajinách vrátane Španielska, Francúzska, Spojeného kráľovstva, Belgicka, Holandska, Slovinska a Českej republiky [1–3]. Naopak, niektoré krajiny, napríklad Nemecko, DCD program legislatívne neumožňujú, čo sa odráža v obmedzenej možnosti expanzie transplantačnej aktivity.
Cieľom tohto prehľadu je analyzovať význam DCD programu v európskom kontexte, porovnať skúsenosti okolitých krajín a zdôrazniť potrebu implementácie DCD programu na Slovensku, vrátane nevyhnutnosti využívania moderných techník strojovej perfúzie – tzv. machine perfusion.
Definícia a klasifikácia DCD
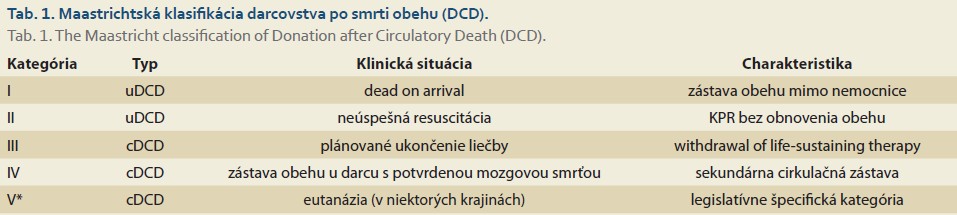
DCD označuje odber orgánov po potvrdení ireverzibilného zastavenia cirkulácie a respiračných funkcií. Maastrichtská klasifikácia (tab. 1) rozlišuje kontrolované (cDCD) a nekontrolované (uDCD) formy na základe okolností vzniku zástavy obehu. V súčasnej európskej praxi dominuje cDCD (kategória III), ktoré prebieha po plánovanom ukončení liečby u pacientov napr. s devastujúcim, či ireverzibilným poškodením mozgu alebo iným stavom s nepriaznivou prognózou [7,8].
Z patofyziologického hľadiska je DCD spojené s obdobím teplej ischémie pred začiatkom orgánovej perfúzie. Funkčná teplá ischémia (fWIT – functional warm ischemia time), definovaná ako interval od poklesu perfúzneho tlaku a saturácie kyslíkom pod kritické hodnoty až po začiatok studenej perfúzie, spúšťa komplexnú kaskádu ischemicko-reperfúzneho poškodenia (IRI). Tá zahŕňa mitochondriálnu dysfunkciu, akumuláciu sukcinátu počas ischémie a jeho rýchlu oxidáciu po reperfúzii s následnou masívnou tvorbou reaktívnych foriem kyslíka (ROS), kalciovú dysreguláciu, poškodenie endotelu a aktiváciu vrodenej imunitnej odpovede prostredníctvom uvoľňovania damage-associated molecular patterns (DAMPs) [9–11]. Žlčové cesty sú obzvlášť citlivé na hypoxiu, najmä vzhľadom na ich závislosť od peribiliárneho vaskulárneho plexu a limitovanú regeneračnú kapacitu cholangiocytov. Preto boli LT od DCD darcov historicky spojené s vyšším výskytom neanastomotických striktúr žlčových ciest a ischemickej cholangiopatie v porovnaní s LT od DBD [12,13]. Historicky boli výsledky LT z DCD darcov spojené so zvýšeným rizikom primárnej afunkcie štepu, závažnejšieho IRI, vyššej incidencie biliárnych komplikácií a nižšieho prežívania štepu [14].
V poslednom desaťročí však pokrok v oblasti optimalizácie výberu darcov, skracovania fWIT a zavedenie regionálnych perfúznych techník – najmä normotermickej regionálnej perfúzie (NRP) – ako aj ex situ strojovej perfúzie (hypotermická oxygenovaná perfúzia – HOPE; normotermická strojová perfúzia – NMP) zásadne zmenili klinické výsledky [13,15–18]. Randomizované a observačné štúdie preukázali, že použitie HOPE významne znižuje výskyt neanastomotických striktúr a zlepšuje skorú funkciu štepu (16). NRP u kontrolovaného DCD vedie k redukcii IRI a k výsledkom prežívania porovnateľným s DBD LT [16,17]. Súčasné údaje z európskych registrov naznačujú, že pri aplikácii moderných perfúznych stratégií sa prežívanie štepu aj pacienta po cDCD LT približuje výsledkom dosahovaným pri DBD darcoch [18].
Európsky vývoj DCD programu
Podľa analýzy Eden et al. bolo v medzinárodnom porovnaní ponúknutých viac ako 34 000 DCD pečení, pričom približne 9 780 bolo transplantovaných [19]. Miera využitia graftov sa výrazne líšila medzi krajinami a bola úzko spojená s implementáciou techník strojovej perfúzie (machine perfusion). Krajiny so zavedeným programom NRP alebo ex situ perfúzie dosahovali vyššiu akceptačnú mieru orgánov. Müller et al. poukazujú na významné rozdiely v transplantačnej aktivite v rámci Európy. V krajinách so silným DCD programom tvorí DCD podiel viac než 20 % všetkých LT, zatiaľ čo v krajinách bez DCD je transplantačná aktivita limitovaná výlučne DBD darcami [20]. Skúsenosti zo Slovinska a Českej republiky ukazujú, že aj stredoeurópske krajiny môžu postupne a bezpečne implementovať DCD program, pokiaľ je zabezpečený jasný legislatívny rámec, odborný konsenzus a koordinácia medzi centrami [21,22]. Tieto modely sú relevantné pre Slovenskú republiku z hľadiska populačnej veľkosti a organizačnej štruktúry zdravotníctva.
Česká republika vs. Nemecko – modelový príklad
Vďaka proaktívnemu prístupu pertinentných orgánov a klinických pracovísk patrí Česká republika medzi krajiny, ktoré DCD program systematicky implementovali v rámci existujúceho transplantačného systému. Česká legislatíva umožňuje konštatovanie smrti na základe ireverzibilného zastavenia obehu a systém je založený na princípe predpokladaného súhlasu. Tento právny rámec vytvoril podmienky pre eticky kontrolované zavedenie najmä kategórie kontrolovaného DCD (Maastricht III) [23].
Podľa údajov európskych registrov a národných transplantačných štatistík sa podiel DCD darcov v Českej republike v posledných rokoch pohybuje približne v rozmedzí 10–20 % zo všetkých zosnulých darcov, v závislosti od konkrétneho roku a typu orgánu [24,25] (KST ČR). V oblasti LT predstavujú DCD štepy v Českej republike menší, ale stabilný podiel, pričom ich implementácia prispela k udržaniu celkového počtu transplantácií aj v obdobiach kolísania počtu DBD darcov. Európske dáta ukazujú, že krajiny využívajúce DCD dosahujú väčšiu flexibilitu systému a širší darcovský pool, čo sa premieta do stabilnejšej transplantačnej aktivity [20,26]. Celkovo sa v Európe podiel DCD pri LT pohybuje približne medzi 5 a 20 %, pričom niektoré krajiny (napr. Spojené kráľovstvo či Holandsko) dosahujú aj vyššie hodnoty [20]. Česká republika a jej model predstavuje úspešný príklad implementácie DCD v regióne bývalej V4, kde je legislatívne a organizačné prostredie porovnateľné. Zavedenie DCD tak prispelo k rozšíreniu darcovskej základne a k zvýšeniu odolnosti systému voči poklesu DBD darcov. Naopak, Nemecko DCD program legislatívne neumožňuje a transplantačný systém je plne závislý od darcov DBD. Podľa analýzy európskej transplantačnej aktivity zaznamenalo Nemecko v poslednom desaťročí pokles počtu LT, pričom celková transplantačná aktivita zostáva pod úrovňou viacerých porovnateľných európskych krajín [20]. V kontexte celoeurópskeho vývoja, kde sa časť krajín snaží kompenzovať pokles DBD práve prostredníctvom DCD, predstavuje absencia tejto stratégie významné štrukturálne obmedzenie darcovského poolu. Európske registre zároveň uvádzajú, že moderné technológie (NRP, ex vivo strojová perfúzia), významne zlepšili výsledky DCD pri LT a postupne redukujú rozdiely v krátkodobom prežívaní medzi DBD a DCD štepmi [27,28]. V situácii, keď je v Nemecku 100 % transplantácií realizovaných výlučne z DBD darcov, zostáva systém zraniteľnejší voči demografickým zmenám a poklesu incidencie mozgovej smrti [20].
Klinické výsledky DCD transplantácií v ére zavedenia techník strojovej perfúzie
Rozvoj techník strojovej perfúzie zásadne zmenil prognózu DCD štepov. HOPE, NMP, a NRP preukázali schopnosť znížiť IRI a redukovať komplikácie. NRP umožňuje obnoviť regionálnu perfúziu orgánov po potvrdení smrti darcu. Tento postup stabilizuje metabolický stav orgánu ešte pred explantáciou a významne redukuje riziko biliárnych komplikácií. HOPE redukuje mitochondriálnu dysfunkciu a oxidačný stres počas reperfúzie. NMP umožňuje funkčné hodnotenie graftu vrátane monitorovania laktátu, produkcie žlče a hemodynamických parametrov, čím znižuje mieru nevyužitých orgánov. Systematická analýza Mastrovangelis et al. ukázala, že použitie NRP pri cDCD je spojené s porovnateľným prežívaním štepu a pacienta ako pri DBD LT [29]. Bonaccorsi-Riani et Brüggenwirth uvádzajú zníženie biliárnych komplikácií a zlepšenie jednoročného prežívania štepu až na 90 % pri použití HOPE [30,31]. Longchamp et al. zdôrazňujú, že moderné perfúzne techniky znižujú incidenciu ischemickej cholangiopatie, ktorá bola historicky najzávažnejšou komplikáciou DCD LT [32]. Strojová perfúzia sa postupne stáva štandardom starostlivosti pri DCD transplantáciách v popredných európskych centrách.
Ekonomické a systémové aspekty
Hoci zavedenie strojovej perfúzie predstavuje významnú počiatočnú investíciu, analýzy z viacerých centier poukazujú na dlhodobú nákladovú efektivitu tohto prístupu. Zníženie počtu nevyužitých orgánov, redukcia reoperácií a nižšia incidencia retransplantácií môžu dlhodobo kompenzovať vstupné náklady. Wehrle et al. v multicentrickej analýze uvádzajú, že využitie NMP umožňuje rozšírenie využiteľnosti marginálnych štepov [33]. Z pohľadu zdravotníckeho systému môže DCD program prispieť k skráteniu čakacích dôb a zníženiu mortality na WL – čo je v kontexte 16% mortality v SR klinicky mimoriadne relevantné.
Potreba implementácie DCD programu na Slovensku
Slovenská republika v súčasnosti nepatrí medzi krajiny s etablovaným programom DCD. V kontexte súčasného európskeho vývoja, kde viaceré štáty systematicky využívajú DCD ako nástroj na stabilizáciu a rozšírenie darcovského poolu, predstavuje absencia tejto stratégie potenciálnu štrukturálnu nevýhodu z hľadiska dostupnosti orgánov a dlhodobej udržateľnosti transplantačného systému. Krajiny, ktoré implementovali DCD program, zaznamenali rozšírenie darcovského poolu v rozsahu približne 10–30 %. V podmienkach Slovenskej republiky by zavedenie DCD a zvýšenie darcovského poolu predstavoval významný posun v transplantačnej aktivite. Pri 468 realizovaných LT v TC BB by nárast znamenal potenciálne desiatky ďalších LT. Z pohľadu populačnej medicíny by to mohlo mať zásadný dopad na mortalitu pacientov zaradených na čakaciu listinu. Ak aktuálna mortalita dosahuje 16 %, zvýšenie dostupnosti orgánov by mohlo viesť k jej významnému zníženiu, a to nielen prostredníctvom zvýšenia počtu realizovaných LT, ale aj prostredníctvom skrátenia času rizika progresie ochorenia, dekompenzácie ochorenia u pacientov. Z makroekonomického hľadiska je LT v dlhodobom horizonte nákladovo efektívnejšia než konzervatívna liečba terminálnych štádií hepatálnych ochorení.
Implementácia DCD programu v Slovenskej republike by mala viacrozmerný efekt:
- zvýšenie darcovského poolu, čo by priamo zvýšilo transplantačnú kapacitu systému;
- zníženie mortality pacientov na WL, prostredníctvom skrátenia čakacej doby a rýchlejšej dostupnosti orgánov;
- skrátenie priemernej čakacej doby a zníženie klinického rizika pre pacientov;
- harmonizáciu slovenského transplantačného systému s odporúčaniami Council of Europe a European Association for the Study of the Liver (EASL), ktoré podporujú využívanie všetkých eticky a medicínsky akceptovaných zdrojov orgánov [2,3];
- posilnenie odbornej a logistickej spolupráce so susednými krajinami, najmä s tými, ktoré už majú skúsenosti s implementáciou DCD – predovšetkým s Českou republikou.
Z pohľadu systémového plánovania tak možno konštatovať, že absencia DCD programu v Slovenskej republike predstavuje potenciálnu rezervu v oblasti rozvoja transplantačnej medicíny. Zavedenie kontrolovaného DCD programu by mohlo významne prispieť k zvýšeniu dostupnosti orgánov, zníženiu mortality pacientov na WL a k zosúladeniu slovenského transplantačného systému s aktuálnymi európskymi trendmi.
Kľúčové predpoklady implementácie DCD programu na Slovensku
Zavedenie programu DCD si vyžaduje komplexný a organizačne koordinovaný prístup. Skúsenosti európskych krajín, ktoré úspešne implementovali cDCD, ukazujú, že efektívnosť a bezpečnosť programu závisí od jasne definovaného právneho rámca, štandardizovaných klinických protokolov a integrácie moderných perfúznych technológií [1–3,20].
Legislatívne ukotvenie definície smrti obehu
Základným predpokladom implementácie DCD je jednoznačné ukotvenie smrti definovanej ako ireverzibilné zastavenie obehu. Council of Europe vo svojich odporúčaniach zdôrazňuje potrebu presnej a transparentnej definície momentu smrti, vrátane stanovenia „no-touch period“, ktorá minimalizuje riziko autorecirkulácie [1–3,23].
Vytvorenie protokolu pre cDCD
Kľúčovým krokom je vypracovanie jednotného protokolu pre cDCD, ktorý bude harmonizovaný s medzinárodnými odporúčaniami [3,20,23]. Jednotný protokol znižuje variabilitu medzi centrami a zvyšuje bezpečnosť aj kvalitu odobratých orgánov.
Povinné oddelenie rozhodovania o ukončení život udržiavajúcej liečby (WLST – withdrawal of life-sustaining therapy) od transplantačného procesu
Jedným zo základných etických princípov DCD je striktné oddelenie rozhodovania o ukončení život udržiavajúcej liečby (WLST – withdrawal of life-sustaining therapy) od transplantačného tímu. Rozhodnutie o WLST musí byť plne nezávislé od úvah o darcovstve orgánov [1,2,33]. Tento princíp minimalizuje konflikt záujmov a posilňuje dôveru verejnosti v transplantačný systém.
Školenie odberových a transplantačných tímov
Implementácia DCD si vyžaduje špecifické odborné zručnosti, najmä v oblasti manažmentu WIT, hemodynamickej stability a koordinácie medzi intenzívnou medicínou a transplantačnými centrami. Skúsenosti z krajín s etablovaným DCD programom poukazujú na potrebu systematického tréningu a simulácií [25]. Nedostatočná pripravenosť personálu je jedným z faktorov zvyšujúcich riziko komplikácií a zníženej kvality graftov.
Centralizovaná implementácia NRP
NRP sa v moderných transplantačných systémoch stala štandardom pri cDCD, najmä v oblasti LT [26,27]. Centralizované zavedenie NRP zabezpečuje štandardizáciu kvality a optimalizáciu výsledkov.
Postupné zavádzanie HOPE a NMP
HOPE a NMP predstavujú významný pokrok v oblasti ex vivo ochrany orgánov [25,26]. Bez integrácie strojovej perfúzie by expanzia DCD programu bola limitovaná vyšším rizikom komplikácií. Moderné perfúzne techniky by preto mali byť integrálnou súčasťou implementačného procesu.
Vytvorenie národného registra výsledkov a systematický audit
Transparentnosť a kontrola kvality sú základom udržateľnosti transplantačného programu. Vytvorenie registra DCD transplantácií umožní monitorovanie:
- prežívania graftu a pacienta;
- incidencie komplikácií;
- miery vyradenia orgánov;
- čakacej mortality.
Council of Europe odporúča systematický audit a medzinárodnú výmenu dát ako nástroj kontinuálneho zlepšovania kvality [2]. Bez pravidelného hodnotenia výsledkov by nebolo možné objektívne posúdiť efektívnosť programu.
Protokol pre DCD pečeň
Výber darcu (donor selection)
Protokol cDCD (Maastricht III) by mal zahŕňať prísne selekčné kritériá s cieľom minimalizovať riziko komplikácií. Medzinárodné odporúčania odporúčajú:
- vek darcu spravidla < 65–70 rokov (individuálne posúdenie);
- absenciu pokročilej steatózy (>30–40 %);
- krátky očakávaný interval medzi WLST a zástavou obehu;
- obmedzenie funkčnej teplej ischémie (fWIT).
Podľa európskych skúseností by fWIT nemal presiahnuť 20–30 min, pričom dlhšie intervaly sú asociované so zvýšeným rizikom biliárnych komplikácií [20,26].
Postup po rozhodnutí o WLST a konštatovaní smrti
Rozhodnutie o WLST musí byť striktne oddelené od transplantačného procesu [2]. Po zástave obehu nasleduje:
- definovaná „no-touch period“, aspoň 5 min;
- potvrdenie ireverzibility zástavy obehu, ktoré si v tomto prípade vyžaduje splnenie minimálne dvoch z nasledujúcich troch kritérií:
a) preukázateľné zistenie absencie elektrickej aktivity na EKG;
b) preukázateľné zistenie absencie pulzovej krivky pri invazívnom monitorovaní krvného tlaku;
c) preukázateľné zistenie absencie mechanickej aktivity srdca pri ultrazvukovom vyšetrení srdca [23];
- okamžitá iniciácia odberového procesu alebo NRP.
Tento postup minimalizuje fWIT a zvyšuje šancu na zachovanie kvality štepu.
NRP ako štandard
V moderných európskych transplantačných programoch sa NRP považuje za štandard pri DCD pečeni [26]. NRP umožňuje:
- obnovenie oxygenovanej perfúzie brušných orgánov;
- zníženie ischemicko-reperfúzneho poškodenia;
- lepšie zhodnotenie funkčnej viability pečene pred explantáciou.
Štúdie preukázali, že využitie NRP významne redukuje incidenciu ischemickej cholangiopatie v porovnaní s tradičným rýchlym odberom bez regionálnej perfúzie [28].
Centralizovaná implementácia NRP by mala byť súčasťou stratégie, aby sa zabezpečila jednotná kvalita a minimalizovali sa regionálne rozdiely.
Ex vivo strojová perfúzia (HOPE/NMP)
Po explantácii by mala nasledovať ex vivo perfúzia:
- HOPE (hypothermic oxygenated perfusion) – redukuje oxidačný stres a mitochondriálne poškodenie;
- NMP (normothermic machine perfusion) – umožňuje funkčné testovanie graftu (laktátová clearance, produkcia žlče, stabilita hemodynamických parametrov) [27,28].
Bez integrácie týchto technológií by expanzia DCD programu bola spojená s vyšším rizikom komplikácií a potenciálnym zvýšením podielu nevyužitých štepov.
Perioperačný a pooperačný manažment
Protokol DCD pečene by mal zahŕňať:
- optimalizovanú imunosupresiu;
- intenzívne monitorovanie funkcie graftu (ALT, AST, bilirubín, INR);
- včasnú gnostiku biliárnych komplikácií;
- multidisciplinárny prístup zahŕňajúci hepatológa, transplantačného chirurga a intenzivistu.
Audit a hodnotenie výsledkov
Súčasťou implementácie musí byť register DCD LT, ktorý bude systematicky sledovať:
- prežívanie štepu a pacienta (1- a 5-ročné);
- incidenciu ischemickej cholangiopatie;
- mieru primárnej dysfunkcie graftu;
- podiel vyradených orgánov;
- mortalitu na WL.
Implementácia DCD programu s jasne definovaným protokolom pre LT predstavuje komplexný, ale realizovateľný proces. Kľúčovými piliermi sú legislatívna jasnosť, etická integrita, štandardizované klinické postupy a integrácia moderných perfúznych technológií (NRP, HOPE, NMP). Bez ich systematického zavedenia by expanzia DCD programu mohla byť limitovaná zvýšeným rizikom komplikácií. Naopak, ich integrácia umožňuje bezpečné rozšírenie darcovského poolu pri zachovaní vysokých klinických štandardov.
Záver
DCD predstavuje významnú a overenú možnosť rozšírenia darcovskej základne v programoch orgánových transplantácií. Európske skúsenosti jasne ukazujú, že krajiny s implementovaným DCD programom dosahujú vyššiu transplantačnú aktivitu a lepšie využitie orgánov. Absencia DCD, ako demonštruje príklad Nemecka, môže viesť k obmedzeniu darcovského potenciálu.
Moderné techniky strojovej perfúzie zásadne zlepšili bezpečnosť a výsledky DCD transplantácií a stali sa kľúčovým nástrojom úspešnej implementácie programu.
Pre Slovenskú republiku, kde napriek fungujúcemu programu LT dosahuje mortalita na čakacej listine 16 %, predstavuje zavedenie DCD programu medicínsky, eticky aj systémovo odôvodnený krok smerom k zvýšeniu dostupnosti život zachraňujúcej liečby.
Poďakovanie
Za pomoc a inšpiráciu si dovoľujeme poďakovať prof. MUDr. Milošovi Adamcovi, CSc., a prof. MUDr. Jiřímu Froněkovi, Ph.D., FRCS.
ORCID autorov
S. Adamcová Selčanová 0000-0001-8181-1937,
D. Žilinčanová 0009-0004-7100-0654,
Ľ. Skladaný 0000-0001-5171-3623.
Doručené/Submitted: 9. 3. 2026
Prijaté/Accepted: 17. 3. 2026
Korespondenčná autorka
MUDr. Svetlana Adamcová Selčanová, PhD.
II. Interná klinika a HEGITO
SZU a FNsP F. D. Roosevelta Banská Bystrica
Nám. L. Svobodu 1
975 17 Banská Bystrica
sselcanova@gmail.com
Literatúra
1. Martin F, Carmona M, Mahillo B et al. Organ donation and transplantation worldwide: the global observatory on donation and transplantation 2024 report. Transplantation 2026; 110(3): e655–e669. doi: 10.1097/TP.0000000000005657.
2. Council of Europe. EDQM releases 9th edition of the guide to the quality and safety of organs for transplantation. 2025 [online]. Dostupné z: https: //www.coe.int/en/web/portal/-/edqm-releases-9th-edition-of-the-guide-to-the-quality-and-safety-of-organs-for-transplantation-1.
3. European Association for the Study of the Liver. EASL Clinical Practice Guidelines: liver transplantation. J Hepatol 2016; 64(2): 433–485. doi: 10.1016/j.jhep.2015.10.006.
4. Wijdicks EFM. The history of donation after circulatory death (DCD): backlash and boomerang. Neurocrit Care 2024. doi: 10.1007/s120 28-023-01919-7.
5. Smith M, Dominguez-Gil B, Greer DM et al. Organ donation after circulatory death: current status and future potential. Intensive Care Med 2019; 45(3): 310–321. doi: 10.1007/s00134-019-05533-0.
6. Langer RM. Donation after carc death – from then to now. Transplant Rep 2023; 8(Suppl 1): 100119. doi: 10.1016/j.tpr.2022.100119.
7. Domínguez-Gil B, Ascher N, Capron AM et al. Expanding controlled donation after the circulatory determination of death: statement from an international collaborative. Intensive Care Med 2021; 47(3): 265–281. doi: 10.1007/s00134-020-06341-7.
8. Allen E, Taylor R, Gimson A et al. Transplant benefit-based offering of deceased donor livers in the United Kingdom. J Hepatol 2024; 81(3): 471–478. doi: 10.1016/j.jhep.2024.03.020.
9. Czigany Z, Lurje I, Schmelzle M et al. Ischemia-reperfusion injury in marginal liver grafts and the role of hypothermic machine perfusion: molecular mechanisms and clinical implications. J Clin Med 2020; 9(3): 846. doi: 10.3390/jcm9030846.
10. Chouchani ET, Pell VR, Gaude E et al. Ischaemic accumulation of succinate controls reperfusion injury through mitochondrial ROS. Nature 2014; 515(7527): 431–435. doi: 10.1038/nature13909.
11. Huang W, Meng W, Zhao J et al. Sterile inflammation and cell death pathways in liver ischemia-reperfusion injury: a review and perspective. Endocr Metab Immune Disord Drug Targets 2026; 26: e18715303401342. doi: 10.2174/0118715303401342250514102731.
12. Oki R, Kerby E, Rocha I et al. The impact of normothermic machine perfusion on biliary complications in donation after circulatory death donor liver transplantation. Transplant Direct 2025; 11(7): e1821. doi: 10.1097/TXD.0000000000001821.
13. Manzi JLL, Oliveira ES, Rombach S et al. Comparisons of liver transplant from DCD outcomes in high-utilization centers versus low-utilization centers in the US: a systematic review and meta-analysis. Front Immunol 2025; 16: 1564551. doi: 10.3389/fimmu.2025.1564551.
14. Jolliffe J, Brookes J, Williams M et al. Donation after circulatory death transplantation: a systematic review and meta-analysis of outcomes and methods of donation. Ann Cardiothorac Surg 2025; 14(1): 11–27. doi: 10.21037/ acs-2024-dcd-0132.
15. van Rijn R, Endo C, Küçükerbil EH et al. Long-term follow-up after hypothermic oxygenated machine perfusion in DCD liver transplantation: results of a randomized controlled multicenter trial (DHOPE-DCD). Ann Surg 2025; 282(5): 717–724. doi: 10.1097/SLA.0000000000006876.
16. Oniscu GC, Mehew J, Butler AJ et al. Improved organ utilization and better transplant outcomes with in situ normothermic regional perfusion in controlled donation after circulatory death. Transplantation 2023; 107(2): 438–448. doi: 10.1097/TP.0000000000004280.
17. Hessheimer AJ, de la Rosa G, Gastaca M et al. Abdominal normothermic regional perfusion in controlled donation after circulatory determination of death liver transplantation: outcomes and risk factors for graft loss. Am J Transplant 2022; 22(4): 1169–1181. doi: 10.1111/ajt.16899.
18. Hill AL, Khan M, Kiani AZ et al. Global liver transplantation: emerging trends and ethical challenges. Langenbecks Arch Surg 2023; 408(1): 418. doi: 10.1007/s00423-023-03144-4.
19. Eden J, Sousa Da Silva R, Cortes-Cerisuelo M et al. Utilization of livers donated after circulatory death for transplantation – an international comparison. J Hepatol 2023; 78(5): 1007–1016. doi: 10.1016/j.jhep.2023.01.025.
20. Müller PC, Kabacam G, Vibert E et al. Current status of liver transplantation in Europe. Int J Surg 2020; 82S: 22–29. doi: 10.1016/j.ijsu.2020.05.062.
21. Danica A, Šimenc J. Donor programme after circulatory death in Slovenia: analysis of the views of professional community and future perspectives. Zdrav Vestn 2020; 89: 255–267. doi: 10.6016/ZdravVestn.2974.
22. Froněk J, Novotný R, Kucera M et al. Liver transplantation using grafts from donors after circulatory death – the first Czech Republic experience. Rozhl Chir 2020; 99(9): 391–396. doi: 10.33699/PIS.2020.99.9.391-396.
23. Cvachovec K, Černý V, Duška F et al. Doporučený postup před odběrem orgánů od zemřelých dárců po nevratné zástavě oběhu. Anest Intenziv Med 2014; 25(2): 145–146.
24. European Liver Transplant Registry (ELTR). Annual reports. 2026 [online]. Dostupné z: https: //eltr.org.
25. Eurotransplant. Annual reports. 2025 [online]. Dostupné z: https: //www.eurotransplant.org.
26. Resch T, Cardini B, Oberhuber R et al. Transplanting marginal organs in the era of modern machine perfusion and advanced organ monitoring. Front Immunol 2020; 11: 631. doi: 10.3389/fimmu.2020.00631.
27. Dutkowski P, Guarrera JV, de Jonge J et al. Evolving trends in machine perfusion for liver transplantation. Gastroenterology 2019; 156(6): 1542–1547. doi: 10.1053/j.gastro.2018.12.037.
28. Ceresa CD, Nasralla D, Pollok JM et al. Machine perfusion of the liver: applications in transplantation and beyond. Nat Rev Gastroenterol Hepatol 2022; 19(3): 199–209. doi: 10.1038/s41575-021-00557-8.
29. Mastrovangelis C, Frost C, Hort A et al. Normothermic regional perfusion in controlled donation after circulatory death liver transplantation: a systematic review and meta-analysis. Transpl Int 2024; 37: 13263. doi: 10.3389/ti.2024.13263.
30. De Goeij FH, De Meijer V, Mergental H et al. Challenges with the implementation of machine perfusion in clinical liver transplantation. Transplantation 2024; 108(6): 1296–1307. doi: 10.1097/TP.0000000000004872.
31. Bonaccorsi-Riani E, Brüggenwirth IM, Buchwald JE et al. Machine perfusion: cold versus warm, versus neither. Update on clinical trials. Semin Liver Dis 2020; 40(3): 264–281. doi: 10.1055/s-0040-1713118.
32. Longchamp A, Nakamura T, Uygun K et al. Role of machine perfusion in liver transplantation. Surg Clin North Am 2024; 104(1): 45–65. doi: 10.1016/j.suc.2023.07.001.
33. Wehrle CJ, Zhang M, Khalil M et al. Impact of back-to-base normothermic machine perfusion on complications and costs: a multicenter, real-world risk-matched analysis. Ann Surg 2024; 280(2): 300–310. doi: 10.1097/SLA.0000000000006291.