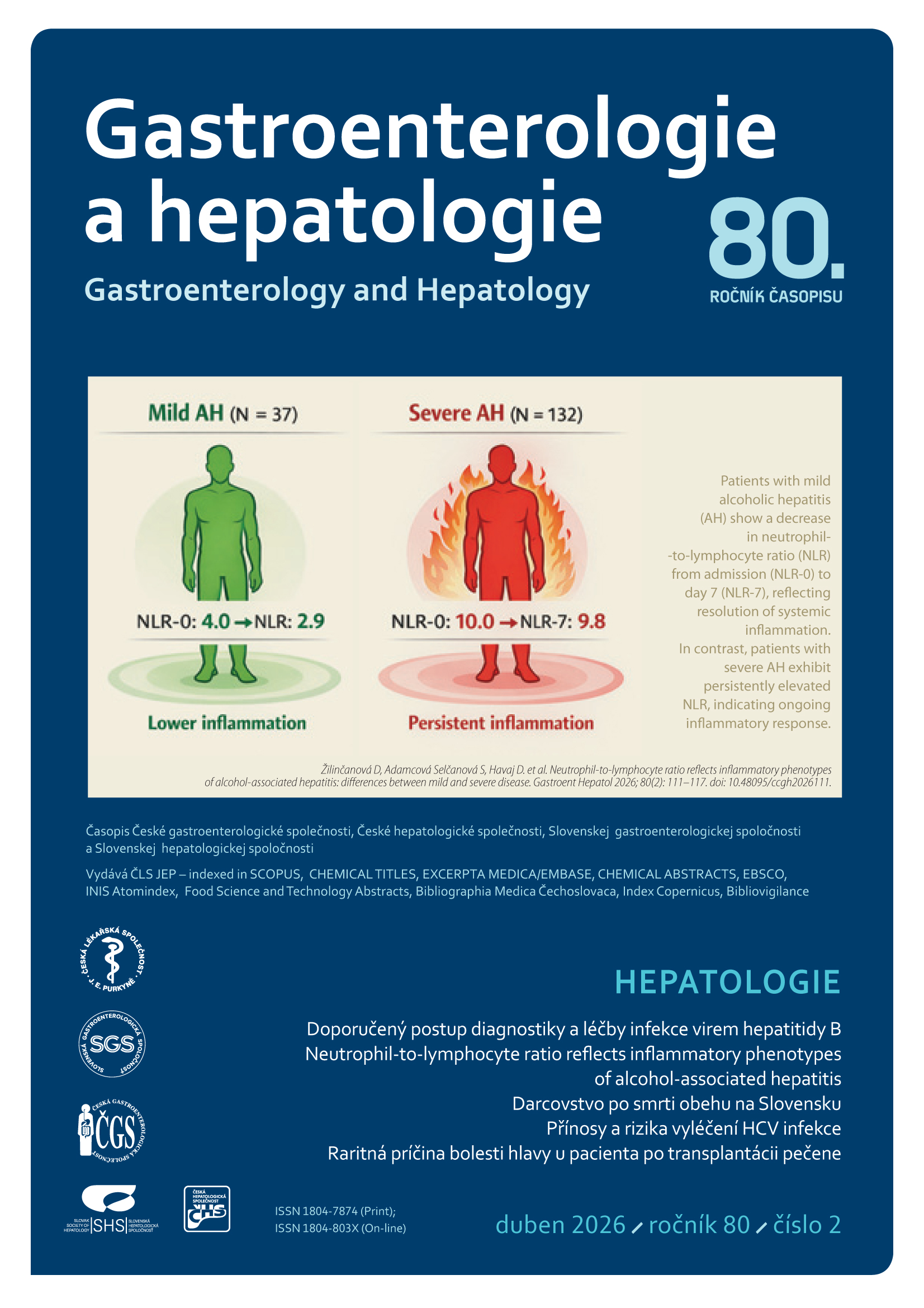
Abstrakt
Invazívne fungálne infekcie patria medzi závažné infekčné komplikácie u pacientov po transplantácii pečene s vysokou morbiditou a mortalitou. Aspergilóza je druhou najčastejšou z invazívnych mykóz a vo väčšine prípadov sa vyskytuje v diseminovanej forme s postihnutím viacerých orgánov. Izolované postihnutie CNS sa považuje za vzácnu komplikáciu. V našej kazuistike prezentujeme prípad pacienta po transplantácii pečene, u ktorého sa vo včasnom posttransplantačnom období rozvinuli bolesti hlavy, ku ktorým sa neskôr pridružili poruchy zraku. Po niekoľkých mesiacoch od začiatku symptómov prinieslo definitívnu gnózu až histologické vyšetrenie lézie lokalizovanej na klinovej kosti lebky s potvrdením infekcie vyvolanej Aspergillus spp. U pacienta bola zahájená antimykotická liečba podľa odporúčaní infektológa s následným frekventným monitorovaním hladín imunosupresív v ambulantnom sledovaní.
Úvod
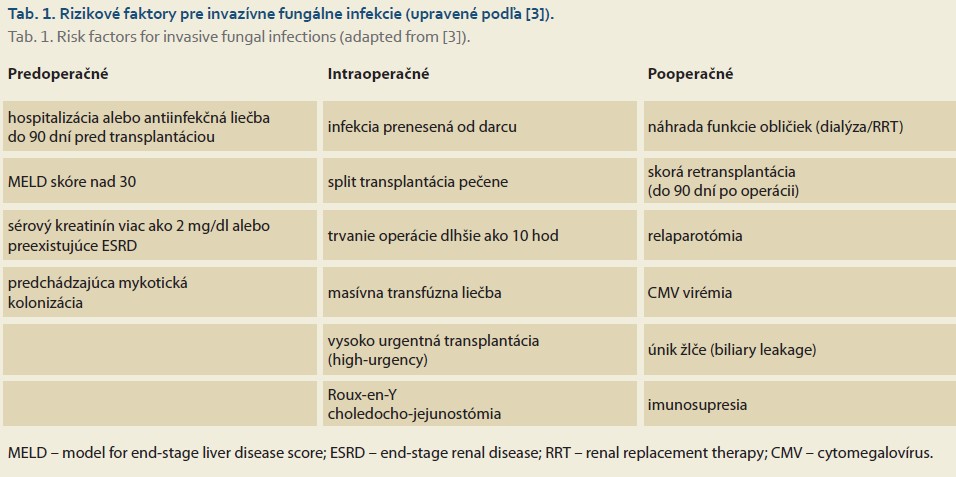
Ortotopická transplantácia pečene je život zachraňujúcim výkonom u pacientov s konečným štádiom chronického ochorenia pečene, akútnym hepatálnym zlyhaním a určitými druhmi malignít [1]. V súvislosti s imunosupresívnou liečbou sú pacienti po transplantácii vystavení viacerým komplikáciám vrátane rejekcie a infekcií. Infekcie sú najčastejšou príčinou úmrtia vo včasnom postoperačnom období [2]. Okrem bežných infekcií sú pacienti náchylní aj na oportúnne infekcie vrátane multirezistentných mikroorganizmov a invazívnych fungálnych infekcií (IFI). Incidencia IFI u pacientov po transplantácii pečene sa pohybuje od 5 do 42 % s mortalitou v rozmedzí od 25 do 80 %. Potenciálne rizikové faktory pre rozvoj IFI možno rozdeliť podľa času výskytu do troch skupín: predoperačné, intraoperačné a postoperačné [3]. Detailný prehľad rizikových faktorov ponúka tab. 1.
Kandidóza je najčastejšou invazívnou mykózou u pacientov po transplantácii solídnych orgánov najmä tenkého čreva, pankreasu a pečene, keďže Candida spp. je bežným komenzálom ľudského tráviaceho traktu. V rámci invazívnych kandidóz je najčastejším patogénom Candida albicans, no v súčasných epidemiologických trendoch sa čoraz častejšie stretávame aj s non-albicans druhmi, ako sú Candida glabrata, Candida crusei či Candida auris. Invazívna aspergilóza je druhou najčastejšou z invazívnych mykóz a jej incidencia je závislá od druhu transplantovaného orgánu, t. j. pľúca (8,6 %), pečeň (4,7 %), pankreas a obličky (4 %), srdce (3,4 %). Najčastejšie izolovaným druhom bez ohľadu na typ transplantovaného orgánu je Aspergillus fumigatus, nasledovaný menej častými Aspergillus flavus, Aspergillus niger a Aspergillus terreus. Trojicu najfrekventnejších IFI uzatvára kryptokokóza, ktorá sa vykytuje u zhruba 8 % pacientov po transplantácii solídnych orgánov. Väčšina prípadov sa týka pacientov po transplantácii obličiek, menej často po transplantácii pečene. Hlavní predstavitelia sú Cryptococcus neoformans a Cryptococcus gattii stricto sensu [4]. Invazívne mykózy predstavujú závažný problém u pacientov po transplantácii a vyžadujú si včasnú gnostiku a liečbu.
Kazuistika
V predkladanej kazuistike prezentujeme prípad pacienta, 68-ročného muža s anamnézou betes mellitus 2. typu, stavu po resekcii sigmy pre adenokarcinóm v roku 2013 – dlhodobo v remisii, s cirhózou pečene na podklade MetALD v štádiu CHP C a MELD skóre 17, ktorý absolvoval transplantáciu pečene v júli v roku 2022 v Transplantačnom centre vo Fakultnej nemocnici s poliklinikou F. D. Roosevelta v Banskej Bystrici. Výkon prebehol bez komplikácií, pacientovi bola postupne nastavená imunosupresívna liečba, zahájená realimentácia a rehabilitácia. V priebehu hospitalizácie bola na kontrolnom USG brucha verifikovaná tekutinová kolekcia v hile heparu, ktorá po doplnení CT brucha a MRCP vyšetrenia viedla k podozreniu na bilóm. Následne bola na angiografickom pracovisku realizovaná drenáž bilómu a cestou endoskopického pracoviska vykonané ERCP so zavedením DB drénu. Na komplexnej liečbe bol stav pacienta klinicky aj laboratórne zlepšený a bol prepustený do ambulantnej starostlivosti s plánovanou extrakciou DB drénu o 3 mesiace.
V decembri toho istého roku bol pacient prijatý na Neurologické oddelenie Fakultnej nemocnice J. A. Reimana v Prešove pre intenzívne bolesti hlavy, ktoré začali v období po transplantácii pečene, keď bol už pacient v ambulantnej starostlivosti. Spočiatku sa jednalo o difúzne bolesti hlavy, ktoré sa postupne premiestnili na pravú polovicu tváre. K zmierneniu bolesti došlo vždy len prechodne po analgetikách s nutnosťou opakovanej úpravy liečby až po potrebu opiátov. Počas hospitalizácie na neurologickom oddelení pacient podstúpil niekoľko vyšetrení: CT angiografia mozgu bez patológie, MR mozgu s ojedinelými léziami demyelinizácie v bielej hmote a nálezom maxillárnej a sphenoidálnej sinusitídy, USG karotíd bez hemodynamicky závažných stenóz, EEG v norme, gnostická lumbálna punkcia bez patologického nálezu. Stav pacienta bol uzavretý ako pravostranná hemikránia charakteru cluster headache. Počas hospitalizácie bola zahájená infúzna analgetická liečba a kortikosteroidy s postupnou detrakciou a zmiernením pacientových ťažkostí s následným prepustením do ambulantnej starostlivosti.
Vo februári roku 2023 bol pacient opätovne hospitalizovaný tentokrát na Oddelení oftalmológie FN J. A. Reimana v Prešove z dôvodu náhle vzniknutej amaurózy na pravom oku. V úvode hospitalizácie bolo doplnené nové MR mozgu s nálezom ojedinelých hypersignálnych lézií bielej hmoty mozgu obojstranne prevažne v paraventrikulárnej a subkortikálnej lokalizácii. Stav bol hodnotený ako suspektná posteriórna ischemická optická neuropatia. Bola zahájená pulzná liečba kortikosteroidmi a vazodilatačná liečba s čiastočným zlepšením vízu na pravom oku a následným demitom pacienta.
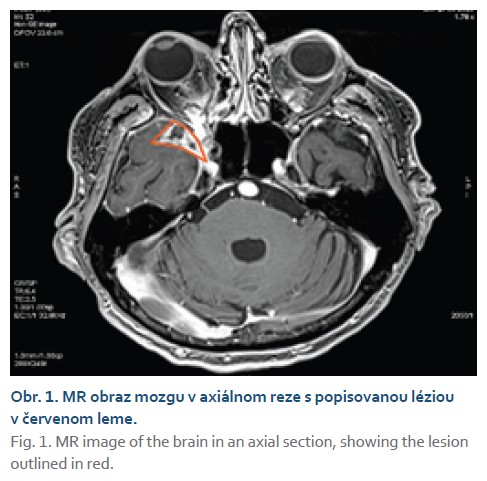
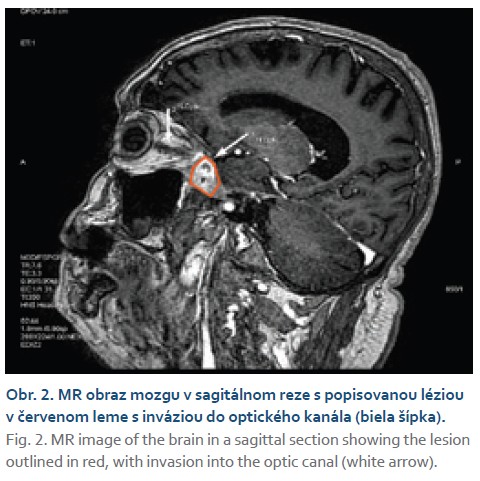
V marci roku 2023 bol pacient odoslaný na Hepatologicko-gastroenterologické a transplantačné oddelenie (HEGITO) vo FNsP F. D. Roosevelta v Banskej Bystrici za účelom doriešenia stavu. U pacienta naďalej pretrvávali bolesti hlavy skôr epizodického charakteru najmä v noci a pár dní pred hospitalizáciou došlo u pacienta opätovne k strate vízu na pravom oku. V úvode hospitalizácie sme u pacienta v akútnom režime doplnili kontrastné CT mozgu, kde bola popisovaná sýtiaca sa lézia o veľkosti 20 × 13 mm lokalizovaná na alla major ossis sphenoidalis l.dx s pokračovaním do orbity do canalis opticus l.dx, kde čiastočne zavzala dorzálnu 1/4 nervus opticus. Následne ešte doplnené MR mozgu potvrdilo uvedenú léziu so zavzatým nervus opticus a čiastočne aj musculus rectus orbit melis. Na základe zobrazovacích metód sa rádiológovia prikláňali k gnóze suspektného tumoru vs. meningeómu, menej pravdepodobná bola možnosť abscesového ložiska (obr. 1, 2).
V rýchlom slede sme počas hospitalizácie zrealizovali oftalmologické konzílium, ktoré potvrdilo amaurózu na pravom oku a edém papily terča zrakového nervu. Konzultovaný neurológ odporučil zahájiť antiedémovú a analgetickú liečbu, doplniť neurochirurgické konzílium.Vzhľadom na nevylúčenú možnosť infekcie sme súbežne empiricky zahájili aj antibiotickú a antimykotickú liečbu (amfotericín B). ORL konzílium vylúčilo prítomnosť fokusu v prínosových dutinách. Kompletné serologické vyšetrenie vrátane vyšetrenia galaktomananu bolo u pacienta negatívne. Po dohovore s neurochirugom sme doplnili ešte MR spektroskopiu, ktorá vyslovila podozrenie na abscesové ložisko s postihnutím leptomeningov. Vzhľadom na daný nález bol pacient indikovaný na odber histologickej vzorky z popisovaného ložiska na Neurochirugickom oddelení. Po obdržaní histologického výsledku sme stav definitívne uzatvorili ako mykotickú infekciu mozgu spôsobenú Aspergillus spp. (obr. 3).
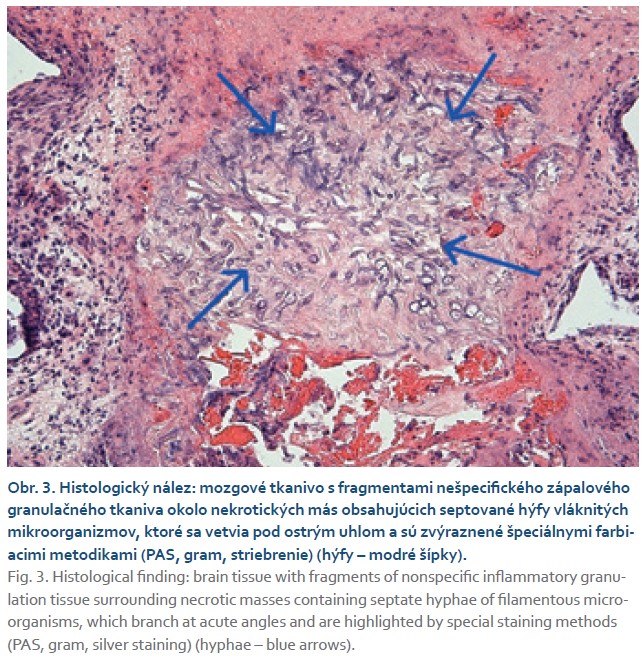
Po konzultácii s infektológom sme zmenili antimykotickú liečbu na Vorikonazol. V priebehu hospitalizácie neboli u pacienta prítomné laboratórne ani morfologické zmeny graftu. Pokračovali sme v imunosupresívnej liečbe v zmysle ponechania Prografu za prísnej kontroly jeho hladín, Myfenax sme prechodne vysadili z liečby, kortikosteroidy boli postupne detrahované. Pacienta sme demitovali do ambulantnej starostlivosti s potrebou dlhodobej antimykotickej liečby a pravidelných kontrol na neurochirurgickej ambulancii.
Diskusia
Invazívna aspergilóza (IA) patrí medzi najčastejšie invazívne fungálne infekcie u pacientov po transplantácii solídnych orgánov (SOT) a je významnou príčinou posttransplantačnej morbidity a mortality [5]. Incidencia a mortalita IA u pacientov po transplantácii pečene (LT) sa za posledné dekády znížila, z 10 na 1,8 % a zo 100 na 50 %, aj keď mortalita po transplantácii ostatných orgánov zostáva stále vysoká. Rizikové faktory, ktoré môžu predisponovať k vzniku IA, sú zhodné s faktormi pre invazívne mykózy všeobecne [6]. Keď sa pozrieme na nášho pacienta, môžeme spoľahlivo identifikovať dva rizikové faktory, a to zo skupiny faktorov asociovaných s pooperačnou starostlivosťou v zmysle prítomného bilómu vo včasnom postransplantačnom období a imunosupresívnu liečbu.
Invazívna aspergilóza sa objavuje vo väčšine prípadov vo včasnom posttransplantačnom období (do 3 mesiacov) v porovnaní s ostatnými orgánmi s výnimkou srdca. Zároveň sa IA u LT recipientov častejšie vyskytuje v diseminovanej forme (cca 50 % prípadov) v porovnaní s ostatnými druhmi SOT. Diseminovaná invazívna aspergilóza môže postihovať pľúca, mozog, obličky, pečeň či kožu (obr. 4) [6].
Izolované postihnutie CNS sa považuje za vzácnu komplikáciu a doteraz bolo publikovaných len niekoľko kazuistík. Príčinou jej vzniku môže byť buď priama invázia do CNS alebo hematogénne rozšírenie [7]. Klinická prezentácia CNS infekcie Aspergillus spp. je variabilná a môže zahŕňať abscesy mozgu, meningitídu, cerebritídu, ventrikulitídu či trombózu kraniálnych sinusov. Pacienti tak môžu vykazovať široké spektrum symptómov ako horúčka, bolesti hlavy, závraty, letargia, alterácia mentálneho stavu, abnormálna chôdza či kŕče [8]. U nášho pacienta bol od začiatku dominujúci symptóm bolesť hlavy, ku ktorej sa neskôr pridružili závažné poruchy vízu. Treba však povedať, že bolesti hlavy sú pomerne časté u pacientov po transplantácii a súvisia väčšinou s užívaním imunosupresie, to sa týka najmä kalcineurínových inhibítorov (takrolimus, cyklosporín). Incidencia bolestí hlavy súvisiaca s užívaním takrolimu sa udáva okolo 32 % a súvisí spravidla s vysokými hladinami lieku. V prípade pretrvávania bolestí hlavy však treba pátrať ďalej a vylúčiť aj ďalšie príčiny, ako sú novovzniknutá hypertenzia, infekcie či malignity [9].
Diagnostika aspergilózy mozgu sa opiera najmä o zobrazovacie vyšetrenia, ako sú kontrastné CT a MR mozgu a histologický či kultivačný dôkaz Aspergillus spp. vo vyšetrovanom tkanive/biologickom materiáli [8]. Konvenčné testy vyšetrovania likvoru sú pomerne málo senzitívne čo sa týka gnostiky aspergilózy CNS. Technika sekvenovania novej generácie (tzv. NGS) sa však ukazuje podľa viacerých štúdií ako nádejná metóda pre identifikovanie patogénov postihujúcich CNS vrátane aspergilózy [10]. Sérologické vyšetrenie galaktomananu poskytuje tiež iba priemerné výsledky. Senzitivita a špecificita pre gnostiku invazívnej aspergilózy je 61 % a 93 % podľa údajov z metaanalýz [11]. Zároveň sa ukazuje, že vyšetrenie galaktomananu je užitočnejšie u pacientov po transplantácii krvotvorných kmeňových buniek v porovnaní s pacientmi po transplantácii solídnych orgánov [12]. Aj v našej kazuistike bolo základné vyšetrenie likvoru a galaktomananu zo séra nepriekazné a definitívnu gnózu priniesla až histologizácia ložiska.
Antimykotická liečba triazolmi predovšetkým Vorikonazolom sa považuje za prvolíniovú liečbu aspergilózy vzhľadom na viacerými štúmi dokázanú schopnosť znížiť celkovú mortalitu u týchto pacientov v porovnaní s ostatnými antimykotikami ako napr. amfotericínom B [8]. Jeho dominanciu podčiarkuje aj výborná penetrácia do CNS, efektivita a dobrá tolerancia [6]. Antimykotiká však nesú určité riziká obzvlášť u transplantovaných pacientov, ktoré treba mať na pamäti. Najčastejšie nežiadúce účinky pri terapii vorikonazolom zahŕňajú:
- eleváciu hepatálnych enzýmov (vo väčšine prípadov sa jedná o asymptomatickú alteráciu hepatálnych testov; je však nevyhnutné sledovať hepatálne parametre jednak pred zahájením liečby Vorikonazolom a potom frekventne v priebehu prvých dvoch týždňov od zahájenia liečby a ďalej každé 2 až 4 týždne);
- poruchy zraku (rozmazané videnie, šeroslepota, zníženie zrakovej ostrosti atď.);
- kožné vyrážky;
- kardiovaskulárne nežiadúce účinky (predĺženie QT intervalu);
- krvná toxicita (anémia, leuko/trombocytopénia) [13].
Pre antimykotiká sú typické aj početné liekové interakcie najmä s imunosupresívami. Triazoly pôsobia ako inhibítory cytochromu P450 v dôsledku čoho môžu zvyšovať hladiny užívaných imunosupresív. Je preto odporúčané, aby sa dávka inhibítorov kalcineurínu (takrolimus) znížila na začiatku liečby Vorikonazolom o 50–60 % pôvodnej dávky s následným pravidelným monitorovaním jeho hladín. Užívanie sirolimu je pri liečbe Vorikonazolom kontraindikované. Kyselina mykofenolová a kortikosteroidy nevyžadujú úpravu dávkovania pri súbežnej liečbe Vorikonazolom [14].
Využitie antimykotík v primárnej prevencii infekcií spôsobených invazívnymi mykózami u pacientov v súvislosti s transplantáciou solídnych orgánov je stále kontroverznou témou. Podľa doterajších odporúčaní prichádza do úvahy antifungálna profylaxia pred transplantáciou pečene u vysoko-rizikových pacientov, a to sú pacienti podstupujúci re-transplantáciu alebo opakovaný chirurgický zákrok v brušnej dutine po transplantácii pečene. Optimálne trvanie antifungálnej profylaxie však nie je jednoznačne stanovené. Vyvstáva tak potreba ďalších randomizovaných kontrolovaných štúdií, ktoré by sa zaoberali vplyvom antimykotik na redukciu výskytu invazívnych mykóz [6].
Záver
Invazívna aspergilóza je vzácna, ale často fatálna komplikácia u pacientov po transplantácii pečene. Dôležitá je preto jej včasná gnostika a okamžitá liečba. Vorikonazol je liekom voľby, no počas jeho užívania sa vyžaduje prísny monitoring hladín imunosupresív s cieľom vyhnúť sa ich predávkovaniu. Našou kazuistikou sa snažíme poukázať aj na potrebu skorej konzultácie transplantačného centra u každého pacienta po transplantácii pečene, pretože aj za tak častým symptómom, ako je bolesť hlavy, sa môže skrývať raritná príčina.
ORCID autorov
N. Kubánek 0000-0001-9905-7741
S. Adamcová Selčanová 0000-0001-8181-1937
D. Žilinčanová 0009-0004-7100-0654
K. K. Šulejová 0009-0005-4149-3694
D. J. Havaj 0000-0001-5979-8326
T. Koller 0000-0001-7418-0073
Ľ. Skladaný 0000-0001-5171-3623
Doručené/Submitted: 18. 3. 2026
Prijaté/Accepted: 24. 3. 2026
Korešpondenčná autorka
MUDr. Natália Kubánek
II. Interná klinika a HEGITO
SZU a FNsP F.D.Roosevelta Banská Bystrica
Nám. L. Svobodu 1
975 17 Banská Bystrica
natalia.bystrianska21@gmail.com
Literatúra
1. Adam R, Karam V, Delvart V et al. Evolution of indications and results of liver transplantation in Europe. A report from the European Liver Transplant Registry (ELTR). J Hepatol 2012; 57(3): 675–688. doi: 10.1016/j.jhep.2012.04.015.
2. Agostini C, Buccianti S, Risaliti M et al. Complications in post-liver transplant patients. J Clin Med 2023; 12(19): 6173. doi: 10.3390/jcm12196173.
3. Senoner T, Breitkopf R, Treml B et al. Invasive fungal infections after liver transplantation. J Clin Med 2023; 12(9): 3238. doi: 10.3390/jcm12093238.
4. Mahmoud DE, Hérivaux A, Morio F et al. The epidemiology of invasive fungal infections in transplant recipients. Biomed J 2024; 47(3): 100719. doi: 10.1016/j.bj.2024.100719.
5. Farahani A, Ghiasvand F, Davoudi S et al. Invasive aspergillosis in liver transplant recipients, an infectious complication with low incidence but significant mortality. World J Transplant 2023; 13(5): 264–275. doi: 10.5500/wjt.v13.i5.264.
6. Melenotte C, Aimanianda V, Slavin M et al. Invasive aspergillosis in liver transplant recipients. Transpl Infect Dis 2023; 25(3): e14049. doi: 10.1111/tid.14049.
7. Abbasi M, Ardakani SS, Fakhar N et al. Catastrophic brain aspergillosis after liver transplantation. Case Rep Transplant 2021; 2021: 8626057. doi: 10.1155/2021/8626057.
8. Khodashahi R, Akhavan Rezayat K, Abdollahzade A et al. CNS fungal infections in liver transplantation. Arch Clin Infect Dis 2024; 19(1): e138411. doi: 10.5812/archcid-138411.
9. Montenovo MI, Jalikis FG, Hoch B et al. A symptomatic de novo pheochromocytoma 23 years after liver transplantation: a case report and review of the literature. Case Rep Transplant 2014; 2014: 934385. doi: 10.1155/2014/934385.
10. Chen F, Zhao Y, Shen C et al. Next generation sequencing for gnosis of central nervous system aspergillosis in liver transplant recipients. Ann Transl Med 2021; 9(13): 1071. doi: 10.21037/atm-21-92.
11. Leung V, Stefanovic A, Sheppard D. Severe cerebral aspergillosis after liver transplant. Transpl Infect Dis 2010; 12(1): 51–53. doi: 10.1111/j.1399-3062.2009.00461.x.
12. Pfeiffer CD, Fine JP, Safdar N. Diagnosis of invasive aspergillosis using a galactomannan assay: a meta-analysis. Clin Infect Dis 2006; 42(10): 1417–1427. doi: 10.1086/503427.
13. Eiden C, Peyrière H, Cociglio M et al. Adverse effects of voriconazole: analysis of the French Pharmacovigilance Database. Ann Pharmacother 2007; 41(5): 755–763. doi: 10.1345/aph.1H671.
14. Barchiesi F, Mazzocato S, Mazzanti S et al. Invasive aspergillosis in liver transplant recipients: epidemiology, clinical characteristics, treatment, and outcomes in 116 cases. Liver Transpl 2015; 21(2): 204–212. doi: 10.1002/lt.24032.
15. Gemini. Prompt: Pacient po transplantácii pečene s invazívnou aspergilózou a postihnutím orgánov: pečeň, mozog, obličky, pľúca a koža. 2026 [online]. Dostupné z: https: //gemini.google.com.