Abstrakt
Chronická infekce virem hepatitidy C (HCV) zůstává celosvětově významnou příčinou nemocnosti a úmrtnosti související s onemocněním jater. Přirozený průběh infekce HCV je velmi variabilní, od bezpříznakového onemocnění až po významnou fibrózu, cirhózu a hepatocelulární karcinom (HCC). Objev přímo působících antivirotik (DAA) znamenal revoluci v léčbě HCV, s dosažením setrvalé virologické odpovědi (SVR) přesahující 95 % ve všech stadiích onemocnění jater. Eradikace viru je spojena se snížením zánětu jater, regresí fibrózy a snížením portální hypertenze. Důležité je, že SVR významně snižuje riziko jaterní dekompenzace, HCC a úmrtnosti související s jaterním onemocněním. Riziko HCC však není zcela vyloučeno, zejména u pacientů s pokročilou fibrózou nebo cirhózou, a je tedy doporučena surveillance HCC. Léčba DAA také umožnila léčbu pacientů s dekompenzovanou cirhózou, což vedlo ke zlepšení jaterních funkcí a ve vybraných případech též k vyřazení pacienta z čekací listiny k transplantaci jater. Odpověď na léčbu a klinický průběh však závisí na výchozí funkci jater, přičemž u pacientů s pokročilým onemocněním (MELD skóre ≥ 20) je šance na dosažení SVR nižší, s vyšším rizikem nežádoucích účinků. I přes dosažení SVR mohou mít na další průběh onemocnění a riziko vzniku HCC negativní vliv metabolické rizikové faktory, včetně obezity, betu a steatózy jater. Nárůst hmotnosti po dosažení SVR může být významný a ovlivněn genetickými faktory hostitele, jako jsou varianty genu PNPLA3.
Úvod
Chronická hepatitida C (HCV) patří mezi hlavní příčiny chronického onemocnění jater ve vyspělých zemích světa. Podle nejnovějších celosvětových dat je prevalence HCV RNA pozitivity přibližně 0,7 %, což představuje asi 56,8 milionu infikovaných osob na celém světě [1]. HCV infekce i dnes patří mezi onemocnění, která zvyšují jaterní morbiditu a mortalitu [2].
Infekce HCV může mít velmi různorodý klinický průběh od asymptomatické formy až po chronickou hepatitidu s fibrózou, která může vyústit v jaterní cirhózu a její komplikace, včetně chronického selhání jater a hepatocelulárního karcinomu (HCC) [3].
Hlavním cílem léčby je eradikace viru z organizmu. Úspěšná eliminace viru předchází poškození jater, zpomaluje nebo zcela zastavuje progresi fibrózy, předchází vzniku cirhózy a pozdních komplikací terminálního poškození jater (dekompenzace cirhózy a vznik HCC). Trvalá eradikace viru, označovaná jako setrvalá virologická odpověď (SVR12 nebo SVR24), znamená nepřítomnost HCV RNA v krvi 12 či 24 týdnů po ukončení léčby [4]. Dosažení SVR odpovídá vyléčení infekce HCV, jelikož k pozdnímu relapsu dochází v méně než 0,2 % případů po 6 měsících sledování [5]. Trvalá eradikace viru je asociována s ústupem zánětlivých změn a zlepšením jaterní fibrózy [4,6]. Navzdory možnosti léčit pomocí přímo působících antivirotik (DAA), která mají vysokou účinnost (více než 95 %) bez ohledu na stadium jaterního onemocnění, se odhaduje, že léčbu pomocí DAA zahájí pouze 13–21 % diagnostikovaných pacientů [4].
Epidemiologie
Hepatitida C (HCV) je celosvětově rozšířenou infekcí, která s prevalencí přibližně 0,7 % v běžné populaci nadále patří mezi hlavní příčiny onemocnění jater v rozvinutých zemích [4]. Podle sérologického průzkumu z roku 2001 byla v České republice zjištěna prevalence 0,2 % [7]. Novější data ze séroprevalenční studie z roku 2015 ukazují 1,67% výskyt anti-HCV protilátek, přičemž 0,93 % osob mělo současně pozitivní HCV RNA, což svědčí o aktivní virové replikaci [8]. Do roku 2007 dominoval v České republice genotyp 1b [9], zatímco aktuální rozložení genotypů je následující: 25 % genotyp 1a, 25 % genotyp 1b a 46,4 % genotyp 3 [8].
Přenos HCV
Hlavním způsobem přenosu HCV je kontakt s infikovanou krví, dále přenos z matky na dítě a infekce pohlavním stykem. Historicky bylo nejdůležitější podání krevní transfuze a krevních derivátů (zejména před rokem 1992), v dnešní době stojí na prvním místě nitrožilní užívání drog a sdílení injekčního instrumentária [10,11].
Průběh onemocnění
Infekce virem HCV je jen zřídka diagnostikována během akutní fáze. Klinické projevy se mohou objevit obvykle během 7–8 týdnů po expozici HCV RNA, u většiny pacientů akutní fáze proběhne zcela bez příznaků. Dostupná data poukazují na fakt, že 50–85 % infikovaných není schopno virus v akutní fázi spontánně eliminovat. Onemocnění poté přechází do chronického sta definovaného arbitrárně jako infekce, která trvá déle než 6 měsíců [4,12].
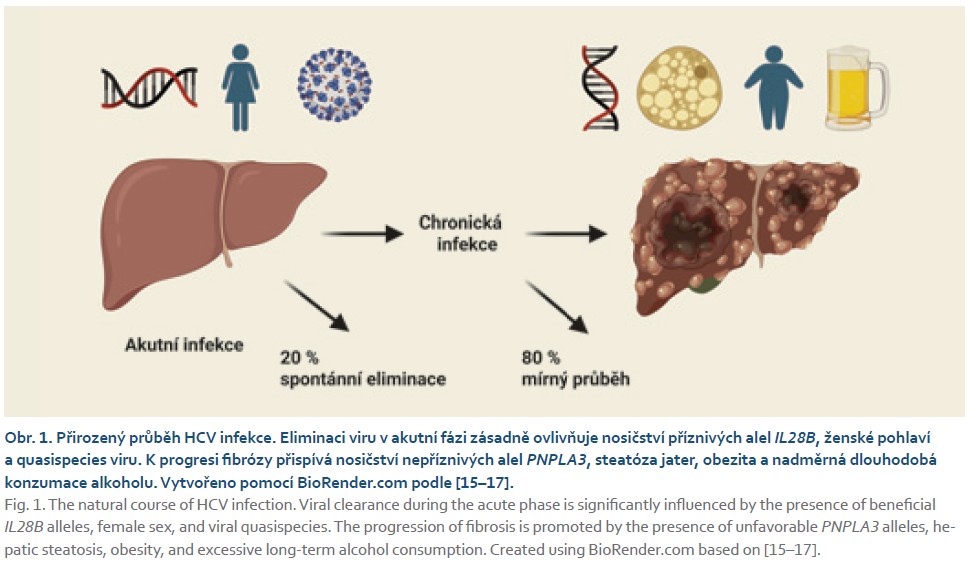
Průběh HCV infekce bývá roky zpravidla mírný a jeho progrese v čase je pomalá [12]. Přesto epidemiologické studie poukazují na fakt, že infekce je spojená s významnou úmrtností [3]. U 15–30 % pacientů dochází k rozvoji jaterní cirhózy během 10–20 let trvání infekce, navíc po 20–30 letech 1,8–8,3 % pacientů vyvine HCC [13]. U imunokompetentních osob bývá onemocnění po dobu přibližně dvou desetiletí většinou málo aktivní. Nejvyšší výskyt cirhózy je zaznamenán po cca 25 letech trvání infekce, kdy cirhózu rozvine přibližně 35 % nakažených. Naopak u pacientů, kteří mají v průběhu infekce dlouhodobě normální aktivity jaterních enzymů, nebyl výskyt cirhózy popsán [3,13]. Progresi fibrózy naopak nepříznivě ovlivňuje dlouhodobý abúzus alkoholu, steatóza jater, obezita a nosičství nepříznivých variant genu PNPLA3 (obr. 1) [14–16].
Přínosy vyléčení HCV a reziduální riziko onemocnění po dosažení SVR
Hlavním cílem léčby HCV infekce je předejít progresi fibrózy jater a zejména pozdním komplikacím onemocnění, jako jsou jaterní cirhóza a HCC. Dalším cílem je prevence přenosu na ostatní zdravé osoby, zejména ve skupinách s vysokou prevalencí infekce, jako jsou nitrožilní uživatelé drog (PWID), muži mající sex s muži, osoby vězněné, pacienti dialyzovaní či pracovníci ve zdravotnictví provádějící invazivní vyšetření [4].
Analýza nákladové efektivity srovnávající strategii léčby pro všechny se strategií léčby podle stupně fibrózy prokázala, že léčba dle stupně fibrózy nákladově efektivní není, léčba DAA má být poskytnuta všem pacientům bez ohledu na pokročilost onemocnění [18].
Snížení stupně fibrózy a stupně portální hypertenze
Eradikace viru snižuje riziko dekompenzace cirhózy a úmrtí na onemocnění jater. Studie z doby léčby IFNα dokazují, že i cirhóza může regredovat u významné části pacientů v okamžiku, kdy dosáhnou SVR. D‘Ambrosio et al. prokázali v roce 2012 regresi fibrózy F4 v jaterní biopsii na nižší stupně fibrózy po úspěšné protivirové léčbě ve více než 60 % případů, medián sledování byl 5 let [19]. Regrese fibrózy byla prokázána i v případě neinvazivního hodnocení fibrózy při léčbě DAA: studie Bachofnera et al. prokázala brzký pokles tuhosti jater měřené pomocí vibracemi kontrolované tranzientní elastografie, současně byl patrný i pokles sérových markerů fibrózy (APRI a FIB-4 skóre) [20]. Španělská studie provedená na souboru více než 500 pacientů léčených DAA potvrdila rychlý pokles tuhosti jater po úspěšné léčbě: po roce došlo k 30% poklesu tuhosti jater [21].
Úspěšná protivirová léčba má rovněž vliv na stupeň portální hypertenze. První studie analyzující HVPG (hepatic venous pressure gradient) po léčbě DAA byla publikována Mandorferem et al. v roce 2016: dosažení SVR zlepší HVPG, u pacientů s HVPG ≥ 16 mmHg je však pokles vyjádřen méně [22]. Stejná skupina autorů zkoumala později HVPG po dosažení SVR u pacientů s klinicky významnou portální hypertenzí před léčbou. Snížení HVPG po léčbě o ≥ 10 % bylo spojeno s významně nižším rizikem dekompenzace jaterní cirhózy [23].
U pacientů s HCV a cirhózou je riziko dekompenzace onemocnění úměrné stupni portální hypertenze. Snížení rizika dekompenzace bylo jasně prokázáno po dosažení SVR ve studiích s režimy založenými na IFNα u pacientů sledovaných déle než 5 let [24]. Léčba DAA umožní v současné době i léčbu pacientů, kteří by v minulosti léčeni být nemohli, zejména z důvodu předpokládaných hematologických nežádoucích účinků, nejčastěji trombocytopenie. Vzhledem ke stále krátké době od zavedení DAA do klinické praxe je významných studií, které by demonstrovaly výstupy léčby u pacientů s cirhózou, jen několik. Francouzská studie nepotvrdila nižší riziko dekompenzace u pacientů léčených DAA a sledovaných dlouhodobě s mediánem 33,4 měsíců [25]. Naopak studie Mendizabalova zahrnující celkem 1 760 pacientů s cirhózou prokázala nižší riziko dekompenzace po léčbě DAA při sledování v horizontu 26,2 měsíce [26].
Snížení rizika HCC a mortality
Aktivní replikace viru představuje nejvýznamnější riziko vzniku HCC. Proto dosažení SVR snižuje riziko HCC nejúčinněji, nezávisle na dosažení SVR léčbou IFNα, IFNα + DAA, nebo pouze DAA. Dosažení SVR snižuje riziko HCC o 71 %, což bylo prokázáno ve studii čítající 62 000 jedinců [27]. Výsledky dříve popsané studie byly potvrzeny i u pacientů léčených výhradně DAA. Žádná ze studií nepotvrdila naprostou minimalizaci rizika HCC, incidence HCC zůstává stabilní mezi 1,5 a 2,3 případy na 100 pacientských let u jedinců s cirhózou a neklesá ani 3,6 roku po dosažení SVR [28].
Riziko vzniku HCC i po úspěšné léčbě je způsobeno několika mechanizmy: regrese pokročilé fibrózy a cirhózy je dlouhodobý proces, během něhož riziko HCC přetrvává. U některých pacientů s cirhózou již proces remodelace není možný, u dalších osob může k progresi fibrózy dojít i z jiných důvodů (nadměrná konzumace alkoholu, společně přítomná nealkoholická steatohepatitida). Dalším faktorem jsou preneoplastické genetické a epigetenické změny, které vzniknou ještě před dosažením SVR a přetrvávají doživotně [29].
Protože eradikace HCV infekce riziko HCC sníží, ale neeliminuje zcela, je riziko u pacientů s těžkou fibrózou (F3 dle METAVIR skóre) a cirhózou (F4) natolik vysoké, že doporučení pokračovat v surveillance HCC i po dosažení SVR je jednoznačné [4,30]. Přesto může být v současnosti protivirová léčba HCV považována za jednu z nejúčinnějších forem chemoprevence tohoto maligního onemocnění.
Důležitým přínosem úspěšné léčby je snížení mortality, které je zřejmé u pacientů s cirhózou léčených DAA. Ve francouzské skupině 3 045 pacientů s cirhózou byl zaznamenán pokles mortality z jakékoli příčiny i z důvodu jaterního onemocnění [25].
Zlepšení syntetické jaterní funkce: „rekompenzace“ a možnost vyřazení z čekací listiny k transplantaci jater
Dosáhnout SVR interferonovými režimy bylo téměř nemožné u pacientů s dekompenzovanou jaterní cirhózou, nyní je možnost léčit i tyto nemocné pomocí DAA. Léčbou může dojít ke zlepšení jaterní funkce. U 50 % pacientů dojde ke zlepšení při léčbě kombinací sofosbuviru a velpatasviru při hodnocení MELD skóre (model for end-stage liver disease) 12 týdnů po léčbě ve srovnání s MELD před zahájením terapie [31]. Ke stejným výsledkům dospěli i Foster et al. v retrospektivní studii hodnotící 409 pacientů: léčba DAA vedla ke snížení MELD skóre v průběhu 6 měsíců. Nižší šance na zlepšení měli pacienti, kteří měli před léčbou sérovou koncentraci albuminu < 35 g/l, Na < 135 mmol/l a byli starší 65 let [32].
U pacientů s dekompenzovanou jaterní cirhózou představují DAA ideální způsob léčby: léčba je krátká, nemá nežádoucí účinky a šance na předčasné ukončení terapie je proto velice nízká [33]. Naopak šance na dosažení SVR je vysoká, nicméně stále nižší než u pacientů s kompenzovaným onemocněním, a riziko nežádoucích účinků, které můžeme léčbě přisuzovat, stoupá s pokročilostí jaterního onemocnění [34].
U pacientů léčených kombinací sofosbuviru a ledipasviru v reálné klinické praxi počty SVR závisely na přítomnosti cirhózy (94 %), anamnéze dekompenzace (90 %) a užívání inhibitorů protonové pumpy (94 %) [34].
Léčba u pacienta s dekompenzovanou jaterní cirhózou před transplantací jater (LTx) má za cíl zlepšení jaterní funkce a prevenci rekurence HCV v jaterním štěpu [35]. U pacientů zařazených do čekací listiny může zlepšení jaterní funkce vést až k vyřazení z čekací listiny, eliminace viru vede k zásadnímu zlepšení hodnot bilirubinu, albuminu a protrombinového času až u jedné třetiny nemocných [36]. Pacienti s funkční klasifikací Child-Pugh B profitují lépe z vyléčení infekce ve smyslu přežití bez nežádoucích příhod 15 měsíců po léčbě ve srovnání s cirhotiky skupiny funkční klasifikace Child-Pugh C [32].
Vyřazení pacienta z čekací listiny při zlepšení funkce jater je zásadní zejména v západních zemích, v situaci nedostatku orgánů vhodných k transplantaci. U pacientů, kteří jsou z čekací listiny vyřazeni pro zlepšení jaterní funkce, musíme i po úspěšné léčbě nadále monitorovat jaterní funkce a provádět screening HCC [4,30].
Dosažení SVR u pacientů v čekací listině k LTx zabrání rekurenci HCV v jaterním štěpu [37]. V dnešní době lze použít libovolnou kombinaci DAA, pouze s ohledem na syntetickou jaterní funkci. Léčebný režim, který obsahuje inhibitor proteázy, je kontraindikován u nemocných funkční klasifikace Child-Pugh B a C. Riziko nežádoucích účinků vyplývá z vysokých koncentrací léků v krvi při jaterní dysfunkci [4]. Účinnost léčby u pacientů s dekompenzovanou cirhózou je nižší ve srovnání s cirhotiky kompenzovanými. U pacientů s MELD skóre ≥ 15 je signifikantně vyšší riziko dekompenzace a rovněž zvýšené riziko nežádoucích účinků spojených s léčbou [32]. Nejvyšší šanci na zlepšení jaterní funkce a vyřazení z čekací listiny po úspěšné protivirové léčbě mají pacienti, kteří mají před léčbou MELD skóre < 16 bodů a dosáhnou poklesu MELD o více než 4 body při ukončení terapie. Naopak u pacientů s MELD skóre ≥ 20 je šance na zlepšení jaterní funkce velice malá [33]. Pacienti dosahující hodnoty MELD skóre ≥ 20 mají být proto léčeni až po LTx, stejně tak jedinci s refrakterními komplikacemi portální hypertenze (ascites, encefalopatie) [4].
Nárůst hmotnosti po úspěšné léčbě
Pacienti úspěšně vyléčení mohou mít i po dosažení SVR vyšší aktivitu jaterních enzymů. Mezi 834 pacienty, kteří dosáhli SVR, mělo trvale vyšší hodnotu ALT 10 % pacientů [38], vyšší hodnota ALT korelovala s výší BMI. Vyšší hodnoty ALT měli rovněž jedinci s diabetem a excesivní konzumací alkoholu [39]. Pacienti s vyšším BMI mají po dosažení SVR vyšší riziko jaterní cirhózy [40].
Recentní studie dokládají nárůst hmotnost po dosažení SVR. V německé studii zahrnující 284 pacientů léčených DAA přibralo 44 % pacientů na hmotnosti, v průměru o 1,45 kg za rok po ukončení léčby. Faktor, který tloustnutí predikoval, byl věk pod 60 let, nikoli však pohlaví, anamnéza betu, cirhózy nebo výše BMI před léčbou [41]. Tyto výsledky byly potvrzeny dalšími studiemi: výsledky prospektivní studie s 11 469 americkými veterány dokládají nárůst hmotnosti u 52,6 % pacientů: 19,8 % z nich přibralo významně, což bylo definováno jako zvýšení hmotnosti ≥ 9 kg 2 roky po léčbě [42]. V této studii byly nezávislými prediktory nárůstu hmotnosti dosažení SVR, mladší věk (< 65 let), cirhóza, FIB-4 skóre > 3,25 a nadváha před léčbou. Naopak abstinence od alkoholu byla faktorem protektivním. Ze studie autoři vyvozují, že nejpravděpodobnějšími mechanizmy způsobujícími nárůst hmotnosti jsou neuropsychiatrické změny a snížení koncentrace cirkulujících prozánětlivých cytokinů. Chronické onemocnění jater je často provázeno ztrátou chuti k jídlu a změnami chuti, proto může úspěšná léčba vést k vymizení těchto příznaků a následnému zvýšení hmotnosti.
Studie provedená na 230 pacientech, kteří dosáhli SVR a byli sledováni další 3 roky po léčbě HCV pomocí DAA, taktéž zaznamenala vzestup BMI, konkrétně o 0,39 kg/m2 po 3 letech. Vzestup hmotnosti byl ovlivněn genotypem PNPLA3 a byl nejvyšší ve skupině nosičů alespoň jedné variantní alely G PNPLA3, hmotnostní nárůst v této skupině činil 0,94 kg/m2. Nosičství alely G PNPLA3 bylo jediným faktorem predikujícím nárůst hmotnosti po léčbě v multivariantní analýze [43].
MASLD jako další jaterní onemocnění
Metabolickou dysfunkcí podmíněná steatóza jater (MASLD) je v současné době nejčastějším onemocněním jater a významnou příčinou morbidity a mortality spojené s jaterními onemocněními [44], proto často existuje společně s HCV. Pacienti s HCV a steatózou jsou vystaveni riziku rychlejší progrese fibrózy a riziku HCC [45]. Dosažení eradikace viru může vést k vymizení steatózy způsobené infekcí, zejména u pacientů s genotypem 3, ale významná část pacientů má steatózu, která s HCV nesouvisí, a může tak způsobit progresi fibrózy.
Diabetes mellitus je zásadním rizikovým faktorem progrese fibrózy při hepatitidě C. HCV infekce zasahuje do inzulinového metabolizmu s následkem inzulinové rezistence a rozvoje betu [45]. Úspěšná protivirová léčba může zabránit rozvoji inzulinové rezistence či betu, ale ti, kteří mají diabetes již před zahájením léčby, normalizace glukózového metabolizmu po dosažení SVR nedosáhnou, mohou však vyžadovat nižší dávky antidiabetik [46]. V rozsáhlé studii bylo sledováno celkem 1 000 pacientů s těžkou fibrózou a cirhózou, kteří dosáhli SVR, medián sledování byl 5,7 roku. Celkem 51 pacientů vyvinulo HCC a u 101 pacientů byla zaznamenána progrese jaterního onemocnění. Přítomnost betu spolu s vyšším věkem a trombocytopenií predikovala výskyt HCC v multivariantní analýze [3].
Závěr
Díky vysoké účinnosti DAA mohou být v současné době léčeni všichni pacienti, kteří o své infekci vědí a k léčbě mají přístup. Eliminaci HCV infekce, a tedy snížení rizika pozdních komplikací, lze docílit v zemích s efektivními screeningovými programy, které jsou zaměřeny zejména na skupiny osob s vysokou prevalencí onemocnění. I osoby úspěšně vyléčené mají setrvat v programu surveillance HCC v případě, že je u nich před léčbou přítomna těžká fibróza nebo cirhóza jater.
ORCID autorky
S. Fraňková 0000-0002-1462-5920
Doručeno/Submitted: 22. 3. 2026
Přijato/Accepted: 27. 3. 2026
Korespondenční autor
MUDr. Tomáš Nesnídal
Klinika hepatogastroenterologie
Institut klinické a experimentální medicíny
Vídeňská 1958/9
140 21 Praha 4
tomas.nesnidal@ikem.cz
Literatura
1. Polaris Observatory HCV collaborators. Global change in hepatitis C virus prevalence and cascade of care between 2015 and 2020: a modelling study. Lancet Gastroenterol Hepatol 2022; 7(5): 396–415. doi: 10.1016/S2468-1253(21)00472-6.
2. Hovaguimian F, Beeler PE, Mullhaupt B et al. Mortality and morbidity related to hepatitis C virus infection in hospitalized adults-A propensity score matched analysis. J Viral Hepat 2023; 30(9): 765–774. doi: 10.1111/jvh.13861.
3. van der Meer AJ, Veldt BJ, Feld JJ et al. Association between sustained virological response and all-cause mortality among patients with chronic hepatitis C and advanced hepatic fibrosis. JAMA 2012; 308(24): 2584–2593. doi: 10.1001/jama.2012.144878.
4. European Association for the Study of the Liver. EASL recommendations on treatment of hepatitis C: final update of the series. J Hepatol 2020; 73(5): 1170–1218. doi: 10.1016/j.jhep.2020.08.018.
5. Sarrazin C, Isakov V, Svarovskaia ES et al. Late relapse versus hepatitis C virus reinfection in patients with sustained virologic response after sofosbuvir-based therapies. Clin Infect Dis 2017; 64(1): 44–52. doi: 10.1093/cid/ciw676.
6. Calvaruso V, Craxi A. Hepatic benefits of HCV cure. J Hepatol 2020; 73(6): 1548–1556. doi: 10.1016/j.jhep.2020.08.006.
7. Nemecek V, Castkova J, Fritz P et al. The 2001 serological survey in the Czech Republic – viral hepatitis. Cent Eur J Public Health 2003; (Suppl 11): S54–S61.
8. Chlibek R, Smetana J, Sosovickova R et al. Prevalence of hepatitis C virus in adult population in the Czech Republic – time for birth cohort screening. PloS One 2017; 12(4): e0175525. doi: 10.1371/journal.pone.0175525.
9. Cornberg M, Razavi HA, Alberti A et al. A systematic review of hepatitis C virus epidemiology in Europe, Canada and Israel. Liver Int 2011; 31(Suppl 2): 30–60. doi: 10.1111/j.1478-3231.2011.02539.x.
10. Frankova S, Jandova Z, Jinochova G et al. Therapy of chronic hepatitis C in people who inject drugs: focus on adherence. Harm Reduct J 2021; 18(1): 69. doi: 10.1186/s12954-021-00519-y.
11. Edlin BR. Perspective: test and treat this silent killer. Nature 2011; 474(7350): S18–S19. doi: 10.1038/474S18a.
12. Kenny-Walsh E. Clinical outcomes after hepatitis C infection from contaminated anti-D immune globulin. Irish Hepatology Research Group. N Engl J Med 1999; 340(16): 1228–1233. doi: 10.1056/NEJM199904223401602.
13. Toshikuni N, Arisawa T, Tsutsumi M. Hepatitis C-related liver cirrhosis – strategies for the prevention of hepatic decompensation, hepatocarcinogenesis, and mortality. World J Gastroenterol 2014; 20(11): 2876–2887. doi: 10.3748/wjg.v20.i11.2876.
14. Llamosas-Falcon L, Shield KD, Gelovany M et al. Impact of alcohol on the progression of HCV-related liver disease: a systematic review and meta-analysis. J Hepatol 2021; 75(3): 536–546. doi: 10.1016/j.jhep.2021.04.018.
15. Frankova S, Uzlova N, Merta D et al. Predictors of significant liver fibrosis in people with chronic hepatitis C who inject drugs in the Czech Republic. Life (Basel) 2023; 13(4): 932. doi: 10.3390/life13040932.
16. Senkerikova R, Frankova S, Jirsa M et al. PNPLA3 rs738409 G allele carriers with genotype 1b HCV cirrhosis have lower viral load but develop liver failure at younger age. PloS One 2019; 14(9): e0222609. doi: 10.1371/journal.pone.0222609.
17. Asselah T, Bieche I, Sabbagh A et al. Gene expression and hepatitis C virus infection. Gut 2009; 58(6): 846–858. doi: 10.1136/gut.2008.166348.
18. Younossi ZM, Singer ME, Mir HM et al. Impact of interferon free regimens on clinical and cost outcomes for chronic hepatitis C genotype 1 patients. J Hepatol 2014; 60(3): 530–537. doi: 10.1016/j.jhep.2013.11.009.
19. D’Ambrosio R, Aghemo A, Rumi MG et al. A morphometric and immunohistochemical study to assess the benefit of a sustained virological response in hepatitis C virus patients with cirrhosis. Hepatology 2012; 56(2): 532–543. doi: 10.1002/hep.25606.
20. Bachofner JA, Valli PV, Kroger A et al. Direct antiviral agent treatment of chronic hepatitis C results in rapid regression of transient elastography and fibrosis markers fibrosis-4 score and aspartate aminotransferase-platelet ratio index. Liver Int 2017; 37(3): 369–376. doi: 10.1111/liv.13256.
21. Pons M, Rodriguez-Tajes S, Esteban JI et al. Non-invasive prediction of liver-related events in patients with HCV-associated compensated advanced chronic liver disease after oral antivirals. J Hepatol 2020; 72(3): 472–480. doi: 10.1016/j.jhep.2019.10.005.
22. Mandorfer M, Kozbial K, Schwabl P et al. Sustained virologic response to interferon-free therapies ameliorates HCV-induced portal hypertension. J Hepatol 2016; 65(4): 692–699. doi: 10.1016/j.jhep.2016.05.027.
23. Mandorfer M, Kozbial K, Schwabl P et al. Changes in hepatic venous pressure gradient predict hepatic decompensation in patients who achieved sustained virologic response to interferon-free therapy. Hepatology 2020; 71(3): 1023–1036. doi: 10.1002/hep.30885.
24. Nahon P, Bourcier V, Layese R et al. Eradication of hepatitis C virus infection in patients with cirrhosis reduces risk of liver and non-liver complications. Gastroenterology 2017; 152(1): 142.e2–156.e2. doi: 10.1053/j.gastro.2016.09.009.
25. Carrat F, Fontaine H, Dorival C et al. Clinical outcomes in patients with chronic hepatitis C after direct-acting antiviral treatment: a prospective cohort study. Lancet 2019; 393(10179): 1453–1464. doi: 10.1016/S0140-6736(18)32111-1.
26. Mendizabal M, Pinero F, Ridruejo E et al. Disease progression in patients with hepatitis C virus infection treated with direct-acting antiviral agents. Clin Gastroenterol Hepatol 2020; 18(11): 2554–2563.e3. doi: 10.1016/ j.cgh.2020.02.044.
27. Ioannou GN, Green PK, Berry K. HCV eradication induced by direct-acting antiviral agents reduces the risk of hepatocellular carcinoma. J Hepatol 2017; S0168-8278(17)32273-0. doi: 10.1016/j.jhep.2017.08.030.
28. Kanwal F, Kramer JR, Asch SM et al. Risk of hepatocellular carcinoma in HCV patients treated with direct acting antiviral agents. Hepatology 2020; 71(1): 44–55. doi: 10.1002/hep.30823.
29. Paradis V, Dargere D, Bonvoust F et al. Clonal analysis of micronodules in virus C-induced liver cirrhosis using laser capture microdissection (LCM) and HUMARA assay. Lab Invest 2000; 80(10): 1553–1559. doi: 10.1038/labinvest. 3780165.
30. European Association for the Study of the Liver. EASL Clinical Practice Guidelines on the management of hepatocellular carcinoma. J Hepatol 2025; 82(2): 315–374. doi: 10.1016/j.jhep.2024.08.028.
31. Curry MP, O’Leary JG, Bzowej N et al. Sofosbuvir and velpatasvir for HCV in patients with decompensated cirrhosis. N Engl J Med 2015; 373(27): 2618–2628. doi: 10.1056/NEJMoa1512614.
32. Foster GR, Irving WL, Cheung MC et al. Impact of direct acting antiviral therapy in patients with chronic hepatitis C and decompensated cirrhosis. J Hepatol 2016; 64(6): 1224–1231. doi: 10.1016/j.jhep.2016.01.029.
33. Belli LS, Berenguer M, Cortesi PA et al. Delisting of liver transplant candidates with chronic hepatitis C after viral eradication: a European study. J Hepatol 2016; 64(6): 1224–1231. doi: 10.1016/j.jhep.2016.05.010.
34. Terrault NA, Zeuzem S, Di Bisceglie AM et al. Effectiveness of ledipasvir-sofosbuvir combination in patients with hepatitis C virus infection and factors associated with sustained virologic response. Gastroenterology 2016; 151(6): 1131–1140 e5. doi: 10.1053/j.gastro.2016.08.004.
35. Fraňková S, Pítová V, Šperl J. Transplantace jater pro chronickou hepatitidu C – význam protivirové léčby v roce 2024. Gastroent Hepatol 2024; 78(2): 108–114. doi: 10.48095/ccgh2024108.
36. Belli LS, Duvoux C, Berenguer M et al. ELITA consensus statements on the use of DAAs in liver transplant candidates and recipients. J Hepatol 2017; 67(3): 585–602. doi: 10.1016/ j.jhep.2017.03.006.
37. Curry MP, Forns X, Chung RT et al. Sofosbuvir and ribavirin prevent recurrence of HCV infection after liver transplantation: an open-label study. Gastroenterology 2015; 148(1): 100–107.e1. doi: 10.1053/j.gastro.2014.09.023.
38. Welsch C, Efinger M, von Wagner M et al. Ongoing liver inflammation in patients with chronic hepatitis C and sustained virological response. PloS One 2017; 12(2): e0171755. doi: 10.1371/journal.pone.0171755.
39. Tacke F, Boeker KHW, Klinker H et al. Baseline risk factors determine lack of biochemical response after SVR in chronic hepatitis C patients treated with DAAs. Liver Int 2020; 40(3): 539–548. doi: 10.1111/liv.14186.
40. Benhammou JN, Moon AM, Pisegna JR et al. Nonalcoholic fatty liver disease risk factors affect liver-related outcomes after direct-acting antiviral treatment for hepatitis C. Dig Dis Sci 2021; 66(7): 2394–2406. doi: 10.1007/s10620-020-06457-2.
41. Schlevogt B, Deterding K, Port K et al. Interferon-free cure of chronic hepatitis C is associated with weight gain during long-term follow-up. Z Gastroenterol 2017; 55(9): 848–856. doi: 10.1055/s-0043-112656.
42. Do A, Esserman DA, Krishnan S et al. Excess weight gain after cure of hepatitis C infection with direct-acting antivirals. J Gen Intern Med 2020; 35(7): 2025–2034. doi: 10.1007/s11606-020-05782-6.
43. Pítová V, Fraňková S, Holinka M et al. PNPLA3 I148M variant is the main driver of weight gain after hepatitis C cure. Sci Rep 2025; 15(1): 25543. doi: 10.1038/s41598-025-11085-9.
44. Eslam M, Newsome PN, Sarin SK et al. A new definition for metabolic dysfunction-associated fatty liver disease: an international expert consensus statement. J Hepatol 2020; 73(1): 202–209. doi: 10.1016/j.jhep.2020.03.039.
45. Bugianesi E, Salamone F, Negro F. The interaction of metabolic factors with HCV infection: does it matter? J Hepatol 2012; 56(Suppl 1): S56–S65. doi: 10.1016/S0168-8278(12)60007-5.
46. Dawood AA, Nooh MZ, Elgamal AA. Factors associated with improved glycemic control by direct-acting antiviral agent treatment in Egyptian type 2 betes mellitus patients with chronic hepatitis C genotype 4. Diabetes Metab J 2017; 41(4): 316–321. doi: 10.4093/dmj.2017.41.4.316.