Úloha endoskopické ultrasonografie s cílenou biopsií v diferenciální diagnostice ložiskových procesů slinivky břišní
Radan Keil Orcid.org 1, Luděk Hrdlička Orcid.org 2,3, Jan Leffler Orcid.org 4, Jaromír Šimša Orcid.org 5, Daniela Kodetová Orcid.org , Pavel Pafko Orcid.org
+ Pracoviště
Souhrn
Úvod: Autoři ve svém sdělení hodnotí přesnost predoperační diagnostiky u souboru pacientů s podezřením na tumor pankreatu, kteří byli vhodnými kandidáty operačního řešení. Věnují se zejména roli endoskopické ultrasonografie s cílenou biopsií (EUS s FNAB).
Cíl studie: Cílem studie je prokázat vysokou senzitivitu EUS s FNAB u pacientů s ložiskovým postižením pankreatu na vlastním souboru pacientů.
Materiál a metodika: 52 pacientů s patologickým ložiskem v hlavě pankreatu, potencionálně operabilních, byl vyšetřen predoperačné endoskopickou retrográdní cholangiopankreatikografií (ERCP), počítačovou tomografií (CT) a EUS ke stanovení diagnózy a stagingu. Dále byla provedena cílená punkční biopsie pod kontrolou lineární EUS. Výsledek punkční biopsie byl později porovnán s histologickým nálezem tkání odebraných při operaci (resekát pankreatu u radikálně operovaných, excise či peroperační punkční biopsie u radikálně neresekovaných pacientů) - „zlatým standardem" v rozlišení mezi karcinomem pankreatu a jinými ložiskovými změnami slinivky břišní, zejména při chronické pankreatitidě.
Výsledky: Nejsensitivnější metodou je endoskopická ultrasonografie s cílenou biopsií (senzitivita 78 %), ostatní metody (CT - senzitivita 61 %, ERCP - senzitivita 73 %) jsou v našem souboru pacientů méně citlivé. Ve vyšetřovaném souboru nebyla zaznamenána žádná závažná komplikace vyšetření.
Závěr: Nejvhodnější metodou v diagnostice a stagingu choroby se podle výsledků studie jeví endoskopická ultrasonografie s cílenou biopsií (senzitivita 78%). Výsledky jsou v rámcové shodě s už publikovanými pracemi.
Klíčová slova: aspirační biopsie - endosonografie - chronická pankreatitida - nádor pankreatu - operace.
ÚVOD
Karcinom pankreatu je onemocnění se stále se zvyšující incidencí a jeho celkové 5leté přežití je nižší než 1 %(1). Jeho etiologie, příčina rychlé progrese, časné generalizace a velmi špatné prognózy nejsou ještě zcela detailně objasněny. Průměrné přežití neléčených pacientů je jen několik měsíců od stanovení diagnózy. V literatuře je sice uváděno průměrné 5leté přežití operovaných pacientů 3 %, nicméně po resekcích pankreatu, kde okraje resekátu nebyly infiltrované nádorem a regionální lymfatické byly negativní, se 5leté přežití blížilo 25 %(2). Ačkoliv vývoj nových chemoterapeutických režimů přináší alespoň částečně optimistické výhledy, radikální úspěšná chirurgická léčba je stále jedinou terapeutickou modalitou signifikantně zlepšující prognózu nemocného. Proto je nezbytné zlepšení časné diagnostiky a předoperačního stagingu.
Klasickými diagnostickými metodami bylo sonografické vyšetření, vyšetření počítačovou tomografií (CT) a endoskopická retrográdní cholangiopan-kreatikografie (ERCP). Později přibylo zobrazení pomocí nukleární magnetické rezonance (MRI) pozitronové emisní tomografie (PET) stanovení tumorových markerů (CA 19-9, CEA). Endosonografická ultrasonografie (EUS) se stala rutinní součástí diagnostiky ložiskových změn pankreatu, zejména díky přesnosti lokálního stagingu a možnosti cíleného odběru patologické tkáně (fine needle aspiration - FNA). Dříve byl neoperační odběr tkáně možný jen při CT zaměřené biopsii. Tato metoda má však velké riziko peritoneální diseminace tumoru a je zatížena poměrně vysokým procentem falešně negativních nálezů, kterých je kolem 20 %(3). Podobně je více než 30% falešnou negativitou nálezů zatížena kartáčová cytologie odebraná při ERCP(4).
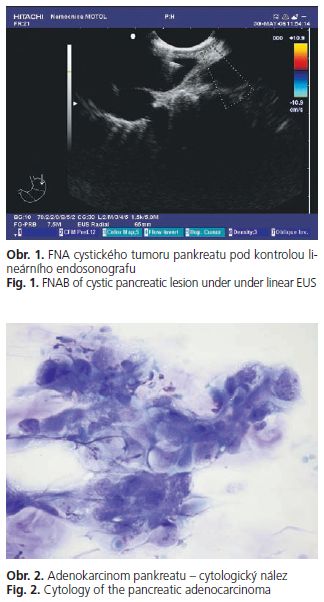
Žádná z uvedených metod zatím nebyla stanovena zlatým standardem v diagnostice karcinomu pankreatu a v diferenciální diagnostice ložiskových lézí pankreatu, zejména s ložiskovými změnami při chronické pankreatitidě(5-12).
Lehce kontroverzní je otázka, kteří pacienti se suspekcí na tumor pankreatu jsou k EUS-FNA jednoznačně indikováni a kteří mohou být směřováni k chirurgické intervenci bez tohoto vyšetření. Většina autorů se shoduje, že indikací je předchozími vyšetřeními ověřený neoperabilní nález k získání cytologie pro adjuvantní chemo- nebo rádioterapii, ale vyloučení jiného typu nádoru než karcinomu (lymfom, neuro endokrinní nádor, metastáza) vyžadujícího odlišný terapeutický přístup, potvrzení pravděpodobné diagnózy karcinomu u pacientů, kteří nechtějí absolvovat rozsáhlý chirurgický výkon bez jednoznačné histologický ěřené povahy ložiska a dále verifikace benigního nálezu pravděpodobného z předchozích vyšetření(13).
Zvláštní roli má EUS a FNA v diferenciální diagnostice cystických expanzí pankreatu. Stanovením koncentrace jednotlivých tumorových markerů v aspirátu, jako je CEA, CA 19-9 aj. kombinaci s cytologickým šetřením může s pravděpodobností predikovat biologickou povahu cystické léze(14).
Cílem práce bylo u pacientů, kde vzniklo podezření na ložiskový proces v oblasti pankreatu (solidní či cystický) předchozích vyšetření (ERCP, CT, EUS), považovaných za vhodné kandidáty operačního řešení, provést cílenou biopsii z oblasti ložiska pod endosonografickou kontrolou (EUS-FNA). U vyšetřených nemocných poté byla provedena chirurgická revize a histologické šetření resekátu. U pacientů s neresekabilným nálezem byla provedena peroperační biopsie. Výsledek biopsie pod EUS kontrolou byl srovnán s histologickým nálezem tkání odebraných při operaci. Naší snahou bylo prokázat vysokou senzitivitu a specificitu endosonografické cílené biopsie u ložiskového procesu pankreatu a v neposlední řadě ji porovnat s ostatními zobrazovacími metodami používanými v diagnostice karcinomu pankreatu a srovnat námi získaná data s již publikovanými pracemi, stejně jako zhodnotit bezpečnost metody.
MATERIÁL A METODIKA
Nemocní s patologickým ložiskem v hlavě pankreatu byli vyšetřeni předoperačné , CT, EUS ke stanovení stagingu a byla provedena cílená punkční biopsie pod EUS kontrolou. U solidních tumorů byla hodnocena cytologie z FNA odběru, u cystických cytologie a biochemie (CA 19-9, CEA) z aspirátu. Výsledek punkční biopsie byl později srovnán s histologickým nálezem tkáních odebraných při operaci (resekát pankreatu u radikálně operabilních, excise či peroperační punkční biopsie u radikálně neresekovaných pacientů).
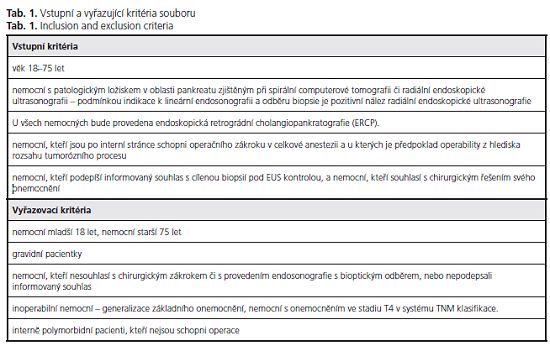
Vstupní (inclusion) vyřazující (exclusion) kriéria našeho souboru jsou uvedena v tabulce 1.
Náš soubor zahrnuje 52 pacientů, z toho 28 mužů (54 %) a 24 žen (46 %). Průměrný věk nemocných byl 58 let.
Staging byl prováděn podle AJCC (American Joint on Cancer), z roku 2002. Vyšetření byla realizována v Endoskopickém centru Interní kliniky FN Motol za použití lineárního endosonografu Pentax FG-38UX, zobrazovací jednotky Hitachi - 6500, aspirační cytologie byla prováděna punkční jehlou ECHOTIP Ultra kalibru 22 GA (Cook).
Všechna endoskopická vyšetření a odběry materiálu byly provedeny jedním endosonografistou, aspiráty byly hodnoceny jedním cytopatologem.
VÝSLEDKY
V souboru byl solidní tumor zjištěn u pacientů (79%), cystický pak u (21 %) nemocných. Průměrná velikost bioptovaného tumoru byla 29,1 mm. Průměrně byly prováděny 2 biopsie při jednom sezení.
Pozitivní nález malignity z výsledku FNAB (cytologie, jednoznačná pozitivita Tu markerů u cystických ádorů) byl zachycen u pacientů (46 %). Operovaných bylo 37 pacientů z našeho souboru (71 %). Neoperováno bylo 15 nemocných (29 %) pro benigní nález nevyžadující operační řešení, následně zjištěnou generalizaci onemocnění nebo pro neúnosnost k náročnému operačnímu výkonu zjištěnou bezprostředně před plánovaným výkonem (pacient k němu kontraindikován anesteziologem).
U operovaných pacientů byla shoda v histologické diagnóze mezi nálezem FNAB a resekátem nebo peroperačním histologickým nálezem u z 37 operantů (78%). Co se stagingu u karcinomů týče, bylo dle EUS nálezu 7% ve stadiu TI, 41 % ve stadiu T2, 52 % ve stadiu T3.
Shoda T před operací dle EUS s operačním nálezem byla v 88 %. U 12 % nemocných se dle EUS jednalo o stadium T2, operačně pak zjištěn karcinom ve stadiu T3.
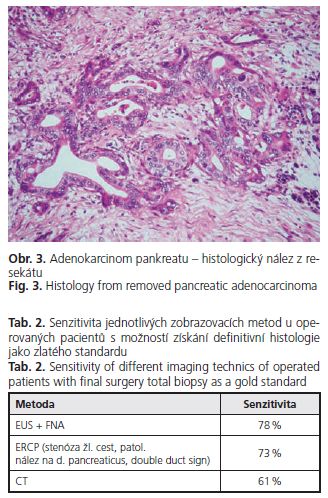
U operovaných pacientů byla senzitivita v předoperačním stanovení diagnózy vyšší u EUS s FNA (78 %), nižší u ERCP a CT (tab. 2).
V našem souboru nebyla zaznamenána žádná komplikace tohoto invazivního vyšetření.
ZÁVĚR
Senzitivita EUS s v diagnostice ložiskových procesů v pankreatu byla v našem souboru operovaných pacientů vysoká (78 %), převyšovala senzitivitu ostatních stagingových předoperačních zobrazovacích metod. Velmi vysoká byla výtěžnost metody v lokálním stagingu (88 %), avšak u 12 % nemocným bylo při operaci zjištěno vyšší stadium choroby.
DISKUSE
V literatuře jsou nejčastěji srovnávány dvě nejužívanější a nejsenzitivnější diagnostické metody - EUS a CT (v kontrastní, spirální variantě). Metaanalýza 4 rozsáhlých studií, porovnávajících tyto metody(5), zjiš»uje větší senzitivitu EUS nad CT (97 % vs. 73 %) v diagnostice karcinomu pankreatu, větší přesnost ve stanovení resekability (91 vs. 83 %) a v detekci invaze do cévních struktur (91 % vs. 64 %). Avšak, jsou-li jednotlivé podstudie hodnoceny samostatně, dvě z nich zjiš»ují EUS rovnocenné s CT(6,7)a dvě studie hodnotí EUS jako senzitivnější než CT(8,9), stejně jako naše publikace vycházející z předběžných výsledků(15). Senzitivita EUS se ještě zvýší při EUS cílené FNA – 85-90 % senzitivita, 90-95 % specificita pro detekci tumorů, 88% senzitivita pro detekci patologicky změněných mízních uzlin(10,11). Rozdíly ve výtěžnosti jednotlivých vyšetření se extrémně zvýrazňují ve prospěch EUS s FNA u drobných tumorů pankreatu do velikosti 20 mm(12).
Citovaná literární data jsou z renomovaných světových center s tradicí provádění EUS s FNA. Výsledky jsou srovnatelné a k číslům výše citovaným se blíží.
Na našem pracovišti používáme punkční jehlu o kalibru 22 G. Průměrně byly při vyšetření jednoho pacienta provedeny dva vpichy aspirace. Nedošlo k žádné závažné komplikaci. V literatuře je jako nejčastější a zároveň nejzávažnější komplikace uváděno retroperitoneální krvácení bud z pankreatické tkáně punkčním kanálem, nebo z velkých cév v okolí pankreatu poškozených punkční jehlou. Bohužel z personálních důvodů nebyla realizovatelná trvalá přítomnost cytopatologa u šetření. Prospektivní práce Eriksona et al. (2004) totiž prokázala na souboru 109 nemocných, do kterého byla zahrnuta biopsie tumorů pankreatu, sedmi zvětšených lymfatických a sedmi jaterních metastáz, vhodnost přítomnosti cytopatologa přímo při odběru. Ze závěrů této studie vychází, že pokud není patolog přímo přítomen u odběru bioptického materiálu, je počet biopsii bud příliš nízký (tím klesá i diagnostická přesnost metody), či vysoký (tím stoupají náklady a riziko komplikací). Tato práce dále ukázala, že k dobře diferencovaných adenokarcinomů bylo třeba signifikantně většího počtu biopsii než u nádorů středně či špatně diferencovaných. V práci jsme diagnostickou přesnost s na různou diefrenciaci nádorů nehodnotili. I podle ostatních prací je senzitivita a specificita vyšší, pokud je cytopatolog přítomen přímo na pracovišti(16). Přítomnost cytopatologa při vyšetření je tedy směr, kam se při snaze o zpřesnění a zefektivnění metody ubírat.
Z výše uvedeného se zdá pravděpodobné, že tato metoda se při stále plošnějším rozšíření stane doporučovaným zlatým standardem v diagnostice ložiskových změn slinivky břišní.
LITERATURA
- 1. Santo E. Pancreatic cancer imaging: Which method? JOP 2004, 5: 253-7.
- 2. Stephens J, et al. Surgical morbidity, mortality and long term survival in patients with pancreatic cancer following pancreaticoduodenectomy. Am J Surg 1997; 174: 600-604
- 3. Bret PM, et al. Percutaneus fine-needle aspiratin biopsy of pancreas. Diagn Cytopathol 1986; 2: 221-227.
- 4. Lee JG, et al. Tissue sampling at ERCP in suspected pancreatic cancer. Gastrointest. Endo Clin N Am 1998;8:221-235.
- 5. Hunt GC, et al. Assessment of EUS for diagnosing, staging and determining resectability of pancreatic cancer: a review. Gastrointest Endosc 2002; 55: 232-237.
- 6. Legmann, et al. Pancreatic tumors: Comparison of dual phase helical CT and endoscopic sonography AJR am J Roent 1998; 170: 1315-1322.
- 7. Midwinter MJ, et al. Correlation between spiral CT, EUS and findings at operation in pancreatic and ampullary tumors. Br J Surg 1999; 86: 189-193.
- 8. Mertz HR, et al. EUS, PET and CT scanning for evaluation of pancreatic carcinoma. Gastrointest Endoscop 2000; 52: 367-371.
- 9. Harewood GC, et al. Endosonography-guided FNAB in the evaluation of pancreatic masses. Am J Gastronetrol 2002; 97: 1386-1391.
- 10. Chang KJ, et al. The clinical utility of EUS guided FNA in the diagnosis and staging of pancreatic carcinoma. Gastrintest Endosc 1997; 45: 387-393.
- 11. Levy MJ, et al. Chronic pancreatitis: Focal pancreatitis or cancer? Is there a role for FNA/biopsy? Autoimune pancreatitis. Endoscopy 2006, 38 (SI): 30-35.
- 12. Maguchi, et al. Small pancreatic lesions: Is there need for EUS-FNA preoperatively? What to do with incidental lesions? Endoscopy 2006; 38 (Suppl 1): 50-53.
- 13. Wallace MB, et al. EUS and FNA forpancreatic cancer Digestive Endoscopy 2004; 16 (Suppl 2): 193-196.
- 14. Brugge WR, et al. Cystic pancreatic lesions: Can we diagnose them accurately what to look for? FNA marker, molecular analysis resection, surveillance, or endoscopic treatment? Endoscopy 2006; 38 (Suppl 1): 40-47.
- 15. Keil R, Hrdlička L, Leffler J, Šimša J, Pafko P, Kodetová D. Dignostika tumoru pomocí cílené biopsie kontrolované lineárním endosonografem. Bulletin HPB 2006; 14: 104-107.
- 16. Rickes S, Malfertheiner P. Echo-enhanced sonography - an increasingly used procedure for the differentiation of pancreatic tumour. Dig Dis 2004; 22: 32-38.
Práce byla řešena s podporou grantu IGA 1 A/8611-3.
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené