Samoexpandibilní potahovaný metalický stent Daniš jako bridging k transplantaci jater
Eva Kostolná Orcid.org 1, Soňa Fraňková Orcid.org 1, Jan Šperl Orcid.org 1, Pavel Drastich Orcid.org 1, Tomáš Hucl Orcid.org 1, Julius Špičák Orcid.org 1
+ Pracoviště
Souhrn
Popisujeme případ 66leté pacientky, dlouhodobě bez zásadních interních onemocnění, která byla v září 2010 léčena 3 týdny amoxicilinem v dávce 1 000 mg denně pro suspektní Lymskou boreliózu (erythema migrans). Těsně před ukončením antibiotické léčby se u pacientky objevil ikterus. Byla diagnostikována pokročilá jaterní cirhóza velmi pravděpodobně autoimunní etiologie, zhoršení stavu uzavřeno jako „acute on chronic“ jaterní selhání při lékové toxicitě. Pro progresi jaterní dysfunkce byla nemocná indikována k transplantaci jater. Třetí den po zařazení do čekací listiny došlo ke krvácení z jícnových varixů, které se nepodařilo ošetřit endoskopickou ligací, a nemocné byl zaveden samoexpandibilní potahovaný metalický jícnový stent Daniš. Při významné jaterní insuficienci a trvající encefalopatii nebylo možné provést transjugulární intrahepatální portosystémovou spojku (TIPS) a pacientka byla ponechána s Danišovým stentem až do samotné transplantace jater. Třetí den po ortotopické transplantaci jater, celkově pak 12. den po zavedení stentu, byla provedena jeho nekomplikovaná extrakce, na sliznici jícnu byly popsané jen minimální povrchové ulcerace. Pacientka je téměř 7 let po úspěšné transplantaci jater s dobrou funkcí štěpu.
Klíčová slova
samoexpandibilní stent, transplantace jater, varikózní krvácení
Úvod
Incidence jaterní cirhózy celosvětově narůstá, u > 50 % nemocných dochází k dekompenzaci a rozvoji portální hypertenze s jícnovými varixy. Varikózní krvácení patří mezi velmi závažné a potenciálně letální komplikace portální hypertenze. Roční riziko krvácení u nemocných s kompenzovanou jaterní cirhózou činí kolem 4–8 %. U nemocných s velkými varixy a dekompenzovanou jaterní cirhózou pak riziko krvácení stoupá na 10–15 %. Dochází-li k rozvoji dalších komplikací, zvyšuje se riziko až na 60–70 % [1,2]. První ataka krvácení je stále zatížena vysokou letalitou. Navzdory intenzivní terapii se mortalita pohybuje v rozmezí 15–20 %. Nemocní jsou navíc ohroženi recidivou, nejvíce v prvních 5 dnech [2]. Pacienti indikovaní k transplantaci jater patří mezi skupinu rizikových pacientů ohrožených varikózním krvácením při progresi základního onemocnění, a tím i možným úmrtím na čekací listině. Účinná terapie je zajištěna endoskopickou ligací či sklerotizací v kombinaci s vazoaktivní léčbou. Při recidivujícím či endoskopicky neošetřitelném krvácení je možným řešením provedení transjugulární intrahepatální portosystémové spojky (TIPS). Přechodným řešením může být balonková tamponáda. Dnes běžně uznávanou metodou zástavy významného krvácení je zavedení samoexpandibilního potahovaného metalického jícnového stentu (Daniš), který slouží jako alternativa balonkové sondy či je přemostěním k provedení TIPS. Stejně tak je efektivním řešením u pacientů, u kterých je TIPS kontraindikován
[2,3–5].
Popis případu
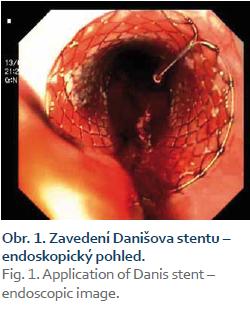
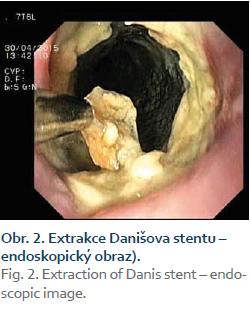
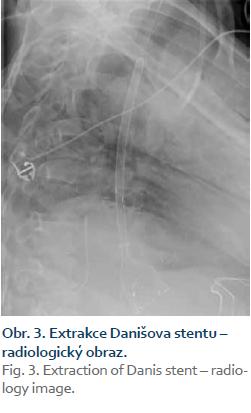
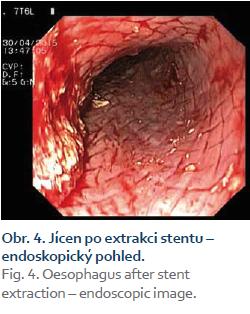
Pacientka, 66 let, byla přijata na naši kliniku v říjnu 2010 pro jaterní selhání jako kandidátka transplantace jater. Dlouhodobě byla bez zásadních interních onemocnění. V srpnu 2010 začala pro významnou pyrózu užívat omeprazol v celkové dávce 40 mg denně. Během září 2010 jí byla nasazena 3týdenní kůra antibiotik (amoxicillin 1 000 mg denně) pro suspektní Lymskou boreliózu, erythema migrans na levé dolní končetině. Již před ukončením antibiotické léčby pozorovala pacientka tmavou moč a světlou stolici, zhoršila se dyspepsie, měla subfebrilie až febrilie. K medikaci jí bylo proto doporučeno užívání paracetamolu (1–2 tablety 500 mg denně po dobu 7 dní). Následně došlo k rozvoji ikteru. Nemocná byla hospitalizována na interním oddělení, vstupní hodnota celkového bilirubinu byla 255 µmol/l, dále byla patrna výrazná elevace aktivity aminotransferáz (AST 47 µkat/l, ALT 27,25 µkat/l) i cholestatických enzymů (ALP 5,4 µkat/l, GGT 6,42 µkat/l). Během hospitalizace byly vyloučeny virové hepatitidy A, B, C i E, dále cytomegalovirus, leptospiróza. Negativní byly vyšetřené autoprotilátky LKM, AMA, ASMA, pozitivní byly ANA protilátky v titru 1: 160. Laboratorně byly zaznamenány vyšší hodnoty gamaglobulinů (39,5 %) a AFP (36,5 g/l). Sonografií popsána difuzní hepatopatie a mírná splenomegalie, nebyl přítomen ascites. Gastroskopicky zjištěny malé jícnové varixy. Pacientka klinicky nejevila známky encefalopatie. Pro progresi ikteru (celkový bilirubin 411 µmol/l), hypoalbuminemie (26,3 g/l) a koagulopatie (INR 1,7) byla zahájena kortikoterapie (prednisolon v úvodní dávce 60 mg/den), přesto nedošlo k poklesu hodnot celkového bilirubinu, pouze k poklesu aktivity hodnot aminotransferáz na polovinu. V říjnu 2010 byla pacientka přeložena na naši kliniku. Při přijetí hodnocena jako plně orientovaná, bez známek encefalopatie, sytě ikterická. Vstupní laboratorní vyšetření potvrdilo významnou poruchu syntetické jaterní funkce, hodnota celkového bilirubinu byla 366 µmol/l, AST 17,02 µkat/l, ALT 12,86 µkat/l, ALP 3,78 µkat/l, GGT 2,42 µkat/l, albumin 19,0 g/l, INR 1,5, AFP 34,4 µg/l. Jaterní dysfunkce odpovídala stupni C Child-Pughovy klasifikace (11 bodů), MELD skóre bylo 26 bodů. Sonografické vyšetření břicha popisovalo cirhotickou přestavbu nezvětšených jater, bez ložiskového procesu, s normálním tokem v portální žíle (13 mm) a v jaterních žilách, nově s malým ascitem, beze změn na žlučovém intra-i extrahepatálním stromu, slezina měřila 12 cm. Na základě provedených vyšetření byla etiologie onemocnění uzavřena jako autoimunní cirhóza, akutní zhoršení jsme přisoudili polékovému poškození. V následujících 7 dnech nedošlo při stávající terapii kortikoidy (prednisolon 60–50–40 mg/den) k poklesu celkového bilirubinu (374,3 µmol/l), trvala koagulopatie (INR 1,5). Desátý den hospitalizace byla provedena transjugulární biopsie s nálezem těžké fibrózy až cirhózy jater a rozsáhlými plošnými subakutními nekrózami a těžkou cholestázou. Vzhledem k faktu, že nedošlo ke zlepšení syntetické jaterní funkce, ale progredovala encefalopatie a ascites, byla pacientka protokolárně vyšetřena jako kandidátka transplantace jater. Během hospitalizace, 26. den, byla nemocná zařazena na čekací listinu k transplantaci jater se základní diagnózou dosud neléčené autoimunní jaterní cirhózy s akutním zhoršením jaterních funkcí při antibiotické léčbě („acute on chronic“ jaterní selhání). Následující den (28. hospitalizační den) došlo k masivní hemateméze, anemizaci (hemoglobin 83 g/l) a progresi encefalopatie. Gastroskopie prokázala krvácení z velkých jícnových varixů. Byla zahájena endoskopická ligace varixů, avšak po naložení dvou ligatur došlo k dalšímu masivnímu krvácení, které již nebylo možné endoskopicky ošetřit. Vzhledem k významné jaterní dysfunkci s encefalopatií nebylo v tomto případě indikováno zavedení TIPS, ale bylo přistoupeno k zavedení samoexpandibilního potahovaného metalického jícnového stentu (SX-Ella stent Danis®) (obr. 1). Současně byla zahájena terapie terlipresinem v dávce 1 mg i.v./4 hod, byly podány celkem čtyři transfuzní jednotky erymasy. Po zavedení stentu došlo ihned k zástavě krvácení z varixů a stabilizaci celkového stavu. V následujících dnech nedošlo k recidivě krvácení ani progresi jaterní dysfunkce, jaterní encefalopatie byla stacionárně II. stupně. Devátý den po krvácení podstoupila pacientka se stále zavedeným jícnovým stentem ortotopickou transplantaci jater celým štěpem, s časnou operační revizí pro hemoperitoneum. Histologický nález v jaterním explantátu byl shodný s nálezem v transjugulární biopsii, morfologicky dobře kompatibilní s klinicky zvažovanou autoimunní etiologií. Třetí den po transplantaci jater, celkově tedy 12. den po zavedení jícnového stentu, byla provedena jeho nekomplikovaná extrakce (obr. 2–4). Kontrolní gastroskopie prokázala pouze minimální povrchové ulcerace v oblasti distálního jícnu, varixy nebyly přítomny. Rozvoj funkce jaterního štěpu byl okamžitý, další průběh nekomplikovaný. Nyní je pacientka téměř 7 let po transplantaci v dobré klinické kondici.
Diskuze
Varikózní krvácení při portální hypertenzi je nejčastější život ohrožující komplikací. U nemocných s pokročilou jaterní cirhózou i při intenzivní terapii má první ataka krvácení stále vysokou letalitu
(15–20 %), až 2/3 nemocných mohou zemřít v důsledku krvácení v prvních 24 hod. Současně je vysoké riziko recidivy krvácení, zejména v prvních 5 dnech [1]. Metodou první volby u akutního krvácení je endoskopická ligace, v kombinaci s vazoaktivní terapií přináší nejlepší kontrolu akutního varikózního krvácení a současně snižuje riziko časné recidivy krvácení [2]. Mezi rizikové faktory selhání léčby patří prohlubující se porucha syntetické jaterní funkce (Child B–C), progrese portální hypertenze (vysoký portosystémový gradient HVPG > 16–20 mm Hg, vstupní známky šoku, aktivní krvácení v době endoskopického výkonu, asociovaná trombóza portální žíly či renální insuficience [2,6]. V případě nutnosti dočasného zajištění zástavy akutního krvácení lze použít trojcestnou balonkovou Sengstaken-Blakemorovy sondu, která je vysoce účinná, ale po jejím uvolnění je recidiva krvácení stále > 50 %. Zavedení sondy je možné jen po dobu 24 hod s pečlivým monitorováním tlaku v jícnovém balonku, současně je často nutné přistoupit k intubaci pacienta pro riziko aspirace. Mezi další komplikace patří ulcerace až lacerace, tlakové nekrózy nebo perforace jícnu. Od roku 2002 je k zástavě varikózního krvácení používán samoexpandibilní metalický jícnový stent (SX-Ella stent Danis®) [2,5], který svým přímým expanzním tlakem stěny komprimuje krvácející varix, a působí tak proti portálnímu tlaku. V porovnání s balonkovou sondou dochází k zástavě krvácení v 90–100 % [5], přináší možnost delšího časového úseku zajištění pacienta k překlenutí období s vysokým rizikem recidivy krvácení, a tím otvírá možnost zahájení adekvátní následné terapie, v prvé řadě zavedení TIPS. Zároveň poskytuje jeho zavedení větší komfort pro nemocné a umožňuje při stabilizaci stavu obnovit částečný perorální příjem. U nemocných s pokročilým jaterním onemocněním poskytne prostor k restituci jaterních funkcí a následné léčbě základního jaterního onemocnění. Ponechání jícnového stentu je doporučováno 2–10 dní [7]. Na základě konsenzuálního workshopu v italském Bavenu v roce 2015 je použití jícnového stentu doporučováno jako alternativa při recidivujícím varikózním krvácení, při nemožnosti urgentní por-tosystémové spojky nebo k překlenutí doby k provedení TIPS. Za záchrannou léčbu je stále považováno zavedení TIPS, které vede k okamžité zástavě krvácení u 91–100 % nemocných. Danišův stent je alternativou také tam, kde není možné zavést TIPS z důvodu těžké poruchy syntetické jaterní funkce, progrese encefalopatie či jiné závažné komorbidity [2,8]. V literatuře je dokumentováno několik retrospektivních studií [5,9,10]. V roce 2015 byla publikována retrospektivní metaanalýza autorů ze Španělska a Belgie [9] zahrnující celkem 13 studií se 146 pacienty. Analyzováno bylo využití samoexpandibilního jícnového stentu u významného či recidivujícího varikózního krvácení u pacientů s jaterní cirhózou. Ve 12 studiích byl používán SX-Ella stent, v jedné studii jiný potahovaný metalický stent. Primárním cílem bylo zhodnocení mortality obecně (40 %), mortality ve vztahu k jaternímu onemocnění (41 %) a 30denní mortality (36 %). Sekundárním cílem bylo hodnocení mortality ve vztahu k varikóznímu krvácení, které činilo 12 %, selhání léčby jícnovým stentem (18 %) a recidiva krvácení po extrakci jícnového stentu (16 %). Dislokace stentu byla popisována u 28 % pacientů. Méně než 40 % nemocných léčených zavedením jícnového stentu zemřelo v průběhu 30 dní. U 26 % pacientů bylo definitivní léčbou krvácení zavedení TIPS, u 10 % transplantace jater. V roce 2016 byla publikována zatím jediná multicentrická randomizovaná studie španělských autorů [5] srovnávající užití trojcestné balonkové Sengstaken-Blakemorovy sondy a samoexpandibilního metalického jícnového stentu
(SX-Ella stent Danis®) u pacientů s pokročilou jaterní cirhózou (Child B–C) s recidivujícím akutním varikózním krvácením, u kterých selhala medikamentózní a endoskopická terapie. Primárním cílem studie byla úspěšná terapie krvácení, přežití 15 dní a absence recidivujícího krvácení a závažných komplikací obou metod. Do studie bylo během 4 let zařazeno 28 pacientů (15 pacientů s ba-lonovou tamponádou zavedenou 24 hod, 13 pacientů s jícnovým stentem zavedeným po dobu 7 dnů). Tam, kde selhala terapie varikózního krvácení jednou či druhou metodou, bylo rescue metodou zavedení TIPS. Významný statistický rozdíl ve prospěch Danišova stentu byl hlavně v posouzení absence recidivy krvácení během 15 dní (85 vs. 47 %; p = 0,037), přežití ve skupině s jícnovým stentem bylo lepší než u balonové tamponády bez statistické významnosti (69 vs. 47 %; p = 0,39) a výskyt nežádoucích komplikací byl podstatně nižší ve skupině Danišova stentu (15 vs. 47 %; p = 0,077). Ve skupině s jícnových stentem bylo také méně zavedených TIPS (4 vs. 10 pacientů; p = 0,12). Studie prokázala, že použití samoexpandibilního jícnového metalického stentu ve srovnání s balonkovou tamponádou se jeví jako efektivní metoda v zajištění kontroly akutního či recidivujícího varikózního krvácení u pacientů s pokročilou jaterní cirhózou s podstatně menší incidencí komplikací. Na našem pracovišti byl v období 6 let (únor 2010 až únor 2017) aplikován Danišův stent u 21 pacientů s krvácením při portální hypertenzi (11 mužů a 10 žen, průměrný věk 54,5 let, rozmezí 27–80 let). U 17 pacientů (81,0 %) byla příčinou portální hypertenze jaterní cirhóza (52,9 % Child-Pugh C), u 4 pacientů (21,1 %) trombóza portální žíly či venookluzivní nemoc jater. Danišův stent byl aplikován 5 nemocným (23,8 %) pro první ataku významného varikózního krvácení bez předchozí endoskopické intervence, 6 pacientům (28,6 %) pro recidivující varikózní krvácení (po předchozích 1–3 epizodách) a 10 pa-cientům (47,6 %) pro krvácení z ulcerací po předchozí endoskopické ligaci či sklerotizaci. Technická úspěšnost zavedení stentu byla u 19 pacientů (90,5 %), u 2 pacientů (9,5 %) se stent nepodařilo zavést vůbec (v prvním případě docházelo k opakované dislokaci stentu, v druhém případě došlo k technickému problému nerozvinutí stentu). Aplikovaný stent byl ponechán průměrně 10,6 dní (v rozmezí 1–35 dní). Dislokace stentu proximálně do jícnu a částečně do žaludku byla zaznamenána pouze ve 2 případech (9,5 %), přesto byl stent ponechán. Při extrakci stentu nebyly shledány významné změny na sliznici jícnu, pouze v 6 případech (21,4 %) byly viditelné hojící se ulcerace, v 1 případě (3,6 %) mykotické postižení. Z 21 nemocných bylo po stabilizaci stavu indikováno provedení TIPS u 7 pacientů (33,3 %). K transplantaci jater pak bylo indikováno 6 pa-cientů (28,6 %), z nichž pouze 2 pa-cienti transplantaci jater podstoupili (1 pacientka se zavedeným Danišovým stentem – viz popis případu, 1 nemocná 8 měsíců po extrakci stentu), 1 nemocný zemřel na čekací listině pro progresi jaterního onemocnění, 2 nemocní zemřeli před zařazením na čekací listinu a 1 nemocná transplantační léčbu odmítla. Ve sledovaném souboru zemřelo celkem osm pacientů (38,1 %) v období 1.–35. den od epizody krvácení. Dva nemocní (33,3 %) zemřeli do 24 hodin pro hemoragický šok i po technicky úspěšné aplikaci stentu, jeden nemocný (12,5 %) krátce po neúspěšném zavedení stentu, pět pacientů (62,5 %) zemřelo z důvodu progrese jaterního selhání, infekčních nebo nádorových komplikací (úmrtí v rozmezí 5.–35. den). Čtyři retrospektivní studie hodnotící celkem 79 pacientů popisují osm pacientů, kterým byl zaveden Danišův stent, a následně byli indikováni k transplantační léčbě [11–14]. Čtyři pacienti (10 %) pak transplantační léčbu úspěšně podstoupili. Potahovaný jícnový stent zde sehrál roli jako bridging k definitivní léčbě. Pouze v jedné z uváděných prací je popsána krátká kazuistika 62letého pacienta s akutním jaterním selháním, indikovaného k urgentní transplantaci ja-ter [12]. Několik hodin před operačním výkonem došlo k významnému krvácení z jícnových varixů a ulcerací. Pro pokračující krvácení z ulcerací i po endoskopické ligaci varixů a nemožnosti provedení TIPS byl zaveden Danišův stent, který byl extrahován po nekomplikované úspěšné transplantaci jater.
Závěr
Popisovaný případ demonstruje, že zavedením jícnového samoexpandibilního metalického stentu došlo nejen k zástavě endoskopicky neošetřitelného varikózního krvácení, a tím i k efektivnímu překlenutí období s vysokým rizikem recidivy varikózního krvácení v době na čekací listině. Potahovaný jícnový stent v dané situaci pomohl překlenout období, kdy nebylo možné provést TIPS pro těžkou jaterní dysfunkci s progredující encefalopatií a zajistil tak stabilizaci pacientky na čekací listině. Nemocná pak podstoupila v krátkém horizontu úspěšnou ortotopickou transplantaci jater se stále zavedeným Danišovým stentem. Ten byl úspěšně extrahován po samotné transplantaci jater.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané
do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“
for biomedical papers.
Doručeno/Submitted: 3.5. 2017
Přijato/Accepted: 24. 7. 2017
MUDr. Eva Kostolná
Klinika hepatogastroenterologie
Transplantcentrum, IKEM
Vídeňská 1958/9
140 21 Praha 4
eva.kostolna @ikem.cz
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Haq I, Tripathi D. Recent advances in the management of variceal bleeding. Gastroenterol Rep (Oxf) 2017; 5 (2): 113–126. doi: 10.1093/gastro/gox007.
2. de Franchis R. Baveno VI Faculty. Expanding consensus in portal hypertension: report of the Baveno VI Consensus Worshop: stratifying risk and individualizing care for portal hypertension. J Hepatol 2015; 63 (3): 743–752. doi: 10.1016/j.jhep.2015.05.022.
3. Krajina A, Hulek P, Fejfar T et al. Quality improvement guidelines for Transjugular Intrahepatic Portosystemic Shunt (TIPS). Cardiovasc Intervent Radiol 2012; 35 (6): 1295–1300. doi: 10.1007/ s00270-012-0493-y.
4. Boyer TD, Haskal ZJ, American Association for the Study of Liver Diseases. The Role of Transjugular Intrahepatic Portosystemic Shunt (TIPS) in the Management of Portal Hypertension: update 2009. Hepatology 2010; 51 (1): 306. doi: 10.1002/hep.23383.
5. Escorsell À, Pavel O, Cárdenas A et al. Esophageal balloon tamponade versus esophageal stent in controlling acute refractory variceal bleeding: a multicentre randomized, controlled trial. Hepatology 2016; 63 (6): 1957–1967. doi: 10.1002/hep.28360.
6. Bañares R, Albillos A, Rincón D et al. Endoscopic treatment versus endoscopic plus pharmacologic treatment for acute variceal bleeding: a meta-analysis. Hepatology 2002; 35 (3): 609–615.
7. Fejfar T, Safka V, Jirkovsky V et al. Danišův jícnový stent v terapii varikózního krvácení. Gastroent Hepatol 2013; 67 (2): 98–103.
8. Fejfar T, Vaňásek T, Brůha R et al. Léčba krvácení v důsledku portální hypertenze při jaterní cirhóze – aktualizace doporučených postupů ČHS ČLS JEP. Gastroent Hepatol 2017; 71 (2): 105–116. doi: 10.14735/amgh2017105.
9. Marot A, Trépo E, Doerig C et al. Systematic review with meta-analysis: self-expanding metal stents in patients with cirrhosis and severe or refractory oesophageal variceal bleeding. Aliment Pharmacol Ther 2015; 42 (11–12): 1250–1260. doi: 10.1111/apt.13424.
10. Drastich P, Brezina J, Sperl J et al. Treatment of uncontrollable acute variceal bleeding with self-expanding metal stent: a single center experience. Gastroenterology 2016; 150 (4 Suppl 1): S339. Abstract Sa1600. doi: 10.1016/S0016-508 5 (16) 31190-8.
11. Dechêne A, El Fouly AH, Bechmann LP et al. Acute management of refractory variceal bleeding in liver cirrhosis by self-expanding metal stents. Digestion 2012; 85 (3): 185–191. doi: 10.1159/000335 081.
12. Holster IL, Kuipers EJ, van Buuren HR et al. Self-expandable metal stents as definitive treatment for esophageal variceal bleeding. Endoscopy 2013; 45 (6): 485–488. doi: 10.1055/s-0032-1326227.
13. Hubmann R, Bodlaj G, Czompo M et al. The use of self-expanding metal stents to treat acute esophageal variceal bleeding. Endoscopy 2006; 38 (9): 896–901.
14. Müller M, Seufferlein T, Perkhofer L et al. Self-expandable metal stents for persisting esophageal variceal bleeding after band ligation or injection-therapy: a retrospective study. PLoS One 2015; 10 (6): e0126525. doi: 10.1371/journal.pone.0126525.