Extraezofageální a gastroezofageální reflux – vztah k astma bronchiale
Lucie Heribanová1
+ Pracoviště
Souhrn
Koincidence astma bronchiale a patologického gastroezofageálního nebo extraezofageálního refluxu je častá, tyto choroby se často různými mechanizmy vzájemně negativně ovlivňují. Klinické projevy patologického gastroezofageálního a extraezofageálního refluxu mohou astma imitovat nebo ovlivnit hodnocení kontroly astmatu. Uplatňuje se zde vagově zprostředkovaný reflex, nárůst bronchiální hyperreaktivity, mikroaspirace a změny v imunitní odpovědi. Naopak v důsledku bronchiální obstrukce dochází k progresi negativity pleurálního tlaku a narůstá thorakoabdominální gradient. Systémové kortikosteroidy, užívané v terapii těžkého astmatu, mají negativní vliv na reflux, u ostatních antiastmatik je tento nepříznivý vliv sporný. Každý astmatik by měl být dotazován na přítomnost symptomů refluxu, i když si, bohužel, řada z nich obtíže neuvědomuje. V diagnostice refluxní choroby jícnu i extraezofageálního refluxu je možné využít ezofagogastroduodenoskopii, 24hodinovou dvoukanálovou pH-metrii, typické známky refluxu je možné zjistit laryngoskopií i bronchoskopií. Méně běžnými testy je měření pH v oblasti orofaryngu a Peptest. Možné je i provedení diagnosticko-terapeutického testu. Základem terapie, vedle režimových a dietních opatření, jsou inhibitory protonové pumpy, vhodná jsou prokinetika, především u extraezofageálního refluxu. Léčba refluxu pozitivně ovlivňuje kontrolu astmatu.
Klíčová slova
astma bronchiale, extraezofageální reflux, gastroezofageální refluxÚvod
Astma bronchiale je heterogenní onemocnění charakterizované chronickým zánětem a remodelací průdušek spojené s jejich hyperreaktivitou a variabilní, často reverzibilní obstrukcí. Projevuje se opakovanými stavy hvízdavého dýchání, kašlem, dušností a svíráním na hrudi [1]. Patologický gastroezofageální reflux (GER) je jedním z onemocnění, která mohou průběh astma bronchiale zhoršovat [2].
GER je zpětný tok žaludečního obsahu ze žaludku do jícnu, který může, ale nemusí být patologický. Patologický GER opět nemusí vždy způsobovat jakékoli patologické změny nebo symptomy. Pokud GER působí obtíže nebo komplikace, označujeme tento stav refluxní choroba jícnu (RCHJ) [3]. Pod označení GER je někdy nesprávně zahrnován i reflux extraezofageální (EER). Jedná se o stav, kdy dochází k průniku (duodeno) gastrického obsahu nad úroveň horního jícnového svěrače. Pokud EER působí obtíže a/nebo komplikace v laryngu, faryngu, respiračním traktu a ústní dutině, jedná se o extraezofageální refluxní chorobu (EERCH). K poškození sliznice laryngu vedou již tři refluxní epizody za 24 hod, 50 jícnových refluxních epizod je horní hranice normy [4,5]. Extraezofageální projevy (kašel, bronchospazmus) může mít ale i RCHJ bez EER [3,4].
EERCH a RCHJ jsou tedy dvě samostatné klinické jednotky, které se mohou vyskytovat buď samostatně, nebo současně [4]. V souvislosti s astma bronchiale má větší význam EER než ER.
Prevalence RCHJ v Evropě se podle dostupných studií odhaduje na 8,8–25,9 % a její výskyt pravděpodobně narůstá [6], prevalence EERCH známá není [4]. Prevalence astma bronchiale se v naší republice pohybuje okolo 8 % [7]. RCHJ pravděpodobně postihuje 38–80 % pacientů s astmatem [2].
Etiopatogeneze RCHJ a EERCH, vliv na astma bronchiale
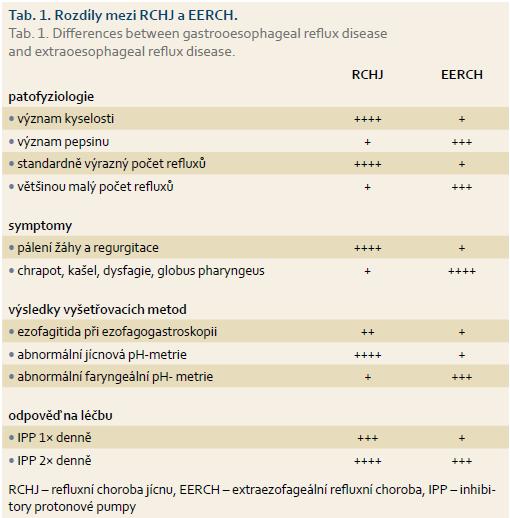
Etiopatogeneze RCHJ i související EERCH je multifaktoriální. Uplatňuje se zde především snížení tonu dolního jícnového svěrače, resp. horního jícnového svěrače u EERCH, dysmotilita jícnu a žaludku. Mohou se uplatnit i různě změněné anatomické poměry (např. hiátová hernie) a zevní vlivy (léky, některé potraviny a nápoje, nikotinizmus apod.). Zejména u EECHR je důležité složení refluxátu, kde se vedle kyseliny chlorovodíkové uplatňuje i pepsin, soli žlučových kyselin a pankreatické enzymy a délka jeho působení na sliznice. Sliznice extraezofageální oblasti (horních i dolních dýchacích cest) je na refluxát mnohem citlivější než sliznice jícnu, více se zde uplatňuje toxický synergizmus pepsinu, kyseliny chlorovodíkové a duodenálního obsahu a negativně zde působí i slabě kyselé refluxní epizody [3–5,8,9]. Rozdíly mezi RCHJ a EERCH shrnuje tab. 1 [9].
Jedním z mechanizmů možného působení GER na dolní dýchací cesty je vagově zprostředkovaný ezofagobronchiální reflex. Podráždění aferentních vláken nervus vagus v jícnu refluxátem může vést u některých osob k bronchospazmu a záchvatu kašle. Výsledky studií, které se zabývaly okamžitou reakcí plicních funkcí na přítomnost kyseliny v jícnu, však nejsou jednoznačné [10,11]. Významný je průkaz zvýšení bronchiální reaktivity na metacholin po vystavení jícnu působení kyseliny [12]. Bronchiální hyperreaktivita je jedním ze základních rysů astma bronchiale a právě zvýšení reaktivity na nespecifické bronchokonstrikční podněty značně ovlivňuje stupeň a úroveň kontroly astma bronchiale. Cestou vagových reflexů akutně působí i EER, kdy podráždění dýchacích cest (především distální části laryngu) refluxátem může vést k laryngospazmu, bronchospazmu nebo záchvatu dráždivého kašle [10,13].
Opakované mikroaspirace duodenogastrického obsahu vyvolávají chronický chemický zánět sliznice především horních dýchacích cest a snižují i lokální imunitu. EER může vést ke vzniku např. chronické rinitidy, refluxní laryngitidy, dysfunkce hlasových vazů, chronické laryngotracheitidy, ale i subglotické a laryngeální stenózy, recidivujících bronchopneumonií, nebo se podílet na vzniku bronchiektázií [4,10,13,14]. Z hlediska astmatu může v důsledku chronického zánětu dýchacích cest docházet ke zvýšení bronchiální hyperreaktivity [13], ale symptomy výše uvedených změn mohou být také mylně považovány za projevy zhoršené kontroly astma bronchiale a v krajním případě vést i ke zbytečné dlouhodobé systémové kortikoterapii. Další souvislost mezi astmatem a patologickým GER i EER představuje možnost vlivu refluxu na navození nebo posílení Th2 imunitní odpovědi [15–17].
Astma bronchiale také může naopak negativně ovlivňovat RCHJ. Jedním z faktorů je nárůst negativity pleurálního tlaku při progresi bronchiální obstrukce, který zvyšuje torakoabdominální gradient. Plicní hyperinflace v důsledku air-trappingu vede k oploštění bránice, a tím přispívá k narušení antirefluxní bariéry. Také chronický kašel, který je jedním z častých příznaků astmatu, ovlivňuje reflux podobným mechanizmem [10,13,18].
Sporná je otázka nepříznivého vlivu antiastmatik na GER. Teofyliny mají pravděpodobně klinicky významný vliv na snížení tonu dolního jícnového svěrače jen při dosažení vysokých plazmatických koncentrací [19]. β-2-mimetika také mohou snížit tonus dolního jícnového svěrače [20], na druhou stranu jejich bronchodilatační působení může v důsledku normalizace pleurálního tlaku působit na reflux i příznivě [13,21]. Negativní vliv na RCHJ mají systémové kortikosteroidy [2,22].
Diagnostika
Problémem při diagnostice RCHJ i EERCH jsou nespecifické projevy, navíc tíže onemocnění nemusí korelovat s tíží příznaků [4,14].
Anamnéza
Nepřítomnost klasických příznaků – pyrózy a regurgitace – RCHJ nevylučuje, u pacientů s EER se tyto příznaky objevují dokonce jen u 5–15 % pacientů. Jednou skupinou příznaků (jak v rámci extraezofageálních projevů RCHJ, tak při EER) jsou chronický kašel, zahlenění, chrapot nebo pocit cizího tělesa v krku (globus faryngeus). Může se objevit i zvýšená kazivost zubů nebo zápach z úst. Dalšími projevy, které vedou pacienta nejčastěji primárně do pneumologické ambulance, jsou záchvatovitý suchý kašel a opakující se záchvatovitá dušnost v důsledku laryngospazmu nebo bronchospazmu [3,4,14,23].
Z důvodu časté koincidence a vzájemného negativního ovlivňování RCHJ (resp. EERCH) a astma bronchiale bychom se každého pacienta s diagnostikovaným astmatem i vyšetřovaného pro možné astma měli v rámci odběru anamnézy aktivně ptát na příznaky refluxu – především na výskyt zhoršování symptomů astmatu v souvislosti s jídlem, polohou těla (vleže, v předklonu), ve spánku a v návaznosti na pyrózu. Důležitý je i údaj o chronickém nebo opakovaném chrapotu [2]. Zvýšenou pozornost z hlediska možné přítomnosti RCHJ nebo EER je vhodné věnovat pacientům s noneozinofilním astmatem se začátkem v dospělosti, u astmatiků nereagujících dostatečně na běžnou léčbu, při atypických symptomech astmatu (např. je-li převažujícím symptomem kašel), ale i u nejasného zhoršení kontroly onemocnění u pacientů s eozinofilním astmatem [2,10,24].
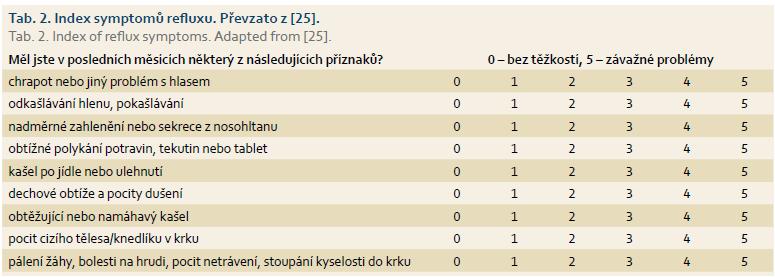
Užitečný při odběru anamnézy může být dotazník Indexu symptomů refluxu podle Belafskyho. Pokud je součet bodového ohodnocení jednotlivých položek vyšší než 13, je vysoká pravděpodobnost přítomnosti patologického EER (tab. 2) [25].
Vyšetřovací metody
V diagnostice RCHJ i EERCH je možné využít řadu vyšetření. Posloupnost vyšetření závisí na charakteru a závažnosti obtíží pacienta.
Ezofagogastroduodenoskopie doplněná o histologické vyšetření biopsie jícnu by měla být provedena u pacientů s déletrvajícími nebo varovnými příznaky RCHJ (dysfagie, odynofagie, hubnutí, anémie, hemateméza, meléna) a u pacientů dostatečně nereagujících na léčbu. Není však nezbytné ji provádět u všech pacientů se suspektní EERCH. K průkazu kyselých extraezofageálních refluxních epizod se využívá 24hodinová dvoukanálová pH-metrie, kdy je jeden ze senzorů sondy umístěn nad horní jícnový svěrač. Má však své limity v průkazu málo kyselých refluxních epizod, kde se lépe uplatní 24hodinová impedance a pH-metrie umožňující monitorovat i oblast horního jícnového svěrače a hodnotit charakter refluxátu z hlediska plynného obsahu. Manometrie se uplatní v hodnocení motility jícnu (RCHJ). Při laryngoskopii svědčí pro EERCH obraz refluxní laryngitidy – hypertrofie nebo zarudnutí zadní komisury, zarudnutí arytenoidních výběžků, difuzní otok hrtanu, pseudoulcus, poruchy kmitání hlasivek a jejich granulomy [3,4,14]. Bronchoskopie má z hlediska refluxu význam spíše při diferenciálně-diagnostickém vyšetřování pacientů s obtížně léčitelným astmatem nebo chro- nickým kašlem, nicméně vedle již uve- dených změn v oblasti laryngu může být při EERCH zjištěna i tracheální stenóza nebo zánětlivé změny tracheobronchiální sliznice. Nespecifickým mar- kerem aspirace je přítomnost zvýšeného počtu lipofágů v tekutině získané bronchoalveolární laváží [4,26]. Dalšími méně běžnými testy je měření pH v oblasti orofaryngu (bez nutnosti zavádění katetru do jícnu) a detekce pepsinu (Peptest) ve slinách sputu nebo středoušní tekutině. Svůj význam může mít i rentgenové vyšetření polykacího aktu [4,14]. Diagnosticko-terapeutický test s inhibitory protonové pumpy (IPP) má poměrně nízkou specifitu a musí mu předcházet pečlivé zhodnocení anamnézy [4,9,27]. IPP je doporučeno podávat 2× denně v dostatečné dávce (lansoprazol 30 mg, omeprazol 20 mg, pantoprazol 40 mg). Zhodnocení efektu u RCHJ je možné už po jednom týdnu, u EERCH je vzhledem k větší citlivosti sliznic hypofaryngu a horních dýchacích cest k refluxátu hodnocení efektu vhodné až po šesti týdnech [3,4,9].
Terapie
Léčba RCHJ i EERCH zahrnuje režimová a dietní opatření, farmakoterapii a chirurgickou léčbu.
Režimová a dietní opatření
Důležitou součástí léčby RCHJ i EERCH jsou režimová a dietní opatření. Pa- cient by měl omezit příjem potravin a nápojů, které snižují tonus dolního jícnového svěrače, prodlužují evakuaci žaludku, zvyšují žaludeční sekreci nebo vyvolávají u pacienta subjektivní obtíže (např. káva a jiné kofeinové nápoje, alkohol, kynuté pečivo, čokoláda, cibule, česnek, ostrá kořeněná jídla apod.). Vhodné je jíst často a v malých dávkách, nevhodné je jíst hlavní velké jídlo večer před ulehnutím. Z režimových opatření má význam omezení aktivit, které vedou ke zvýšení nitrobřišního tlaku (práce v předklonu, některá cvičení), a to zejména do 2–3 hod po jídle, vhodné je doporučit redukci hmotnosti a zákaz kouření, při převažujících nočních obtížích spát se zvýšenou horní polovinou těla [3,4,10,28].
Inhibitory protonové pumpy
IPP jsou základem léčby RCHJ i EERCH [3,4], i když u pacientů s převažujícím EER s větším podílem nekyselých nebo slabě kyselých refluxních epizod může být efekt méně výrazný [29]. Vzhledem k nutnosti pravidelné a dlouhodobé léčby (3–6 měsíců) bývá problémem nedostatečná compliance. Celková doba léčby je individuální. Zahájení podávání IPP bez potvrzení diagnózy RCHJ nebo EERCH některým z výše uvedených invazivních vyšetření je možné u pacientů mladších 45 let s epizodickými obtížemi bez varovných příznaků [3,4,28]. V několika studiích byl prokázán příznivý efekt IPP na kontrolu astmatu (zejména redukcí nočních obtíží), plicní funkce i bronchiální hyperreaktivitu u pacientů s koincidencí astma bronchiale a patologického refluxu [30–32].
Kompetitivní blokátory histaminových receptorů 2
Kompetitivní blokátory histaminových receptorů 2 mají menší účinnost než IPP, je ale možné tyto léky kombinovat u refrakterních obtíží [28]. U pacientů s astmatem a RCHJ byl pozorován jen malý účinek ranitidinu na noční příznaky astmatu a žádný signifikantní vliv na plicní funkce [10].
Antacida
Antacida (hydroxid aluminia a magnézia, bikarbonát a citrát sodný) je možné použít jen ke krátkodobé symptomatické úlevě [28]. U pacientů s EERCH může mít příznivý účinek suspenze bikarbonátu s alginátem z důvodu vazby pepsinu a žlučových kyselin, je možné je kombinovat s IPP [4,33].
Prokinetika
Prokinetika zvýšením tonu dolního jícnového svěrače a stimulací motility trávicího traktu prográdním směrem snižují počet refluxních epizod, jejich přidání k terapii IPP je vhodné především u mimojícnových projevů refluxu [4,14,28]. Chirurgická léčba, tedy laparoskopická fundoplikace, je krajním řešením po vyčerpání konzervativních možností léčby [4].
Závěr
Aktivní přístup k diagnostice EERCH a RCHJ a správná léčba může u pacientů s astmatem zabránit zbytečnému navyšování antiastmatické terapie a významně přispět ke zlepšení kontroly zejména u pacientů s obtížně léčitelným astma bronchiale. Poznání vztahů mezi astma bronchiale a refluxu na úrovni ovlivnění imunitní odpovědi může přinést nový pohled na tato onemocnění. Mezioborová spolupráce je zde nezbytná.
Použité zkratky
GER – gastroezofageální reflux
RCHJ – refluxní choroba jícnu
EER – extraezofageální reflux
EERCH – extraezofageální refluxní choroba
IPP – inhibitory protonové pumpy
Autorka deklaruje, že v souvislosti s předmětem studie nemá žádné komerční zájmy.
The author declares she has no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Doručeno/Submitted: 5. 9. 2016
Přijato/Accepted: 3. 10. 2016
MUDr. Lucie Heribanová
Pneumologická klinika
1. LF UK a Thomayerovy nemocnice
Vídeňská 800
140 59 Praha 4
lucie.heribanova@ftn.cz

Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Teřl M, Čáp P, Dvořáková R et al. Doporučený postup diagnostiky a léčby bronchiálního astmatu. 1. vyd. Semily: GEUM 2015: 5–48.
2. Sedlák V, Chlumský J, Teřl M et al. Doporučený postup diagnostiky a léčby obtížně léčitelného bronchiálního astmatu 2011. [online]. Dostupné z: www.pneumologie.cz/guidelines/.
3. Lukáš K, Bureš J, Drahoňovský V. Refluxní choroba jícnu. Standardy České gastroenterologické společnosti – aktualizace 2009. Vnitr Lek 2009; 55 (10): 967–975.
4. Brandtl P, Lukáš K, Turzíková J. et al. Extraezofageální refluxní choroba – mezioborový konsenzus. Časopis lékařů českých 2011; 150 (9): 513–518.
5. Koufman JA. Laryngopharyngeal reflux is different from classic gastroesophageal reflux disease. Ear Nose Throat J 2002; 81 (9 Suppl 2): 7–9.
6. El-Serag HB, Sweet S, Winchester CC et al. Update on the epidemiology of gastrooesophageal reflux disease: a systematic review. Gut 2014; 63 (6): 871–880. doi: 10.1136/gutjnl-2012-304269.
7. Kašák V. Asthma bronchiale. In: Kolek V et al. Pneumologie. Praha: Maxdorf 2011: 149.
8. Ford CN. Evaluation and management of laryngopharyngeal reflux. JAMA 2005; 294 (12): 1534–1540.
9. Zeleník K, Komínek P, Chlumský J. Příručka pro praxi: Extraezofageální reflux. 1. vyd. Praha: Merck 2013: 4.
10. Issac M. The relationship between GERD and asthma. US Pharmacist 2009; 34 (7): 30–35.
11. Field SK. A critical review of the studies of the effects of simulated or real gastroesophageal reflux on pulmonary function in asthmatic adults. Chest 1999; 115 (3): 848–856.
12. Herve P, Denjean A, Jian R et al. Intraesophageal perfusion of acid increases the bronchomotor response to methacholine and to isocapnic hyperventilation in asthmatic subjects. Am Rev Respir Dis 1986; 134 (5): 986–989.
13. Dal Negro RW, Aubier M. Bronchial asthma and gastro-oesophageal reflux. In: Chung F, Fabbri LM. Asthma. Sheffield: ERS Journals 2003: 260–277.
14. Zeleník K, Komínek P. Extraezofageální reflux. Remedia 2010; 20: 398–401.
15. Kohata Y, Fujiwara Y, Machida H et al. Role of Th-2 cytokines in the development of Barrett’s esophagus in rats. J Gastroenterol 2011; 46 (7): 883–893. doi: 10.1007/s00535-011-0405-y.
16. Barbas AS, Downing TE, Balsara HE. Chronic aspiration shifts the immune response from Th1 to Th2 in a murine model of asthma. Eur J Clin Invest 2008; 38 (8): 596–602. doi: 10.1111/j.1365-2362.2008.01976.x.
17. Isomoto H, Nishi Y, Kanazawa Y et al. Immune and inflammatory responses in GERD and lansoprazole. J Clin Biochem Nutr 2007; 41 (2): 84–91. doi: 10.3164/jcbn. 2007012.
18. Zerbib F, Guisset O, Lamouliatte H et al. Effects of bronchial obstruction on lower esophageal sphincter motility and gastroesophageal reflux in patients with asthma. Am J Respir Crit Care Med 2002; 166 (9): 1206–1211.
19. Pomari C, Micheletto C, Turco P et al. Does i.v. theophylline increase gastro-esophageal reflux (GER) ? Am J Respir Crit CareMed 1997; 155 (4): 967.
20. Crowell MD, Zayat EN, Lacy BE et al. The effects of an inhaled beta2-adrenergic agonist on lower esophageal function: a dose-response study. Chest 2001; 120 (4): 1184–1189.
21. Pomari C, Michelleto C, Tognella S et al. Salbutamol MDI does not affect gastro-esophagel reflux. Am J Respir Crit CareMed 1997; 155 (4): 967.
22. Lazenby JP, Guzzo MR, Harding SM et al. Oral cortico steroids increase esophageal acid contact times in patients with stable asthma. Chest 2002; 121 (2): 625–634.
23. Sataloff R, Castell D, Katz P et al. Reflux laryngitis and related disorders. 3rd ed. San Diego: Plural Publishing 2005: 171.
24. Richter JE. Gastroesophageal reflux disease and asthma: the two are directly related. Am J Med 2000; 108 (Suppl 4a): 153S–158S.
25. Belafsky CP, Postma GN, Koufman JM. The validity and reliability of the reflux finding score. Laryngoscope 2001; 111 (8): 1313–1317.
26. Sweet MP, Patti MG, Hoopes C et al. Gastrooesophageal reflux and aspiration in patients with advanced lung dis- ease. Thorax 2009; 64 (2): 167–173. doi: 10.1136/thx.2007.082719.
27. Vaezi MF. Extraesophageal manifestations of gastroesophageal reflux disease. Clin Cornerstone 2003; 5 (4): 32–38.
28. Kroupa R, Ječmenová M, Dolina J. Terapie refluxní nemoci jícnu. Postgraduální medicína. Praha: Mladá fronta 2013; 15 (4): 435–439.
29. Galmiche JP. Non-erosive reflux disease and atypical gastrooesophageal reflux disease manifestations: treatment results. Drugs 2006; 66 (Suppl 1): 7–13.
30. Kiljander TO, Salomaa ER, Hietanen EK et al. Gastroesophageal reflux in asthmatics: a double-blind, placebo-controlled crossover study with omeprazole. Chest 1999; 116 (5): 1257–1264.
31. Dal Negro R, Pomari C, Micheletto C et al. Omeprazole (OM), but not placebo (P), reduces the bronchiale response to methacholine (MCH) in mild non-atopic asthmatics with gastroesophageal reflux (GER). Am J Respir Crit Care Med 1996; 153 (4): A517.
32. Harding SM. Gastroesophageal reflux and asthma: insight into the association. J Allergy Clin Immunol 1999; 104 (2 Pt 1): 251–259.
33. Belafsky CP, Postma GN, Amin RM et al. Symptoms and findings of laryngopharyngeal reflux. Ear, Nose & Throat Journal 2002; 81 (9): 10–13.