Dysfunkce dolní části gastrointestinálního traktu u kriticky nemocných – současný pohled
Karel Balihar Orcid.org 1, Jana Koželuhová Orcid.org 2, Lucie Fremundová Orcid.org 3, Martin Matějovič Orcid.org 4
+ Pracoviště
Souhrn
Akutní gastrointestinální dysfunkce (acute gastrointestinal injury – AGI) je jeden z velmi častých a v klinické praxi klíčových aspektů syndromu multiorgánové dysfunkce u kriticky nemocných. Její výskyt je spojen s vyšší morbiditou a mortalitou. V dolní části gastrointestinálního traktu (GIT) má velmi různorodé projevy a důsledky. Jde o komplex: 1. snížené absorpce základních živin a stopových prvků; 2. narušení střevní hybnosti dále komplikující příjem živin a defekaci; 3. významné změny fekálního mikrobiomu a bariérové funkce střeva se zvýšenou střevní permeabilitou a rizikem endotoxemie; 4. v neposlední řadě velmi významným akcelerátorem AGI je přítomnost intraabdominální hypertenze. Na rozdíl od jiných orgánových systémů neexistuje univerzální biomarker AGI. K diagnostice AGI v dolní části GIT máme v běžné praxi především informace z klinického vyšetření GIT a vitálních funkcí, neopomenutelným přínosem je možnost monitorace intraabdominálního tlaku. Z laboratorních markerů se jeví slibným vyšetření plazmatického citrulinu a proteinů mezibuněčných spojení (tight junction). Bohužel většina dalších diagnostických metod je využitelná jen v rámci klinických studií, protože provádění v podmínkách intenzivní péče je komplikované. Terapeuticky kromě rutinní podpůrné a cílené terapie kritického stavu je v ovlivnění AGI kladen důraz na 1. zajištění adekvátní výživy a střevní hybnosti; 2. zamezení bakteriálního přerůstání a udržení integrity fekálního mikrobiomu; 3. konzervativními opatřeními, event. chirurgickou dekompresí korigovat intraabdominální hypertenzi. Časné rozpoznání a terapie AGI vede ke snížení morbidity a v některých aspektech i mortality kriticky nemocných.
Klíčová slova
gastrointestinální trakt, intestinální motilita, intraabdominální hypertenze, kriticky nemocný, microbiomÚvod
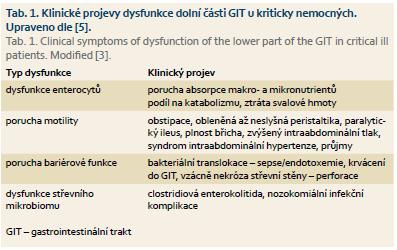
Tento článek navazuje na předchozí pojednání o dysfunkci horní části gastrointestinálního traktu (GIT) a podává souhrnný pohled na problematiku dysfunkce dolní části GIT u kriticky nemocného pacienta [1]. Dolní částí GIT dle oficiální terminologie rozumíme tenké střevo od ligamentum Treitzi po anus [2]. Toto dělení shledáváme jako praktické, protože klinické symptomy vycházející z horní a dolní části GIT jsou odlišné a vyžadují jiný přístup. Kritický stav je definován jako velmi heterogenní skupina nemocí a stavů, pro které je charakteristické riziko nebo rozvoj orgánové dysfunkce, dlouhodobá morbidita a vysoká mortalita. Všechny kritické stavy v rozvinuté formě přechází do syndromu multiorgánové dysfunkce (MODS), který je definován jako přítomnost víceorgánové dysfunkce u akutně nemocného pacienta, kdy homeostázy nelze dosáhnout bez intervence [3]. GIT hraje klíčovou roli u kriticky nemocných a narušení jeho komplexních fyziologických funkcí (digesce, absorpce, hybnost, bariérová funkce, imunitní a endokrinní funkce) kritickým stavem je považováno za ohnisko, které je motorem rozvoje MODS [4]. Dysfunkce GIT v rámci MODS je dle nové terminologie nazývána akutní gastrointestinální dysfunkcí (acute gastrointestinal injury – AGI) [5]. AGI se u kriticky nemocného v dolní části GIT projevuje velmi různorodými symptomy spojenými se sníženou absorpcí základních živin, s porušenou střevní motilitou (od průjmů přes obstipaci až po ileus), patologicky změněnou kolonickou mikroflórou, sníženou integritou střevní stěny (ischemie, bakteriální translokace, krvácení do střev, nekróza střevní stěny, vzácně až perforace) a syndromem intraabdominální hypertenze (IAH) (tab. 1) [5]. AGI je přítomna u více než poloviny kriticky nemocných a zvyšující se počet přítomných gastrointestinálních symptomů exponenciálně koreluje s nemocniční mortalitou nemocných [6]. Přestože důležitost dysfunkce GIT při rozvoji MODS je známa již více než 20 let a v posledních letech je toto téma intenzivně studováno, stále nejsou k dispozici kvalitní klinické a laboratorní nástroje ke kvantifikaci, cílené monitoraci a léčbě AGI [7]. Článek shrnuje aktuální poznatky, koncepty, diagnostické a terapeutické možnosti tohoto důležitého gastroenterologického aspektu intenzivní medicíny.Absorpce nutrientů a stopové prvky u kriticky nemocných
Naše znalosti ohledně absorpce základních živin a stopových prvků v kritickém stavu jsou velmi omezené. Je známo, že u kriticky nemocných je narušena absorpce glukózy i lipidů z tenkého střeva [8,9]. Absorpce sacharidů je snížena bez ohledu na stupeň gastroparézy, což poukazuje na účast faktorů spojených s funkcí tenkého střeva. Jednou z okolností může být narušený mezenteriální průtok, který koreluje se stupněm snížení absorpční kapacity [10]. Z experimentálních studií lze usuzovat, že klíčovým problémem bude dysfunkce enterocytů. Pro jejich výživu je kromě dostatečné tkáňové perfuze důležitá i přítomnost intraluminálních nutrientů k jejich výživě. Ve studii srovnávající časnou enterální výživu a výživu podanou se čtyřdenním zpožděním byla zjištěna významně zhoršená absorpce glukózy u pacientů s později zahájenou enterální výživou [11]. Z tohoto pohledu je pro obnovu funkce enterocytů nejpodstatnější oběhová stabilizace, dobrá splanchnická oxygenace a časná enterální výživa.Problematika dodávky živin při dysfunkci horní části GIT byla diskutována v předchozím souhrnném článku [1]. Dysfunkce dolní části GIT je obtížnějším problémem. V praxi narážíme obvykle na dvě hraniční situace, a to 1. střevní paralýza se stázou střevního obsahu a 2. urychlená pasáž stolice při průjmech. V obou situacích při zajištěné dodávce enterální výživy není jisté, kolik se z podané výživy vstřebá. V této situaci je vhodným pomocníkem nepřímá kalorimetrie, která určí skutečné energetické potřeby pacienta, umožní optimalizovat energetický příjem a vyhnout se překrmování či nedostatečné dodávce výživy se všemi negativními klinickými důsledky. Tato metoda však není rutinně dostupná a využívaná na všech JIP. Zhruba u 10–30 % kriticky nemocných se nedaří v důsledku GIT dysfunkce dodávku živin zajistit enterálně a jsou indikováni k totální či doplňkové parenterální výživě.
Absorpce mikronutrientů u kriticky nemocných je komplikované a široké téma přesahující rámec tohoto sdělení. Pro přiblížení této problematiky možno obecně zmínit, že snížené hladiny stopových prvků a vitaminů u kriticky nemocných jsou pouze parciálně odrazem porušené absorpce. Velký podíl na snížených hladinách mikronutrientů v krvi má zvýšená konsumpce při šoku, snížené hladiny proteinových nosičů a redistribuce do třetího prostoru. Všeobecně suplementace těchto prvků je doporučena dle klinického zvážení hlavně u pacientů s popáleninami, polytraumatem a nebo při nutnosti kontinuální hemodialýzy, kde je rozvoj klinicky významného deficitu vyšší. Suplementace má být podávána parenterálně, lépe v kontinuální infuzi, aby byla dodávka nutrientů do organizmu efektivní [12].
Motilita tenkého a tlustého střeva u kriticky nemocných
Asi polovina ventilovaných kriticky nemocných vykazuje známky porušené intestinální motility. U většiny pacientů se poruchy motility manifestují jako neefektivní či zpomalená peristaltika, paralýza a obstipace (až 83 % kriticky nemocných), o něco méně častěji jako hypermotilita klinicky projevená průjmovitými stolicemi. Důsledkem snížené hybnosti tlustého střeva je delší doba umělé ventilace a protrahovanější hospitalizace oproti pacientům, kteří tuto poruchu nevyvinou [13]. Patofyziologie je velmi komplexní, neboť vlivů, které se na dysfunkci podílí, je velmi mnoho. Hlavní význam má pravděpodobně systémová zánětlivá odpověď, sepse, systémová či regionální hypoxemie a hypoperfuze, ale podílí se i elektrolytové dysbalance, poruchy glukózového metabolizmu, acidobazické rovnováhy, změny hydratace a nelze opomenout ani vliv abdominální chirurgie či poškození centrální nervové soustavy [14]. Celá řada bioaktivních substancí a mediátorů vyplavených v reakci na fyzický stres jako kortikotropin stimulující faktor, katecholaminy, serotonin a nebo oxid dusnatý podporuje zpomalení a dysfunkci střevní motility. V neposlední řadě množství farmak nezbytných k léčbě kriticky nemocných jako anestetika, sedativa, opiáty, katecholaminy, agonisté alfa adrenergních receptorů (clonidin či dexmedetomidin) zhoršuje střevní hybnost. Tranzit tenkým střevem u ventilovaných kriticky nemocných měřený kapslovou endoskopií je asi dvakrát pomalejší než u zdravých jedinců a tranzit tlustým střevem je pomalejší přibližně desetkrát s velkými individuálními rozdíly [15]. Kvalitativně je v tenkém střevě častější retrográdní aktivita a zpomalená peristaltika a tlusté střevo má výrazně snížený počet i intenzitu kontrakcí.V hodnocení klinické významnosti střevní dysmotility je třeba mít na paměti, že v běžné populaci u jinak zdravých jedinců je střevní hybnost velmi varibilní, od 2–3 stolic denně až po jednu stolici za 3–4 dny [16]. Intenzivista obvykle nezná, jaká byla střevní hybnost v předchorobí u svého pacienta. Pacienti, kteří trpí chronickými interními či neurologickými onemocněními, jako např. Parkinsonským syndromem, různými neuropatiemi, diabetes mellitus, funkční dyspepsií, tyreopatií, některými systémovými autoimunitami aj., mají vyšší riziko, že rozvinou významnou poruchu hybnosti. Hraje také roli, zda pacient užíval v předchorobí chronicky laxativa. Svou roli pravděpodobně hraje i nikotinizmus a abúzus alkoholu v anamnéze. Alkohol zpomaluje hybnost tenkého střeva a nikotin stimuluje evakuaci rekta a esovité kličky [17].
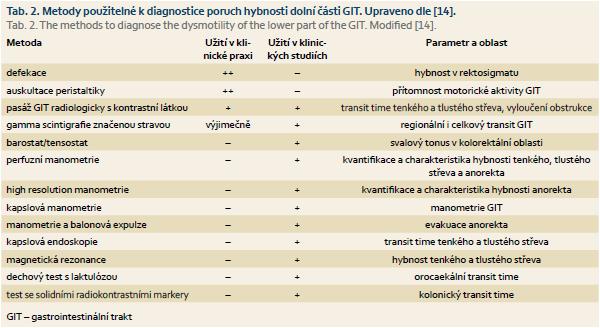
Nevyřešeným denním problémem v intenzivní péči je diagnostika a kvantifikace dysmotility. Přítomnost defekace je hrubým, ale jasným indikátorem propulzivní funkce rekta a esovité kličky. Auskultace peristaltiky je v praxi často prováděna, ale je obtížně interpretovatelná. Často není zřejmé, zda je neslyšná peristaltika problémem, který je třeba intervenovat, či naopak, zda slyšitelná peristaltika je či není propulzivní. Přehled současných metod použitelných k diagnostice poruch hybnosti tenkého a tlustého střeva, jejich užití v klinických studiích či v klinické praxi a parametry, které hodnotí, jsou obsaženy v tab. 2 [14]. Bohužel většina těchto metod není snadno proveditelná v podmínkách intenzivní péče.
Léčebné intervence intestinální dysmotility v naší praxi jsou dosud velmi omezené. Prakticky asi nejdůležitějším a nejdostupnějším opatřením je maximální redukce léků, které inhibují intestinální motilitu (viz výše). Uvážlivě restriktivní politika v užívání sedace a opiátů u kriticky nemocných a pravidelné denní přerušení analgosedace je spojeno s kratší délkou umělé plicní ventilace, délky hospitalizace, nižší morbiditou a mortalitou [18]. Další možností, jak podpořit intestinální motilitu, jsou laxativa, která zlepšují střevní hybnost obnovou vodní rovnováhy stolice. Nejčastěji užívaná laxativa jsou laktulóza a polyetylenglykol, lze však užít i laxativa stimulační [14]. Laktulóza oproti polyetylenglykolu je fermentabilní střevními bakteriemi, takže může za nepříznivých okolností vést k bakteriálnímu přerůstání, flatulenci a zvýšení intraabdominálního tlaku. V randomizované studii na 308 ventilovaných pacientech s oběhovou podporou prokázala laktulóza i polyetylenglykol srovnatelně vyšší efektivitu v navození defekace než placebo, přičemž časnější defekace byla spojena s kratší délkou hospitalizace bez vlivu na mortalitu pacientů [19].
Specifickou podskupinou kriticky nemocných se střevní hypomotilitou jsou pacienti s opiáty navozenou obstipací. Pokud jsou opiáty dominantním mechanizmem střevní hypomotility, lze ji zvrátit orální aplikací antagonisty opiátů. V ČR jsou k dispozici preparáty naloxon a naltrexon. Při orálním podání mají vzhledem k vysokému „first pass“ efektu v játrech velmi nízkou biologickou dostupnost (kolem 2 %) a nedochází k antagonizaci analgetického efektu opiátů ani vzniku abstinenčního syndromu, pokud není překročena kapacita jater pro jejich metabolizaci [20]. Existují i pilotní práce s jiným preparátem, metylnaltrexonem, který velmi omezeně prochází hematoencefalickou bariérou a při subkutánním nebo intravenózním podání má velmi příznivý efekt na obnovu střevní hybnosti u kriticky nemocných při zachovaném analgetickém efektu systémových opiátů. Pokud se tato data potvrdí ve větší randomizované studii, půjde o perspektivní, nicméně nákladnou možnost, jak ovlivnit obstipaci u této specifické subpopulace kriticky nemocných [21].
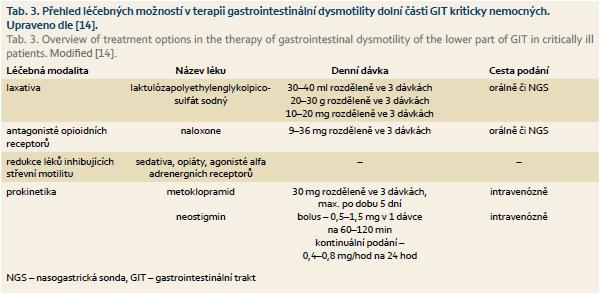
Jiným postupem, jak podpořit obleněnou střevní peristaltiku, je podání prokinetik. V ČR je řada preparátů nedostupných (např. erytromycin, ceruletide) nebo byly tyto preparáty staženy z trhu pro nežádoucí účinky (cisaprid). V intenzivní péči jsou ceněna prokinetika, která lze podat intravenózně. Perorální aplikace vzhledem k omezené absorpci z GIT jsou méně preferovaná. Tradičním a stále dostupným intravenózním preparátem je metoklopramid, antagonista dopaminových receptorů. Jeho prokinetický efekt je patrný především v horní části GIT a klinicky významný účinek na tlusté střevo není spolehlivě dokumentovaný. U kriticky nemocných má příznivý dopad na intestinální tranzit a zlepšuje toleranci enterální výživy, je‑li podán intravenózně, nikoli však při enterálním podání [22]. Neovlivňuje délku pooperačního ileu. Hlavní limitací užití metoklopramidu jsou jeho nežádoucí účinky. Na podkladě zprávy Státního ústavu pro kontrolu léčiv z 1. 8. 2013 je podání metoklopramidu limitováno pouze pro krátkodobé užití (do pěti dnů), neboť pak narůstá riziko extrapyramidových motorických reakcí [23]. Druhým a v podstatě již posledním prokinetikem, které lze aplikovat intravenózně a je běžně užívané v praxi, je neostigmin. Je to reverzibilní inhibitor acetylcholin‑esterázy s rychlým nástupem prokinetického účinku v řádu minut. Ve vyšší dávce zlepšuje hybnost tlustého střeva u postoperačního ilea, u postresekčních stavů na kolon a u syndromu intestinální pseudoobstrukce [24,25]. Mezi významné nežádoucí účinky neostigminu patří symptomatická bradykardie reverzibilní při podání atropinu a bronchiální a slinná hypersekrece. Nesmí být podán při intestinální obstrukci, koronární ischemii, srdečních arytmiích nebo při významné bronchiální spasticitě. Při renální dysfunkci je třeba dávku adekvátně redukovat. Souhrn přípravků uplatňujících se v terapii obleněné motility dolní části GIT u kriticky nemocných s dávkováním je zobrazen v tab. 3 [14].
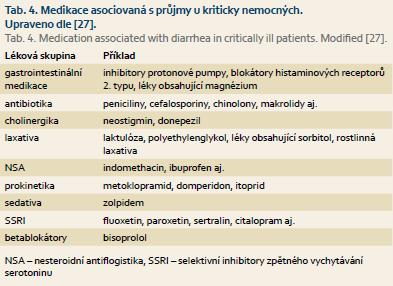
GIT dysfunkce manifestovaná průjmy postihuje až 68 % kriticky nemocných a většina průjmů je neinfekčního původu [26]. Nejčastějšími příčinami jsou podávaná medikace, změny v důsledku vlastního onemocnění, enterální výživa nebo nasedající infekce. Medikace je nejčastějším faktorem přispívajícím ke vzniku průjmů u kriticky nemocných svými nežádoucími účinky, toxicitou a narušením střevního mikrobiomu (tab. 4) [27]. Z infekčních příčin je hlavní a obávanou příčinou průjmů infekce Clostridium difficile (CD), která vzniká hlavně u pacientů se sníženou diverzitou střevního mikrobiomu. Kolonizováno CD je až 23 % hospitalizovaných pacientů [28]. Testování pacientů s průjmy na toxin CD již patří mezi rutinní postupy nejen v rámci intenzivní péče, ale i na standardních odděleních. Ostatní bakteriální či virové infekce jsou méně časté, u imunosuprimovaných pacientů je vhodné pomýšlet na oportunní infekce, např. cytomegalovirovou nebo mykotickou. Mnohé studie poukazují na asociaci mezi větší tíží základního kritického onemocnění a výskytem průjmů [26]. Mechanizmy, které se na vzniku průjmů podílejí, jsou především zvýšení intestinální permeability a slizniční poškození v těsné vazbě na kompromitovanou střevní imunitu a složení mikrobiomu. Ke vzniku průjmů může také přispívat enterální výživa, a to trojím mechanizmem. Za prvé osmoticky, neboť enterální výživa je obvykle roztok hypertonický. Za druhé tím, že jde o výživu bezezbytkovou, chudou na nevstřebatelné oligosacharidy, které jsou substrátem pro kolonické bakterie produkující mastné kyseliny o krátkém řetězci a tyto kyseliny jsou dále nezbytné pro výživu a udržení absorpční funkce kolonocytů. A za třetí pro bakteriální kontaminaci vlastní enterální výživy. Většinou jde o gramnegativní nozokomiální kmeny bakterií, které nejprve osídlí retrográdně nutriční set (do 24 hod je kontaminováno až 48 % setů) a posléze pronikají až k vlastnímu vaku s výživou. Po pomnožení jejich aplikace s výživou do traktu pacienta přispívá k urychlené kolonizaci GIT patogenními nemocničními kmeny [29].
V praxi je vhodné u každého kriticky nemocného s nově vzniklým průjmem vyloučit infekční příčinu včetně otestování na toxin CD, revidovat medikaci potenciálně podporující průjmy, při podezření na dysmikrobiální průjmy zvážit individuálně, nikoli paušálně, obohacení enterální výživy o vlákninu anebo probiotika (viz následující odstavec). Sety a vaky s enterální výživou je vhodné měnit po 24 hod v prevenci bakteriální kontaminace.
Bariérová funkce GIT a fekální mikrobiom u kriticky nemocných
Střevní permeabilita je definována jako určitý stupeň pasivní difuze napříč střevní stěnou. Z praktického pohledu v intenzivní péči je podstatná především prostupnost střevní stěny pro bakterie a toxické bakteriální produkty. Mezi mechanizmy, které zvyšují střevní permeabilitu u kriticky nemocných, patří především ischemicko‑reperfuzní poškození sliznice GIT, intraabdominální hypertenze a syndrom bakteriálního přerůstání [30]. V konečném důsledku dochází k poškození funkce mezibuněčných spojení (tight junction) ve střevní sliznici a narušená střevní bariéra vede ke zvýšené bakteriální translokaci do mezenteriálního řečiště s excesivní aktivací imunitního systému, která je pak „motorem“ rozvoje MODS se všemi negativními důsledky.Měření střevní permeability není v praxi běžně dostupné a je založeno na orální aplikaci látek o vysoké molekulové hmotnosti, které mohou být absorbovány pouze paracelulárně. Jejich výskyt v moči nepřímo vypovídá o funkci mezibuněčných spojení ve střevní sliznici. Sukróza odráží permeabilitu gastroduodenální, neboť je rychle enzymaticky degradována v proximálním tenkém střevě. Nejčastěji užívaná kombinace laktulózy a manitolu vypovídá o permeabilitě tenkého střeva, protože obě látky jsou přeměněny bakteriemi až v céku [31]. Oproti tomu sukralóza je rezistentní vůči bakteriální fermentaci a je užívána k ozřejmění celkové permeability GIT [32]. Hlavní limitací těchto vyšetření je obtížná interpretace výsledků při renální dysfunkci, která často provází kritické stonání.
Alternativními markery bariérové funkce střeva, které zlepšují výtěžnost a interpretaci předchozích testů, jsou D‑laktát, plazmatický citrulin a fatty acid binding protein (FABP). D‑laktát je produkován pouze abnormální střevní flórou nebo pokud masa mikrobiomu intenzivně roste jako např. při bakteriálním přerůstání. Jeho vyšší hladina v plazmě provází také akutní zánětlivá střevní onemocnění. Citrulin je aminokyselina, která je syntetizována především v enterocytech. Pokles plazmatického citrulinu u kriticky nemocných je markerem snížené funkce enterocytární masy a je nezávislým prediktorem mortality po 24 hod od přijetí na JIP [33]. Určitou limitací vyšetření je snížená degradace citrulinu při akutním renálním selhání a možnost zvýšené extraintestinální syntézy citrulinu indukovanou syntetázou oxidu dusnatého při systémové zánětlivé odpovědi [34]. I přes tyto nepřesnosti v interpretaci je citrulin slibným markerem intestinální dysfunkce. Dalším markerem intestinálního poškození je FABP intestinálního či jaterního typu, což jsou malé proteiny obsažené v cytoplazmě enterocytů. Jejich zvýšená plazmatická hladina koreluje s tíží šokového stavu a MODS u pacientů se septickým šokem nebo akutní pankreatitidou [34].
Bakteriální translokace však není univerzálním mechanizmem vzniku sepse, spíše je u disponovaných jedinců motorem progrese kritického onemocnění do MODS [35,36]. Nový vhled do této problematiky přineslo studium fekálního mikrobiomu u kriticky nemocných. Fekální mikrobiom obsahuje zhruba 10× více buněk než má lidské tělo a asi 100× více genů, než je obsaženo v genomu lidském [37]. Obligátní anaerobní bakterie činí zhruba 95 % a fakultativní anaeroby 1–10 % a jejich komplexní interakce udržuje správnou bariérovou funkci střeva. Na počátku kritického stavu (v předchorobí jinak zdravých jedinců) vykazuje fekální mikrobiom velmi podobné složení jako u zdravých kontrol, nicméně po jednom týdnu kritického stonání a intenzivní péče včetně antibiotik je prokazatelná významná alterace mikroflóry s dominancí rodu Enterococcus a úbytkem obligátních anaerobů [38]. Častěji se objevuje také výskyt kmenů CD s rizikem infekce CDe. Tyto změny jsou asociovány se septickými komplikacemi pacientů s těžkou systémovou zánětlivou odpovědí a také s vyšší mortalitou [39]. Mechanizmy, které v kritickém stavu poškozují přirozenou diverzitu střevní mikroflóry, jsou luminální hypoxie a hyperkapnie, poškození sliznice způsobené vlastním šokovým stavem, léky neutralizující kyselou žaludeční sekreci, sedace a analgezie zpomalující střevní motilitu a nutriční vakuum dané chyběním nevstřebatelných sacharidů při definované enterální či parenterální výživě [30].
V současnosti probíhá výzkum na tomto poli ve dvou protichůdných aspektech. První přístup si klade za úkol potlačit patologickou střevní mikroflóru aplikací nevstřebatelných antibiotik do GIT a nazývá se selektivní dekontaminace GIT (SDD). SDD se ukázala být efektivní v redukci septických komplikací a rozvoje MODS. Příznivé ovlivnění mortality však není v literatuře konzistentní [40]. Daní za úspěch SDD však může být selekce multirezistentních bakteriálních kmenů a diskutovány jsou také nemalé náklady spojené s tímto přístupem. SDD je dle mezinárodních konsenzů doporučována jako přístup hodný dalšího výzkumu, který snižuje riziko především ventilátorové pneumonie a lze jej doporučit na pracovištích, kde se tento postup ukázal být efektivní [41]. Druhý přístup se snaží pomocí probiotik, event. synbiotik (kombinace prebiotik a probiotik) udržet fyziologickou fekální mikroflóru. Nevstřebatelná vláknina je nezbytná k udržení intestinální bariéry, neboť bakteriální fermentací vlákniny vznikají mastné kyseliny o krátkém řetězci, které jsou esenciální výživou pro kolonocyty i rezidentní bakterie. Suplementace vlákniny z malých studií je dobře tolerována a má potenciál zlepšovat diverzitu a ochrannou funkci fekálního mikrobiomu [42]. Oproti SDD je aplikace synbiotik z některých sdělení také efektivní ve snížení infekčních komplikací, nicméně nebyl prokázán efekt na podstatné klinické výstupy včetně mortality jako u SDD [43]. Možná bude cestou oba přístupy do budoucna zkombinovat při existenci nových antibiotik, která nejsou toxická pro komenzální bakterie jako např. fidaxomicin.
Intraabdominální hypertenze u kriticky nemocných
Intraabdominální tlak (intraabdominal pressure – IAP) je snadno měřitelná veličina u lůžka kriticky nemocného. V praxi měříme IAP obvykle nepřímo pomocí hladiny vodního sloupce nebo speciálního setu s tlakovým převodníkem, které jsou napojeny na permanentní močový katetr. Intraabdominální hypertenze (IAH) je přítomna, je‑li IAP ≥ 12 mm Hg při alespoň dvou měřeních s odstupem 1–6 hod po sobě a pokud tlak překročí opakovaně 20 mm Hg za rozvoje nové orgánové dysfunkce, pak hovoříme o syndromu břišního kompartmentu (abdominal compartment syndrom – ACS) [44]. Rozvoj AIH v průběhu kritického stonání interferuje s funkcí vitálních orgánů včetně GIT a je nezávislým prediktorem mortality [45]. V experimentálních modelech IAH/ACS vede rychle k dramatickému snížení slizniční perfuze GIT, exponenciálnímu nárůstu permeability střevní stěny, endotoxemii a k erozím a nekrózám jejunálních klků [46]. Rizikovými faktory pro IAH/ACS jsou snížená poddajnost břišní stěny, zvýšený intraluminální obsah (ileus, gastroparéza aj.), zvýšený intra‑ či retroperitoneální obsah (např. hemoperitoneum, tenzní ascites, těžká akutní pankreatitida), dále masivní kapilární leak v těžkém šokovém stavu s pozitivní tekutinovou bilancí nad 5 l/den anebo polytransfuze, obezita i sama umělá plicní ventilace. Časné rozpoznání a léčba IAH a především ACS zvyšuje šanci na přežití, proto je monitorace IAP doporučena u všech kriticky nemocných s rizikovými faktory [44]. Úvodní management je vždy konzervativní (tab. 5), neboť chirurgická dekomprese jako poslední možnost je zatížená signifikantní morbiditou i přes užití moderních chirurgických technik [47].Závěr
AGI je častým a prognosticky zásadním problémem v péči o kriticky nemocného. Proces diagnostiky a terapie této dysfunkce je velmi komplexní a probíhá za spoluúčasti řady odborností včetně gastroenterologa. Širší porozumění této problematice je významným přínosem pro tyto pacienty.Zkratky
GIT gastrointestinální trakt
MODS multiple organ dysfunction syndrome – syndrom multiorgánové dysfunkce
AGI acute gastrointestinal injury – akutní gastrointestinální dysfunkce
IAP intraabdominal pressure – intra- abdominální tlak
IAH intraabdominální hypertenze
SDD selective digestive decontamination – selektivní dekontaminace trávicího traktu
FABP fatty acid binding protein
ACS abdominal compatrment syndrome – syndrom břišního kompartmentu
CD Clostridium difficile
Podpořeno projektem Ministerstva zdravotnictví koncepčního rozvoje výzkumné organizace 00669806 – FN Plzeň, Programem rozvoje vědních oborů Karlovy Univerzity (projekt P36) a projektem CZ.1.05/2.1.00/03.0076 Evropského fondu pro regionální rozvoj.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno/Submitted: 13. 1. 2015
Přijato/Accepted: 17. 5. 2015
MUDr. Karel Balihar
Gastroenterologické a hepatologické oddělení, I. interní klinika LF UK a FN Plzeň
Alej Svobody 80, 304 60 Plzeň
balihar@fnplzen.cz

Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Balihar K, Kozeluhova J, Fremundova L et al. Dysfunkce horní části trávicího traktu u kriticky nemocných: současný pohled a perspektiva. Gastroent Hepatol 2013; 67 (1): 39–44.
2. Lower Gastrointestinal Tract at the US National Library of Medicine Medical Subject Headings (MeSH). [online]. Available from: http: //www.nlm.nih.gov/cgi/mesh/2011/MB_cgi?mode=&term=Lower+Gastrointestinal+Tract/mesh/ MBrowser.html.
3. Bone RC, Balk RA, Cerra FB et al. Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. The ACCP/SCCM Consensus Conference Committee. American College of Chest Physicians/Society of Critical Care Medicine. 1992. Chest 2009; 136 (Suppl 5): e28.
4. Moore FA. The role of the gastrointestinal tract in postinjury multiple organ failure. Am J Surg 1999; 178 (6): 449–453.
5. Reintam BA, Malbrain ML, Starkopf J et al. Gastrointestinal function in intensive care patients: terminology, definitions and management. Recommendations of the ESICM Working Group on Abdominal Problems. Intensive Care Med 2012; 38 (3): 384–394. doi: 10.1007/s00134‑011‑2459‑y.
6. Reintam A, Parm P, Kitus R et al. Gastrointestinal failure score in critically ill patients: a prospective observational study. Crit Care 2008; 12 (4): R90. doi: 10.1186/cc6958.
7. Khadaroo RG, Marshall JC. Gastrointestinal dysfunction in the critically ill: can we measure it? Crit Care 2008; 12 (5): 180. doi: 10.1186/cc7001.
8. Singh G, Harkema JM, Mayberry AJ et al. Severe depression of gut absorptive capacity in patients following trauma or sepsis. J Trauma 1994; 36 (6): 803–808.
9. Fraser RJ, Ritz M, Di Matteo AC et al. Distal small bowel motility and lipid absorption in patients following abdominal aortic aneurysm repair surgery. World J Gastroenterol 2006; 12 (4): 582–587.
10. Sim JA, Horowitz M, Summers MJ et al. Mesenteric blood flow, glucose absorption and blood pressure responses to small intestinal glucose in critically ill patients older than 65 years. Intensive Care Med 2013; 39 (2): 258–266. doi: 10.1007/s00 134‑012‑2719‑5.
11. Nguyen NQ, Besanko LK, Burgstad C et al. Delayed enteral feeding impairs intestinal carbohydrate absorption in critically ill patients. Crit Care Med 2012; 40 (1): 50–54. doi: 10.1097/CCM.0b013e31822d71a6.
12. Berger MM, Shenkin A. Vitamins and trace elements: practical aspects of supplementation. Nutrition 2006; 22 (9): 952–955.
13. Mostafa SM, Bhandari S, Ritchie G et al. Constipation and its implications in the critically ill patient. Br J Anaesth 2003; 91 (6): 815–819.
14. Herbert MK, Holzer P. Standardized concept for the treatment of gastrointestinal dysmotility in critically ill patients – current status and future options. Clin Nutr 2008; 27 (1): 25–41.
15. Rauch S, Krueger K, Turan A et al. Use of wireless motility capsule to determine gastric emptying and small intestinal transit times in critically ill trauma patients. J Crit Care 2012; 27 (5): 534.e7–e12. doi: 10.1016/j.jcrc.2011.12.002.
16. Heaton KW, Radvan J, Cripps H et al. Defecation frequency and timing, and stool form in the general population: a prospective study. Gut 1992; 33 (6): 818–824.
17. Bujanda L. The effects of alcohol consumption upon the gastrointestinal tract. Am J Gastroenterol 2000; 95 (12): 3374–3382.
18. Celis‑Rodriguez E, Birchenall C, de la Cal MA et al. Clinical practice guidelines for evidence‑based management of sedoanalgesia in critically ill adult patients. Med Intensiva 2013; 37 (8): 519–574. doi: 10.1016/j.medin.2013.04.001.
19. van der Spoel JI, Oudemans‑van Straaten HM, Kuiper MA et al. Laxation of critically ill patients with lactulose or polyethylene glycol: a two‑center randomized, double‑blind, placebo‑controlled trial. Crit Care Med 2007; 35 (12): 2726–2731.
20. Meissner W, Schmidt U, Hartmann M et al. Oral naloxone reverses opioid‑associated constipation. Pain 2000; 84 (1): 105–109.
21. Sawh SB, Selvaraj IP, Danga A et al. Use of methylnaltrexone for the treatment of opioid‑induced constipation in critical care patients. Mayo Clin Proc 2012; 87 (3): 255–259. doi: 10.1016/j.mayocp.2011.11.014.
22. Tollesson PO, Cassuto J, Faxen A et al. Lack of effect of metoclopramide on colonic motility after cholecystectomy. Eur J Surg 1991; 157 (5): 355–358.
23. Zpráva Státního ústavu pro kontrolu léčiv z 1.8.2013. [online]. Dostupné z: http: //www.sukl.cz/metoklopramid‑ome- zeni‑pouzivani.
24. Althausen PL, Gupta MC, Benson DR et al. The use of neostigmine to treat postoperative ileus in orthopedic spinal patients. J Spinal Disord 2001; 14 (6): 541–545.
25. Trevisani GT, Hyman NH, Church JM. Neostigmine: safe and effective treatment for acute colonic pseudo‑obstruction. Dis Colon Rectum 2000; 43 (5): 599–603.
26. Jack L, Coyer F, Courtney M et al. Diarrhoea risk factors in enterally tube fed critically ill patients: a retrospective audit. Intensive Crit Care Nurs 2010; 26 (6): 327–334. doi: 10.1016/j.iccn.2010.08.001.
27. Chang SJ, Huang HH. Diarrhea in enterally fed patients: blame the diet? Curr Opin Clin Nutr Metab Care 2013; 16 (5): 588–594. doi: 10.1097/MCO.0b013e328363bcaf.
28. Hung YP, Lee JC, Lin HJ et al. Clinical impact of Clostridium difficile colonization. J Microbiol Immunol Infect 2015; 48 (3): 241–248. doi: 10.1016/j.jmii.2014.04.011.
29. Mathus‑Vliegen EM, Bredius MW, Binnekade JM. Analysis of sites of bacterial contamination in an enteral feeding system. JPEN J Parenter Enteral Nutr 2006; 30 (6): 519–525.
30. Papoff P, Ceccarelli G, d‘Ettorre G et al. Gut microbial translocation in critically ill children and effects of supplementation with pre‑ and pro biotics. Int J Microbiol 2012; 2012: 151393. doi: 10.1155/ 2012/151393.
31. Matejovic M, Krouzecky A, Rokyta R Jr et al. Effects of intestinal surgery on pulmonary, glomerular, and intestinal permeability, and its relation to the hemodynamics and oxidative stress. Surg Today 2004; 34 (1): 24–31.
32. Salles Teixeira TF, Boroni Moreira AP, Silva Souza NC et al. Intestinal permeability measurements: general aspects and possible pitfalls. Nutr Hosp 2014; 29 (2): 269–281. doi: 10.3305/nh.2014.29.2. 7076.
33. Piton G, Manzon C, Monnet E et al. Plasma citrulline kinetics and prognostic value in critically ill patients. Intensive Care Med 2010; 36 (4): 702–706. doi: 10.1007/s00134‑010‑1751‑6.
34. Piton G, Manzon C, Cypriani B et al. Acute intestinal failure in critically ill patients: is plasma citrulline the right marker? Intensive Care Med 2011; 37 (6): 911–917. doi: 10.1007/s00134‑011‑2172‑x.
35. Soeters PB, Luyer MD, Greve JW et al. The significance of bowel permeability. Curr Opin Clin Nutr Metab Care 2007; 10 (5): 632–638.
36. Sedman PC, Macfie J, Sagar P et al. The prevalence of gut translocation in humans. Gastroenterology 1994; 107 (3): 643–649.
37. Gill SR, Pop M, Deboy RT et al. Metagenomic analysis of the human distal gut microbiome. Science 2006; 312 (5778): 1355–1359.
38. Iapichino G, Callegari ML, Marzorati S et al. Impact of antibiotics on the gut microbiota of critically ill patients. J Med Microbiol 2008; 57 (Pt 8): 1007–1014.
39. Shimizu K, Ogura H, Asahara T et al. Probiotic/synbiotic therapy for treating critically ill patients from a gut microbiota perspective. Dig Dis Sci 2013; 58 (1): 23–32. doi: 10.1007/s10620‑012‑2334‑x.
40. Silvestri L, van Saene HK, Milanese M et al. Selective decontamination of the digestive tract reduces bacterial bloodstream infection and mortality in critically ill patients. Systematic review of randomized, controlled trials. J Hosp Infect 2007; 65 (3): 187–203.
41. Dellinger RP, Levy MM, Rhodes A et al. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock, 2012. Intensive Care Med 2013; 39 (2): 165–228. doi: 10.1007/ s00134‑012‑2769‑8.
42. O‘Keefe SJ, Ou J, Delany JP et al. Effect of fiber supplementation on the microbiota in critically ill patients. World J Gastrointest Pathophysiol 2011; 2 (6): 138–145. doi: 10. 4291/wjgp.v2.i6.138.
43. Shimizu K, Ogura H, Goto M et al. Synbiotics decrease the incidence of septic complications in patients with severe SIRS: a preliminary report. Dig Dis Sci 2009; 54 (5): 1071–1078. doi: 10.1007/s10620‑008‑0460‑2.
44. Kirkpatrick AW, Roberts DJ, De Waele J et al. Intra‑abdominal hypertension and the abdominal compartment syndrome: updated consensus definitions and clinical practice guidelines from the World Society of the Abdominal Compartment Syndrome. Intensive Care Med 2013; 39 (7): 1190–1206. doi: 10.1007/s00134‑013‑2906‑z.
45. Reintam A, Parm P, Kitus R et al. Primary and secondary intra‑abdominal hypertension – different impact on ICU outcome. Intensive Care Med 2008; 34 (9): 1624–1631. doi: 10.1007/s00134‑008‑1134‑4.
46. Kirkpatrick AW, Roberts DJ, De Waele J et al. Is intra‑abdominal hypertension a missing factor that drives multiple organ dysfunction syndrome? Crit Care 2014; 18 (2): 124. doi: 10.1186/cc13785.
47. Chiara O, Cimbanassi S, Boati S et al. Surgical management of abdominal compartment syndrome. Minerva Anestesiol 2011; 77 (4): 457–462.