Doporučený postup diagnostiky a léčby infekce virem hepatitidy B
Petr Husa1, Jan Šperl Orcid.org 2, Petr Urbánek Orcid.org 3, Soňa Fraňková Orcid.org 2, Stanislav Plíšek Orcid.org 4, Petr Kümpel Orcid.org 5, Luděk Rožnovský6
+ Pracoviště
Souhrn
Nová doporučení odrážejí nárůst poznatků, které byly publikovány od vydání předchozího českého doporučeného postupu v září 2014. Základem pro napsání tohoto doporučeného postupu byla doporučení Evropské asociace pro studium jater z dubna 2017. Podle kvalifikovaných odhadů je celosvětově chronicky infikováno virem hepatitidy B (HBV) 240 mil. lidí. Česká republika patří mezi státy s nízkou prevalencí infekce HBV. Podle posledních sérologických přehledů z roku 2001 bylo 0,56 % našich občanů chronicky infikováno HBV. V roce 2013 byla provedena obdobná studie jen ve dvou krajích České republiky a zjištěná prevalence byla jen 0,064 %. Infekce HBV může vyvolat závažná, život ohrožující poškození jater – fulminantní hepatitidu, jaterní cirhózu a hepatocelulární karcinom (HCC – hepatocellular carcinoma). Hlavním cílem léčby je prodloužit délku života a zlepšit jeho kvalitu zabráněním progrese chronické hepatitidy do jaterní cirhózy, dekompenzace cirhózy a vzniku HCC. Předpokladem dosažení tohoto cíle je trvalá suprese replikace HBV. Dalšími cíli léčby jsou prevence vertikálního přenosu infekce z matky na novorozence, zábrana reaktivace infekce HBV a léčba extrahepatálních manifestací HBV. Obecně jsou možné dvě strategie léčby chronické hepatitidy B – léčba nukleosidovými nebo nukleotidovými analogy (NA) nebo pegylovaným interferonem alfa. V současnosti je naprostá většina pacientů v České republice a v celé Evropě léčena NA. V Evropské unii je v současnosti schválena léčba následujícími NA – lamivudinem, adefovir dipivoxilem, entecavirem (ETV), telbivudinem (TBV), tenofovir disoproxil fumarátem (TDF) a tenofovir alafenamidem (TAF). TAF a TBV nejsou v České republice komerčně dostupné. Hlavní výhodou léčby vysoce účinnými NA s vysokou genetickou bariérou pro vznik rezistence (ETV, TDF, TAF) je predikovatelně vysoká a dlouhodobá antivirová účinnost vedoucí k dosažení nedetekovatelné HBV DNA v séru u naprosté většiny adherentních pacientů a příznivý bezpečnostní profil těchto léků. Těmito NA může být léčen každý pacient s chronickou hepatitidou B a představují jedinou možnost léčby u pacientů s dekompenzovanou jaterní cirhózou, po transplantaci jater, s extrahepatálními manifestacemi infekce HBV, závažnou akutní hepatitidou B nebo exacerbací chronické hepatitidy B.
Klíčová slova
chronická hepatitida B, entecavir, pegylovaný interferon alfa, tenofovir alafenamid, tenofovir disoproxil fumarát
Preambule
Níže uvedená doporučení pro diagnostiku a terapii infekce virem hepatitidy B (HBV) byla vytvořena členy pracovních skupin pro virové hepatitidy České hepatologické společnosti České lékařské společnosti Jana Evangelisty Purkyně (ČHS ČLS JEP) a Společnosti infekčního lékařství (SIL) ČLS JEP. Nová doporučení odrážejí nárůst poznatků, které byly publikovány od vydání předchozího doporučeného postupu ČHS a SIL v září 2014 [1,2]. Základem pro napsání tohoto doporučeného postupu byla doporučení Evropské asociace pro studium jater (EASL – The European Association for the Study of the Liver) z roku 2017 [3]. Maximální možné dodržování odborných doporučení je podmínkou dosažení efektivní péče o nemocné s virovou hepatitidou B v celostátním měřítku. Předkládaný dokument je oporou při jednání obou odborných společností se státními orgány a s plátci zdravotní péče.
V textu je na řadě míst uvedena kvalita důkazů a síla doporučení, která vychází ze systému GRADE. Kvalita důkazů je hodnocena od I (založená na výsledcích randomizovaných, kontrolovaných studií) přes II-1 (nerandomizované kontrolované studie), II-2 (studie kohortové nebo studie případů a kontrol), II-3 (průřezové populační studie a kazuistiky) až po III (názory respektovaných odborníků, deskriptivní epidemiologie). Síly doporučení potom 1 (silné doporučení) nebo 2 (slabší doporučení) [3].
1. Proč léčit chronickou infekci HBV?
Podle kvalifikovaných odhadů je celosvětově chronicky infikováno HBV 240 mil. lidí. Regionálně jsou obrovské rozdíly v prevalenci infekce HBV – jako nízká prevalence se bere pozitivita povrchového antigenu (HBsAg) u méně než 2 % populace, střední prevalence je 2–8 % a vysoká více než 8 % chronicky infikovaných HBV. ČR patří mezi státy s nízkou prevalencí infekce HBV. Podle posledních celostátních sérologických přehledů z roku 2001 bylo 0,56 % našich občanů chronicky infikováno HBV [4]. Recentnější výsledky z celé ČR nejsou k dispozici. V roce 2013 byla provedena obdobná studie jen ve dvou krajích ČR a zjištěná prevalence byla jen 0,064 % [5]. V posledních letech je u nás hlášeno méně než 100 případů akutní hepatitidy B ročně, výkyvy jsou jen minimální a lze pozorovat trvalý trend k poklesu případů tohoto závažného onemocnění [6]. Je to důsledek dlouhodobé vakcinace významné části naší populace proti HBV. V důsledku migrace obyvatelstva však může dojít k nárůstu výskytu infekce HBV v ČR, jak je to hlášeno z jiných evropských států, především z Německa a z Itálie. V rozvinutých zemích vč. ČR se infekce HBV nejčastěji přenáší sexuálním stykem.
Do chronického stadia přejde méně než 5 % akutních hepatitid B u dospělých imunokompetentních pacientů. Imunokompromitovaní nemocní (pacienti v pravidelném dialyzačním programu, pacienti podstupující protinádorovou či imunosupresivní léčbu, koinfikovaní virem lidského imunodeficitu – HIV) mají sníženou schopnost dosáhnout imunitní kontroly infekce HBV, a proto u nich přechází infekce HBV do chronicity ve více než 50 %. Pravděpodobnost chronicity u novorozenců infikovaných HBV vertikálně od matky je vyšší než 90 %, při infikování dětí mladších 5 let je pravděpodobnost vzniku chronické infekce HBV 25–50 %. Infekce novorozenců a malých dětí jsou v současné době v ČR naprosto výjimečné díky screeningu všech těhotných žen na přítomnost HBsAg a následné pasivní a aktivní imunizaci novorozenců HBsAg pozitivních matek. Navíc od roku 2001 je v naší republice prováděna plošná vakcinace dětí proti HBV – nyní od 9. týdne věku a 12letých dětí, pokud nebyly očkovány již v kojeneckém věku proti HBV.
Infekce HBV může vyvolat závažná, život ohrožující poškození jater – fulminantní hepatitidu, jaterní cirhózu a prokázaný je i příčinný vztah mezi HBV infekcí a hepatocelulárním karcinomem (HCC – hepatocellular carcinoma) – primárním karcinomem jater. Akutní jaterní selhání, jaterní cirhóza nebo HCC vyvolané infekcí HBV patří mezi obecně uznávané indikace pro provedení transplantace jater (TJ). V celosvětovém měřítku vzrostl počet úmrtí na dekompenzovanou jaterní cirhózu a HCC v souvislosti s chronickou infekcí mezi roky 1990 a 2013 o 33 %, v roce 2013 odhadem zemřelo na tato onemocnění více než 686 000 osob. Tato konečná stadia infekce HBV reprezentují indikaci pro 5–10 % TJ.
Morbidita a mortalita spojená s chronickou infekcí HBV závisí na výši virové replikace a vývoji jaterní cirhózy nebo HCC. Podle výsledků longitudinálních studií kolísá v době stanovení diagnózy chronické hepatitidy B 5letá pravděpodobnost vzniku jaterní cirhózy bez antivirové léčby mezi 8 a 20 %. Pět let přežije 80–86 % původně kompenzovaných cirhotiků, ale zhruba u 20 % z nich dojde v tomto období k dekompenzaci cirhózy. Naproti tomu prognóza nemocných s dekompenzovanou jaterní cirhózou je špatná – pravděpodobnost 5letého přežití bez TJ je pouze 14–35 %. Celosvětově narůstá incidence HCC. V současnosti se jedná o pátý nejčastější karcinom, který představuje kolem 5 % všech karcinomů. Roční incidence vzniku HCC je u pacientů s cirhózou vzniklou na podkladě chronické infekce HBV 2–5 %. Vývoj HCC je možný i u pacientů účinně antivirově léčených. Riziko vzniku HCC je zvýšeno u nemocných, kteří mají přítomen jeden nebo více prediktivních faktorů hostitelských (jaterní cirhózu, chronickou zánětlivě-nekrotickou aktivitu, starší věk, mužské pohlaví, africký původ, abúzus alkoholu, chronickou koinfekci s viry jiných typů hepatitid nebo HIV, diabetes mellitus nebo metabolický syndrom, aktivní kuřáctví, pozitivní rodinnou anamnézu HCC) a/nebo ze strany HBV (vysoká koncentrace HBV DNA a/nebo HBsAg, genotyp C více než B, specifické mutace). Uvedené faktory přispívají k progresi do jaterní cirhózy u neléčených pacientů s chronickou hepatitidou B.
V současnosti dostupné terapeutické možnosti mají jak krátkodobý, tak dlouhodobý přínos. Léčba jednoznačně zvyšuje kvalitu života a je „cost-effective“, tj. při splnění indikačních kritérií a při použití standardních postupů je terapie levnější než léčba komplikací pokročilé jaterní cirhózy.
2. Přirozený průběh a klinický obraz HBV infekce
Infekce HBV je spojena s velmi heterogenním spektrem jaterních onemocnění. Akutní hepatitida B je převážně benigní onemocnění končící ve většině případů spontánním uzdravením, v 0,1–1 % případů probíhá onemocnění fulminantně s vysokou mortalitou.
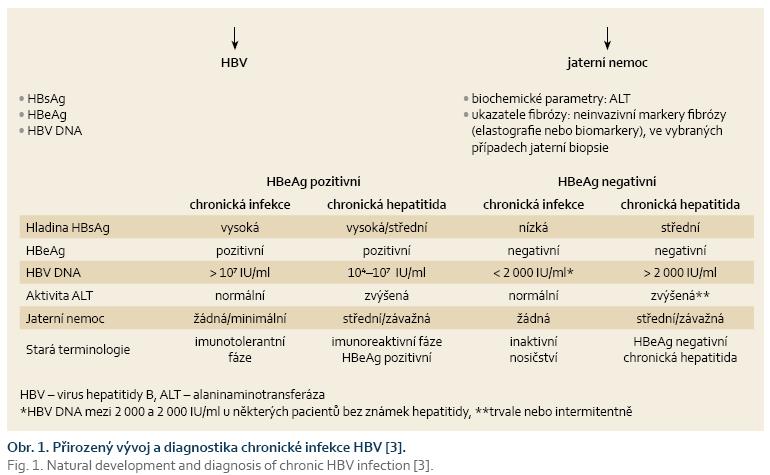
Chronická infekce HBV je označení pro infekci trvající déle než 6 měsíců. Jde o dynamický proces, který odráží interakce mezi virovou replikací a hostitelskou imunitní odpovědí. Ne všichni pacienti chronicky infikovaní HBV mají chronickou hepatitidu B. Přirozený vývoj chronické infekce HBV se schematicky dělí do pěti fází, a to podle přítomnosti HBeAg („e“ antigenu HBV), výše HBV DNA (nukleové kyseliny HBV), aktivity alaninaminotransferázy (ALT) a event. i přítomnosti či absence jaterního zánětu (obr. 1). Současná nomenklatura je založena na popisu dvou základních charakteristik chronicity – infekce vs. hepatitida. Existuje však signifikantní množství pacientů, které nelze jednoznačně zařadit do určité fáze. Opakované testování výše uvedených parametrů může pomoci upřesnit fázi procesu a stanovit optimální terapeutickou strategii. Přesto část hodnocených bude dlouhodobě či trvale spadat do „šedé“ zóny a přístup k jejich léčbě a sledování musí být individualizován.
Fáze 1 – HBeAg pozitivní chronická HBV infekce
Dříve označovaná jako imunotolerantní fáze, je časným stadiem infekce HBV. Je častá zejména u nemocných infikovaných vertikálně od matky, u kterých bývá protrahovaná. Pacienti v této fázi jsou charakterizováni pozitivitou HBeAg, vysokou úrovní replikace HBV, jejímž odrazem je vysoká koncentrace HBV DNA v séru, normální nebo nízkou aktivitou ALT, mírnou nebo žádnou zánětlivě-nekrotickou aktivitou a žádnou nebo pomalou progresí jaterní fibrózy. Již v této časné fázi infekce HBV jsou přítomny známky svědčící pro probíhající hepatokarcinogenezi. Během tohoto období je pravděpodobnost vzniku HBeAg/anti-HBe sérokonverze velmi nízká. Vzhledem k vysoké viremii jsou pacienti vysoce kontagiózní.
Fáze 2 – HBeAg pozitivní chronická hepatitida B
Dříve imunoreaktivní HBeAg pozitivní fáze, zpravidla se vyvine po několika letech trvání fáze 1. Je častější a/nebo rychleji vzniká při infekcích akvírovaných v dospělosti. Jde o HBeAg pozitivní pacienty s vysokou viremií a zvýšenou aktivitou ALT. V játrech jsou prokazatelné středně nebo vysoce závažné zánětlivě-nekrotické změny a akcelerovaná progrese fibrózy. Výsledek této fáze je variabilní. Většina pacientů dosáhne sérokonverze HBeAg/anti-HBe a suprese HBV DNA a přejde do fáze HBeAg negativní infekce. U ostatních pacientů nedojde ke kontrole HBV a vyvine se HBeAg negativní chronická hepatitida B, která může trvat mnoho let.
Fáze 3 – HBeAg negativní chronická infekce HBV
Dříve označovaná jako inaktivní nosičství HBV. HBsAg pozitivní, HBeAg negativní, anti-HBe pozitivní pacienti s velmi nízkou (< 2 000 IU/ml) nebo nedetekovatelnou hladinou HBV DNA v séru a s normální aktivitou ALT. Někteří pacienti v této fázi mohou mít HBV DNA v séru > 2 000 IU/ml (zpravidla < 20 000 IU/ml) ve spojení s trvale normální aktivitou ALT a pouze minimální jaterní zánětlivě-nekrotickou aktivitou a nízkým stupněm fibrózy. Pacienti ve fázi 3 mají nízké riziko vzniku jaterní cirhózy nebo HCC. Na druhé straně možnost progrese do chronické hepatitidy B, obvykle HBeAg negativní, stále existuje. Ke ztrátě HBsAg a/nebo sérokonverzi HBsAg/anti-HBs dochází spontánně u 1–3 % případů ročně.
Fáze 4 – HBeAg negativní chronická hepatitida B
Dříve HBeAg negativní chronická hepatitida B. Tato fáze může následovat HBeAg/anti-HBe sérokonverzi, ke které došlo během fáze 2. Jedná se o HBsAg pozitivní, HBeAg negativní, obvykle anti-HBe pozitivní pacienty, s perzistující nebo fluktuující střední až vysokou hladinou HBV DNA v séru a přechodně nebo trvale zvýšenou aktivitou ALT. V jaterní histologii jsou prokazatelné zánětlivě-nekrotické změny a fibróza. Negativita HBeAg je většinou podmíněna mutací v tzv. pre-core nebo v basal core promotor oblasti genomu viru. Tato fáze je spojena s nízkou pravděpodobností vzniku spontánní remise nemoci.
Fáze 5 – HBsAg negativní fáze
Také označovaná jako okultní infekce HBV. Po ztrátě HBsAg může replikace HBV na nízké úrovni přetrvávat. HBsAg je negativní, celkové anti-HBc protilátky jsou pozitivní, anti-HBs protilátky mohou být detekovatelné, ale nemusí. Zřídka je negativita HBsAg dána nízkou senzitivitou eseje použité pro detekci HBsAg. Pacienti v této fázi mají normální aktivitu ALT, obvykle, ale ne vždy nedetekovatelnou HBV DNA v séru. I u nich však lze většinou prokázat HBV DNA v jaterní tkáni (ve formě cccDNA – covalently closed circular DNA). Ztráta HBsAg je spojena se snížením rizika vzniku jaterní cirhózy, její dekompenzace, vývoje HCC a delším přežíváním. Pokud dojde ke vzniku cirhózy ještě před ztrátou HBsAg, pacient zůstává v riziku HCC a je nutná celoživotní surveillance HCC. Imunosuprese může vést k reaktivaci infekce HBV.
3. Iniciální vyšetření pacienta s chronickou infekcí HBV
Vstupní vyšetření pacienta s nově diagnostikovanou chronickou infekcí HBV musí zahrnovat kompletní anamnézu, fyzikální vyšetření, stanovení aktivity a pokročilosti jaterního onemocnění a markerů infekce HBV. Sexuálním partnerům a osobám žijícím ve společné domácnosti infikovaných by mělo být doporučeno testování sérologických markerů infekce HBV (HBsAg, anti-HBc celkové a třídy IgM, anti-HBs). V případě negativity těchto sérologických ukazatelů by měli být očkováni proti HBV.
Přehled sérologických, molekulárně genetických a histologických nálezů u infekce HBV a jejich význam je uveden na obr. 1. Uvedené nálezy představují nejčastější a nejjednodušší možné varianty. V případech různých mutací virového genomu se mohou sérologické nálezy významně lišit. Při nejasnostech je proto vhodné konzultovat specializované pracoviště.
Vstupní vyšetření
1. Posouzení závažnosti jaterního po-škození je zásadní pro správnou indikaci léčby a surveillance HCC. Základem je vyšetření fyzikální, biochemické – ALT, aspartátamino-transferáza, gama-glutamyltranspeptidáza, alkalická fosfatáza, bilirubin, sérový albumin) a hematologické (krevní obraz a protrombinový čas). U všech pacientů je doporučeno provedení ultrazvukového vyšetření břicha. Jaterní biopsie nebo neinvazivní testy by měly být provedeny k průkazu aktivity nebo pokročilosti jaterního onemocnění, pokud jsou výsledky biochemických vyšetření a markerů HBV nepřesvědčivé. Pokročilost jaterního onemocnění se v současnosti stanovuje především neinvazivními metodami, které zahrnují měření tuhosti jater a sérových biomarkerů jaterní fibrózy. Tranzientní elastografie byla z těchto metod dosud nejvíce studována a je nejpřesnější pro určení pokročilé fibrózy. Diagnostická přesnost všech neinvazivních testů je lepší pro vyloučení než potvrzení pokročilé fibrózy nebo cirhózy. Výsledky tranzientní elastografie mohou být ovlivněny závažnou zánětlivou aktivitou jater spojenou s vysokou aktivitou ALT. Za střední fibrózu, která je vždy indikací k zahájení protivirové léčby, je při neinvazivním elastografickém vyšetření považována taková hodnota tuhosti jater, která přesahuje dolní mez pro střední fibrózu (nebo dosahuje hodnoty F2 a vyšší) ve validační tabulce poskytnuté výrobcem příslušného přístroje. Jaterní biopsie a následné histologické vyšetření získané jaterní tkáně se provádí jen v následujících přesně definovaných případech: a) pokud je nutné stanovit stupeň zánětlivě-nekrotické aktivity a fibrózy u pacientů s nejasnými indikacemi pro okamžité zahájení antivirové léčby a současně výsledek neinvazivního měření tuhosti jater nepřesahuje dolní mez pro střední fibrózu; b) pro posouzení přítomnosti jiných možných příčin jaterního onemocnění, jako jsou steatóza nebo steatohepatitida. Jaterní biop-sie není obvykle nutná u pacientů s jaterní cirhózou nebo u těch, u kterých je léčba indikována bez ohledu na stupeň aktivity a pokročilosti jaterního onemocnění.
2. Stanovení HBeAg a anti-HBe je zásadní pro určení fáze chronické infekce HBV.
3. Stanovení hladiny HBV DNA v séru je nezbytné pro stanovení diagnózy, fáze chronické infekce HBV, rozhodnutí léčit a monitorování efektu léčby. K průkazu HBV DNA v séru se používá vysoce senzitivní polymerázová řetězová reakce (PCR – polymerase chain reaction) v reálném čase. Výsledky získané touto metodou jsou udávány v mezinárodních jednotkách na mililitr (IU/ml). Dolní detekční limit této metody je 10–15 IU/ml.
4. Stanovení hladiny HBsAg v séru může být užitečné, zejména u pacientů s HBeAg negativní infekcí a pacientů léčených pegylovaným interferonem alfa (PEG-IFN-α).
5. Určení genotypu HBV není nezbytné při vstupním vyšetření, ale má svůj prediktivní význam při léčbě PEG-IFN a při stanovení rizika vzniku HCC.
6. Komorbidity musí být systematicky potvrzeny či vyloučeny, vč. alkoholického, autoimunitního a metabolického poškození jater, koinfekce s virem hepatitidy D (HDV), hepatitidy C (HCV) a HIV.
7. Testování přítomnosti protilátek proti viru hepatitidy A (HAV) by mělo být provedeno a pacienti s negativitou protilátek anti-HAV třídy IgG by měli být očkováni proti HAV.
4. Cíle léčby chronické infekce HBV
Hlavním cílem léčby je prodloužit délku života a zlepšit jeho kvalitu zabráněním progrese chronické hepatitidy do jaterní cirhózy, dekompenzace cirhózy a vzniku HCC. Dalšími cíli léčby jsou prevence vertikálního přenosu infekce z matky na novorozence, zábrana reaktivace infekce HBV a léčba extrahepatálních manifestací (EHM) infekce HBV.
Pravděpodobnost, že výše uvedené cíle budou léčbou dosaženy, závisí na fázi přirozeného vývoje infekce HBV, pokročilosti jaterního procesu a věku pacienta v době zahájení léčby. U pacientů s pokročilou fibrózou nebo cirhózou je dalším cílem regrese fibrózy nebo cirhózy, i když tento efekt nebyl ještě klinicky plně objasněn.
U pacientů s HCC na podkladě chronické infekce HBV je cílem léčby nukleosidovými nebo nukleotidovými analogy (NA) nejprve suprese virové replikace, která vede ke stabilizaci jaterního onemocnění, prevenci progrese jaterní choroby a sekundárně ke snížení rizika rekurence HCC po potenciálně kurativní léčbě HCC. Stabilizované jaterní onemocnění je rovněž důležité pro bezpečnou a efektivní léčbu HCC.
U pacientů s akutní hepatitidou B je hlavním cílem léčby prevence rizika akutního nebo subakutního jaterního selhání. Dalšími cíli jsou i zlepšení kvality života zkrácením manifestního jaterního onemocnění a snížení rizika přechodu infekce do chronicity.
5. Klíčové body úspěšné léčby chronické infekce HBV
1. Navození dlouhodobé suprese hladiny HBV DNA v séru, ideálně pod dolním limitem citlivosti PCR v reálném čase (10–15 IU/ml), je hlavním úkolem současných terapeutických strategií (I, 1 – kvalita důkazů I, síla doporučení 1).
2. U HBeAg pozitivních pacientů se za uspokojivý výsledek léčby považuje ztráta HBeAg s dosažením / bez dosažení sérokonverze HBeAg/anti-HBe, což často představuje částečnou imunitní kontrolu chronické infekce HBV (II-1, 1).
3. Biochemická odpověď definovaná jako normalizace ALT by měla být považována za další ukazatel úspěšné léčby, kterého je dosaženo u většiny pacientů s dlouhodobou supresí replikace HBV (II-1, 1).
4. Ideální výsledek léčby představuje u pacientů HBeAg pozitivních i negativních setrvalé vymizení HBsAg se sérokonverzí/bez sérokonverze do anti-HBs. Jde o indikátor hluboké suprese replikace HBV a exprese virových proteinů (II-1, 1).
6. Obecné indikace k léčbě chronické hepatitidy B
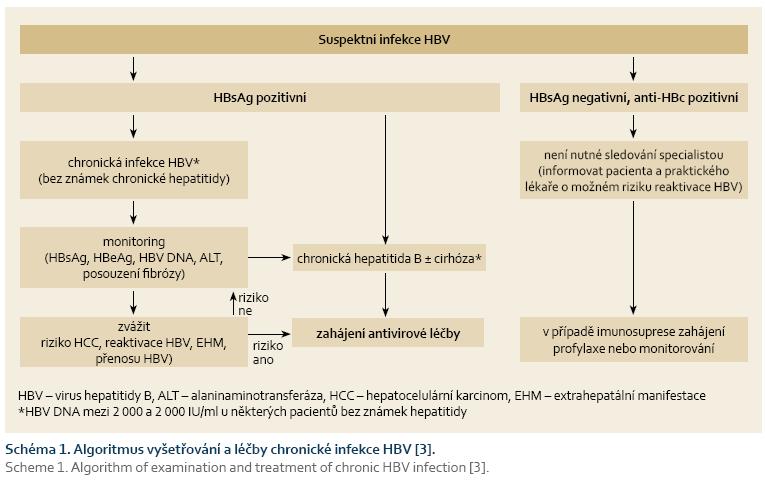
Obecný algoritmus pro indikace léčby infekce HBV je uveden na schématu 1. Pro HBeAg pozitivní i HBeAg negativní formu chronické hepatitidy jsou obecně platná stejná doporučení:
1. Všichni pacienti s HBeAg pozitivní i HBeAg negativní chronickou hepatitidou B, definovanou hladinou HBV DNA v séru > 2 000 IU/ml, ALT > horní hranice normy (ULN – upper limit of normal) a/nebo minimálně středně těžkým zánětlivě-nekrotickým procesem nebo fibrózou, by měli být léčeni (I, 1).
2. Pacienti s kompenzovanou i dekompenzovanou jaterní cirhózou potřebují léčbu, pokud lze u nich detekovat HBV DNA v séru (jakákoli hladina), a to bez ohledu na aktivitu ALT (I, 1).
3. Pacienti s hladinou HBV DNA v séru > 20 000 IU/ml a aktivitou ALT > 2× ULN (označovaní jako nemocní se zjevně aktivní hepatitidou B) by měli zahájit léčbu bez ohledu na stupeň fibrózy (II-2, 1). Proto není u nich nutné provádět před léčbou biopsii jater, jejíž výsledek neovlivní rozhodnutí léčit. Neinvazivní vyšetření je u nich vhodné k posouzení pokročilosti fibrózy a pro potvrzení nebo vyloučení jaterní cirhózy.
4. Pacienti s HBeAg pozitivní chronickou infekcí HBV, s trvale normální aktivitou ALT a vysokou hladinou HBV DNA v séru, by měli být léčeni, pokud jsou starší 30 let, a to bez ohledu na závažnost histologických změn v játrech (III, 2).
5. Pacienti s HBeAg pozitivní nebo HBeAg negativní chronickou infekcí HBV a rodinným výskytem HCC, jaterní cirhózy nebo EHM mohou být léčeni, i když nejsou splněna obecná indikační kritéria (III, 2).
7. Monitorování neléčených pacientů
Pacienty, kteří nejsou kandidáty okamžité antivirové léčby, je třeba monitorovat po stránce aktivity ALT, výše HBV DNA v séru a stupně fibrózy (neinvazivními metodami).
1. Osoby HBeAg pozitivní, mladší 30 let a nesplňující kritéria pro zahájení léčby je třeba kontrolovat minimálně každých 3–6 měsíců (II-2, 1). Ideální jsou kontroly aktivity ALT každé 3 měsíce, hladiny HBV DNA v séru každých 6–12 měsíců a jaterní fibrózy každých 12 měsíců.
2. Pacienty s HBeAg negativní chronickou infekcí HBV a sérovou hladinou HBV DNA < 2 000 IU/ml, kteří nesplňují kritéria pro léčbu, je nutné sledovat každých 6–12 měsíců (II-2, 1) po stránce aktivity ALT. Hladina HBV DNA a stupeň fibrózy by se měly hodnotit zhruba po 2–3 letech.
3. Pacienti s HBeAg negativní chronickou infekcí HBV a sérovou HBV DNA ≥ 2 000 IU/ml, kteří nesplňují kritéria pro zahájení léčby, by se měli kontrolovat první rok po 3 měsících a dále po 6 měsících (aktivita ALT). Hladina HBV DNA a neinvazivní vyšetření fibrózy se během prvních 3 let sledování provádí každý rok, dále potom celoživotně jako u ostatních pacientů v této fázi, tedy každé 2–3 roky (III, 1).
8. Strategie léčby chronické hepatitidy B
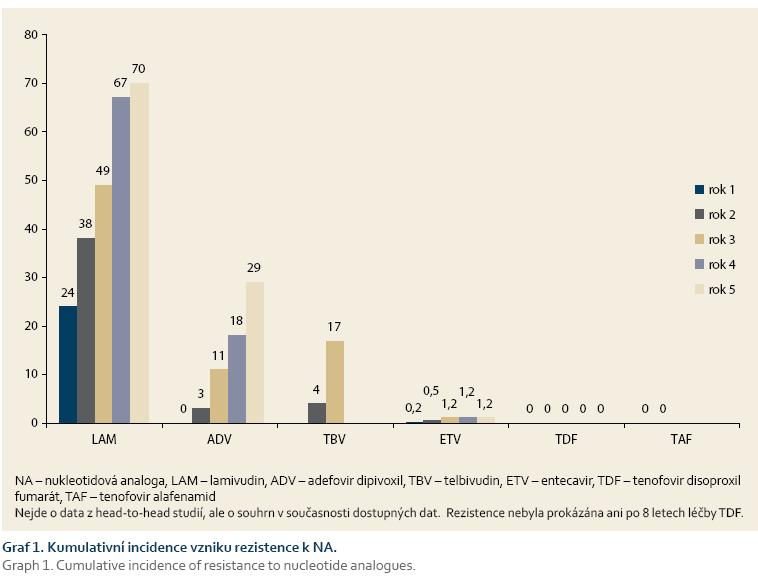
Obecně jsou možné dvě strategie léčby chronické hepatitidy B – léčba NA nebo PEG-IFN. V Evropské unii je v současnosti schválena léčba následujícími NA: lamivudinem (LAM), adefovir dipivoxilem (ADV), entecavirem (ETV), telbivudinem (TBV), tenofovir disoproxil fumarátem (TDF) a tenofovir alafenamidem (TAF). TAF a TBV nejsou v ČR komerčně dostupné. Kumulativní incidence vzniku rezistence při léčbě NA je patrna z grafu 1.
Hlavní výhodou léčby vysoce účinnými NA s vysokou genetickou bariérou pro vznik rezistence (ETV, TDF, TAF) je predikovatelně vysoká a dlouhodobá antivirová účinnost vedoucí k dosažení nedetekovatelné HBV DNA v séru u naprosté většiny adherentních pacientů a příznivý bezpečnostní profil těchto léků. Těmito NA může být léčen každý pacient s chronickou hepatitidou B a představují jedinou možnost léčby u pacientů s dekompenzovanou jaterní cirhózou, po TJ, s EHM, akutní hepatitidou B nebo závažnou exacerbací chronické hepatitidy B.
K prevenci vzniku reaktivace HBV při imunosupresi a prevenci přenosu HBV od pacientů s vysokou viremií, kteří nesplňují typická indikační kritéria pro léčbu, lze použít jen NA.
Logickým základem pro léčbu PEG-IFN je navození dlouhodobé imunologické kontroly časově omezenou léčbou. Hlavní nevýhodou této léčby je vysoká variabilita odpovědi na léčbu a nepříznivý bezpečnostní profil, který způsobuje, že významná část pacientů není pro tuto léčbu vhodná nebo ji odmítá. Před zvolením léčby PEG-IFN je nutné posoudit řadu faktorů virologických (genotyp HBV, hladinu HBV DNA, stav HBsAg, HBeAg) i hostitelských (aktivitu a pokročilost jaterního onemocnění). Nutné je pečlivé monitorování během léčby s uplatňováním pravidel pro její předčasné ukončení (stopping rules), aby byla včas ukončena léčba, která nemá naději na dlouhodobý úspěch.
U teoreticky výhodné kombinace NA s antivirovým efektem a PEG-IFN s imunomodulačním účinkem nebyla dosud prokázána superiorita proti monoterapii. Navíc zůstává řada nevyřešených otázek týkajících se výběru pacientů, načasování začátku léčby a její délky.
9. Definice odpovědi na antivirovou léčbu
Odpověď na léčbu se dělí na virologickou (VR – virological response), sérologickou (SR – serological response), biochemickou (BR – biochemical response) a histologickou. Všechny typy odpovědi je třeba stanovit několikrát během léčby a po jejím skončení. Definice VR se liší podle okamžiku stanovení (během léčby nebo po ní) a typu léčby.
9.1 Virologická odpověď
9.1.1 Léčba NA
-
VR během léčby je definována jako HBV DNA pod hranicí detekovatelnosti metodou PCR v reálném čase, s dolním detekčním limitem 10–15 IU/ml.
- Primární rezistence (non-response) je definována jako pokles HBV DNA v séru o < 1 dekadický logaritmus během prvních 3 měsíců léčby.
- Parciální VR – jedná se o pokles HBV DNA v séru o > 1 dekadický logaritmus, ale ne pod hranici detekovatelnosti (metodou PCR v reálném čase), po nejméně 12 měsících léčby NA u pacientů s dobrou adherencí k léčbě.
- Virologický breakthrough – potvrzený vzestup HBV DNA nejméně o 1 dekadický logaritmus od nejnižší dosažené hodnoty (nadir) během léčby NA.
- HBV rezistence na NA – selekce variant HBV, u kterých substituce aminokyselin vede ke snížené citlivosti na podávaný NA. Vznik těchto variant je příčinou primární rezistence nebo virologického breakthrough.
- Setrvalá VR (SVR) po skončení léčby je definována jako HBV DNA < 2 000 IU/ml nejméně 12 měsíců po skončení léčby.
9.1.2 Léčba PEG-IFN
-
Primární rezistence (non-response) nebyla dosud jasně prokázána.
- VR je definována jako HBV DNA v séru < 2 000 IU/ml. Obvykle se hodnotí po 6 měsících léčby a v době ukončení léčby.
- SVR po skončení léčby je definována jako HBV DNA v séru < 2 000 IU/ml nejméně 12 měsíců po skončení léčby.
9.2 Sérologická odpověď
SR je definována jako ztráta HBeAg nebo sérokonverze HBeAg/anti-HBe (pouze u původně HBeAg pozitivních pacientů) a/nebo ztráta HBsAg nebo sérokonverze HBsAg/anti-HBs (u všech pacientů).
9.3 Biochemická odpověď
BR je definována jako normalizace aktivity ALT. Protože tato aktivita často fluktuuje, je třeba sledovat aktivitu ALT každé 3 měsíce po dobu nejméně 1 roku po skončení léčby a teprve potom lze potvrdit dosažení setrvalé BR (SBR). U některých pacientů lze pozorovat během prvního roku po skončení léčby přechodné elevace aktivity ALT a teprve potom je dosaženo SBR. V těchto případech se jako vhodný čas pro stanovení SBR jeví 2 roky od poslední elevace ALT.
9.4 Histologická odpověď
Histologická odpověď je definována jako pokles nekroinflamatorní aktivity oproti výchozí hodnotě nejméně o 2 body při použití HAI (histology activity index) nebo Ishakova skórovacího systému, bez zhoršení fibrózy.
10. Léčba naivních pacientů NA
10.1 Úspěšnost léčby NA
Úspěšnost léčby NA byla posuzována v řadě randomizovaných klinických studiích fáze III. Strategie léčby NA je stejná u pacientů s jaterní cirhózou i bez ní vzhledem k podobné účinnosti a bezpečnosti dlouhodobé léčby obou skupin pacientů.
1. Dlouhodobé podávání účinných NA s vysokou genetickou bariérou proti vzniku rezistence je léčbou volby bez ohledu na pokročilost jaterního onemocnění (I, 1).
2. Preferovanými režimy jsou monoterapie ETV, TDF nebo TAF (I, 1).
3. LAM, ADV a TBV nejsou doporučeny pro léčbu chronické hepatitidy B (I, 1).
U pacientů s HBeAg pozitivní chronickou hepatitidou B byla po 5 letech léčby ETV 99% kumulativní pravděpodobnost dosažení VR a 53% pravděpodobnost dosažení ztráty HBeAg. U HBeAg negativních pacientů to za stejné období bylo 98 a 95 %, pravděpodobnost vzniku rezistence byla < 1 %.
Za 5 let léčby pacientů s HBeAg pozitivní chronickou hepatitidou B TDF vykazovalo 97 % léčených osob VR, 73 % léčených mělo normální aktivitu ALT, ke ztrátě HBeAg došlo u 49 % pacientů, HBeAg/anti-HBe sérokonverzi u 40 %, ztrátě HBsAg u 10 % a sérokonverzi HBsAg/anti-HBs v 8 % případů. Po 8 letech léčby HBeAg negativní chronické hepatitidy B TDF došlo k VR (definované jako HBV DNA < 400 IU/ml) v 99 % a normalizace ALT v 88 % případů. Rezistence na TDF prokázána nebyla. Pravděpodobnost dosažení ztráty HBsAg byla u HBeAg negativní chronické hepatitidy B léčených TDF nebo ETV velmi nízká – během prvního roku léčby nedošlo k vymizení HBsAg u žádného pacienta a po 8 letech jen zhruba u 1 % léčených.
U pacientů léčených TAF jsou zatím k dispozici data maximálně po 96 týdnech léčby. U pacientů s HBeAg pozitivní chronickou hepatitidou B bylo dosaženo po 48 a 96 týdnech léčby VR v 64, resp. 75 % ztráty HBeAg ve 14 a 22 %, sérokonverze HBeAg/anti-HBe v 10 a 18 % případů. Normalizace ALT dosáhlo po 96 týdnech léčby 75 % léčených TAF, což bylo významně více než při léčbě TDF (68 %). VR byla po 48 a 96 týdnech léčby TAF zaznamenána v 94, resp. 90 % případů. Pravděpodobnost vymizení HBsAg během prvních 96 týdnů léčby byla nízká u HBeAg pozitivní i HBeAg negativní chronické hepatitidy B – do 1 %.
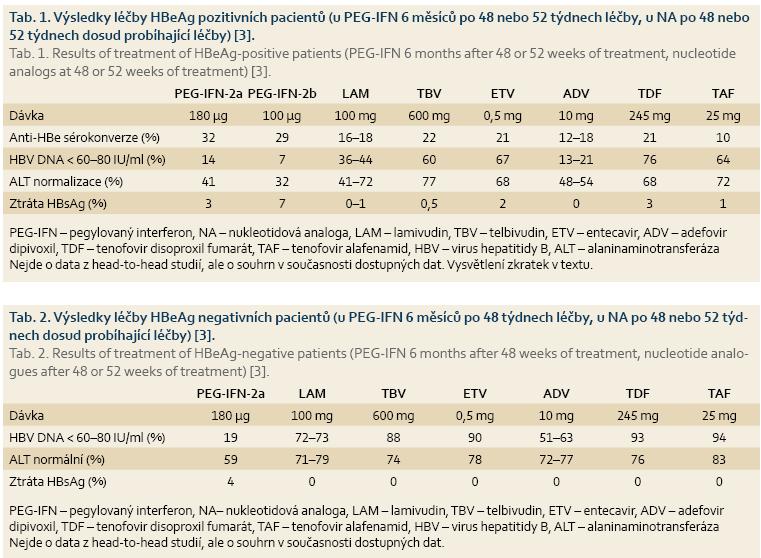
Souhrn účinnosti NA a PEG-IFN je uveden v tab. 1 a 2. Nejde o výsledky head-to-head studií, ale o souhrn dat z různých klinických studií, které se navzájem lišily definicí normalizace aktivity ALT a dolním limitem kvantifikace použitých HBV DNA esejí.
10.2 Monitorování pacientů léčených ETV, TDF nebo TAF
1. Všechny pacienty léčené NA je třeba periodicky kontrolovat vč. aktivity ALT a hladiny HBV DNA v séru (I, 1).
2. U všech pacientů v riziku renální choroby léčených jakýmkoli NA a všech pacientů léčených TDF, bez ohledu na renální riziko, by měly být periodicky vyšetřovány funkce ledvin vč. glomerulární filtrace stanovené výpočtem (eGFR) a sérové hladiny fosfátů (II-2, 1).
3. U všech pacientů léčených TDF, kteří jsou v riziku vzniku a/nebo již mají renální nebo kostní onemocnění, by se měl zvážit přechod na ETV či TAF, v závislosti na předchozí léčbě LAM (II-2/I, 1).
Před zahájením léčby NA s vysokou genetickou bariérou pro vznik rezistence (ETV, TDF, TAF) je třeba vyšetřit krevní obraz, aktivitu ALT, ledvinné funkční testy (eGFR, hladinu sérových fosfátů, biochemické vyšetření moči a sedimentu) a hladinu HBV DNA senzitivní PCR esejí. Redukce dávky ETV a TDF je nutná při eGFR < 50 ml/min, u TAF až < 15 ml/min. Vstupní riziko vzniku renálního postižení by mělo být posouzeno u všech pacientů. Vysoké riziko představuje přítomnost jednoho nebo více z následujících faktorů: dekompenzovaná jaterní cirhóza, eGFR < 60 ml/min, špatně kompenzovaná hypertenze, proteinurie, dekompenzovaný diabetes mellitus, aktivní glomerulonefritida, současné podávání nefrotoxických léků, stav po transplantaci solidního orgánu.
Během léčby by měly být aktivita ALT a sérová hladina HBV DNA kontrolovány každé 3–4 měsíce (během prvního roku léčby), potom 1× za 6 měsíců (ALT) a 6–12 měsíců (HBV DNA). Jestliže bude HBV DNA v séru nedetekovatelná, je vhodné zkontrolovat 1× za 12 měsíců HBsAg – v případě negativity je na místě stanovení protilátek anti-HBs.
Minimální zhoršení ledvinných funkcí často provází dlouhodobou léčbu ETV i TDF, ale nefrotoxický potenciál TDF je vyšší. Výskyt Fanconiho syndromu při léčbě TDF byl opakovaně popsán stejně jako odeznění průjevů tohoto syndromu při náhradě TDF entecavirem. Kromě toho bylo u pacientů léčených TDF prokázáno chronické tubulární postižení, pokles eGFR a denzity kostního minerálu. Proto je vhodné u všech pacientů léčených TDF monitorovat eGFR a hladinu sérových fosfátů každé 3 měsíce (v průběhu prvního roku léčby) a následně každých 6 měsíců, pokud nejsou známky ledvinného postižení. Pečlivější monitorování je třeba u nemocných s eGFR < 60 ml/min nebo hladinou sérových fosfátů < 2 mg/dl (0,8 mmo/l). Stejné monitorování ledvinných funkcí je vhodné i u pacientů léčených jinými NA, pokud jsou ve vysokém riziku renálního postižení. Registrační studie s TAF u chronické hepatitidy B prokázaly, že toto nové proléčivo tenofoviru má ve srovnání s TDF signifikantně sníženou renální a kostní toxicitu. Ke stejným výsledkům se dospělo i u nemocných infikovaných HIV, kteří byli léčeni TDF nebo TAF. U pacientů starších 60 let a/nebo s kostními či ledvinnými alteracemi by měly být preferovány režimy s ETV nebo TAF. Podrobně jsou tato doporučení uvedena v tab. 3.
10.3 Dlouhodobý efekt léčby NA
1. U pacientů dlouhodobě účinně léčených NA by měla surveillance HCC pokračovat během celé doby léčby (II-2, 1).
2. Pokud má pacient před zahájením terapie NA jaterní cirhózu nebo je ve středním nebo vysokém riziku HCC, je surveillance HCC povinná (II-2, 1).
Ukázalo se, že dlouhodobá léčba ETV či TDF zastavuje progresi jaterní choroby, může vést k signifikantnímu poklesu zánětlivě-nekrotických změn a fibrózy vč. regrese již vzniklé jaterní cirhózy. Navíc projevy již dekompenzované cirhózy se mohou zmírnit, nebo dokonce zcela vymizet, a to zejména v časných stadiích dekompenzace. Tím je dramaticky redukována potřeba TJ.
Riziko HCC však trvá a zůstává hlavním problémem pacientů léčených NA. Dlouhodobá léčba má pravděpodobně příznivý vliv na snížení incidence HCC, pokud se vezmou do úvahy výsledky randomizovaných a kohortových studií. Recentní data ukazují, že incidence HCC dále klesá i při pokračování léčby ETV nebo TDF za hranici 5 let. Tento pokles je zejména patrný u pacientů s jaterní cirhózou prokázanou již před zahájením léčby. HCC je pravděpodobně jediným faktorem, který ovlivňuje dlouhodobé přežívání pacientů s chronickou hepatitidou B, léčených ETV či TDF.
Pravděpodobnost přežívání pacientů na dlouhodobé efektivní terapii se všeobecně prodlužuje, a to navzdory přetrvávající možnosti vzniku HCC. Ke ztrátě HBsAg dochází během 5–8 let terapie u 10–12 % původně HBeAg pozitivních, u vstupně HBeAg negativních je tato pravděpodobnost výrazně nižší (< 1–2 % během 5–8 let léčby).
10.4 Ukončení léčby NA
1. Po potvrzeném vymizení HBsAg, se sérokonverzí HBsAg/anti-HBs nebo bez ní, by měla být léčba NA ukončena (II-2, 1).
2. Pokud dojde u původně HBeAg pozitivních nemocných bez jaterní cirhózy ke stabilní sérokonverzi HBeAg/anti-HBe a negativizaci sérové HBV DNA, léčba NA může být ukončena, a to min. 12 měsíců po dosažení tohoto cíle. Následně je doporučeno pečlivé monitorování (II-2, 2).
3. U vybraných HBeAg negativních pacientů bez jaterní cirhózy, u kterých bylo léčbou NA dosaženo dlouhodobé (≥ 3leté) virologické suprese, může být léčba NA ukončena za předpokladu, že je garantováno následné pečlivé monitorování (II-2, 2).
Většina pacientů musí být léčena NA dlouhodobě, protože tato léčba nevede k eradikaci HBV, ale jen udržuje infekci pod kontrolou, a jen zřídka dojde během léčby ke ztrátě HBsAg. Široce akceptovaná pravidla pro ukončení léčby (stopping rules) existují jen pro původně HBeAg pozitivní pacienty, u kterých došlo k sérokonverzi HBeAg/anti-HBeAg a negativitě sérové HBV DNA, a to za 6, lépe však až za 12 měsíců po dosažení tohoto cíle. Podle v současnosti dostupných informací přetrvává 3 roky po ukončení léčby u těchto nemocných zhruba v 90 % sérokonverze HBeAg/anti-HBe a přibližně u poloviny nemocných virologická remise, definovaná jako sérová HBV DNA pod 2 000–20 000 IU/ml. Alternativně může léčba pokračovat až do ztráty HBsAg, což představuje současný nejbezpečnější cíl pro ukončení léčby.
U HBeAg negativních pacientů se většinou doporučuje ukončit léčbu NA až po vymizení HBsAg. Podle nejnovějších informací, pocházejících především z Asie, je možné ukončit léčbu NA u pacientů s opakovaně nedetekovatelnou HBV DNA v séru – celkem 3× s 6měsíčními intervaly mezi jednotlivými stanoveními. Virologickou remisi, definovanou jako sérová HBV DNA pod 2 000–20 000 IU/ml, vykazovala 3 roky po skončení léčby zhruba polovina pacientů, pokud byli léčeni po dosažení virologické remise > 2 roky. Délka virologické remise před „bezpečným“ ukončením léčby NA není tedy zatím jasně definována.
Ukončení léčby NA se u pacientů s jaterní cirhózou obecně nedoporučuje, protože jsou popsány exacerbace hepatitidy (flares) a život ohrožující dekompenzace.
10.5 Ukončení léčby NA
1. Prevence vzniku rezistence spočívá zejména v užití NA s vysokou bariérou proti vzniku rezistence již v 1. linii léčby (I, 1).
2. Ve všech případech selhání léčby NA je nutné zkontrolovat adherenci k léčbě (II-1, 1).
3. Léčba následující po selhání předchozí léčby musí respektovat zkříženou rezistenci mezi NA (II-2, 1).
4. Novou léčbu je nutné podat okamžitě po potvrzení virologického selhání předchozí léčby (II-1, 1).
Základním preventivním opatřením proti vzniku rezistence je použité léků s vysokou genetickou bariérou proti vzniku rezistence a maximální virovou supresí (ETV, TDF, TAF) již v 1. linii léčby. Kombinace léků s nízkou genetickou bariérou proti vzniku rezistence (LAM nebo TBV s ADV) je nevhodná, protože vede k nedostatečné supresi virové replikace a vzniká nebezpečí vzniku multirezistentních kmenů HBV. Ze stejných důvodů je nevhodná i sekvenční terapie s použitím léků s nízkou genetickou bariérou proti vzniku rezistence.
Selhání léčby NA může být definováno jako:
- Primární rezistence (non-response) je téměř exkluzivně spojena s terapií ADV vzhledem k suboptimálnímu antivirovému efektu tohoto léku. Je nutné nejprve zkontrolovat adherenci k léčbě, špatná adherence je nejčastější příčinou primární rezistence u kteréhokoli NA. Nutné je rychlé nahrazení adefoviru ETV nebo TDF. Testování rezistence HBV přispívá ke správné volbě „záchranné“ terapie.
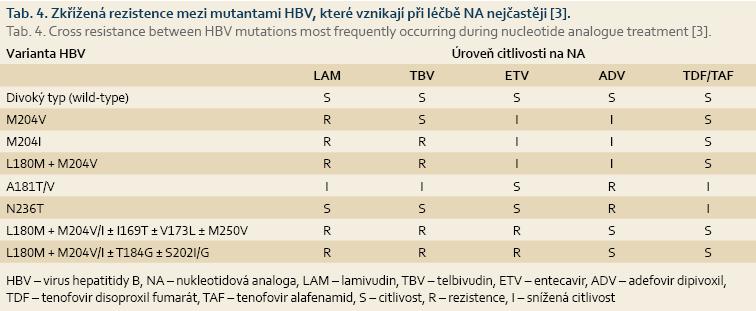
- Parciální VR se může vyskytnout při léčbě jakýmkoli NA. Nutné je opět nejprve zkontrolovat adherenci pacienta k léčbě. Pokud byl nemocný léčen NA s nízkou bariérou pro vznik rezistence (LAM, TBV, ADV), je nutné nahrazení účinnějším lékem při respektování zkřížené rezistence (tab. 4). Parciální VR vzniká při léčbě ETV nebo TDF většinou v důsledku velmi vysoké vstupní viremie. Nejde tedy o nedostatek účinnosti těchto léků, proto je nutné u těchto pacientů srovnávat sérovou hladinu HBV DNA před léčbou a po 48 týdnech léčby a její kinetiku. Pokud došlo k poklesu hladiny HBV DNA, pokračuje se v léčbě stejným lékem, protože déletrvající léčba zvyšuje pravděpodobnost dosažení VR a je velice nízké riziko vzniku rezistence při monoterapii těmito léky. Zatím není jasné, zda totéž platí i pro TAF. Pokud přetrvává hladina sérové HBV DNA bez výrazného poklesu (plateau), je na uvážení i přechod na léčbu jiným účinným lékem nebo kombinací ETV + TDF/TAF – to platí zejména pro pacienty s pokročilým jaterním onemocněním.
- Virologické breakthrough je u adherentních pacientů většinou spojeno s vývojem rezistence HBV k použitému léku. Na místě je okamžitá náhrada jiným účinným lékem a kontrola aktivity ALT a hladiny HBV DNA v séru za 1 měsíc poté, aby se zabránilo další progresi jaterní choroby a snížilo riziko jaterního selhání.
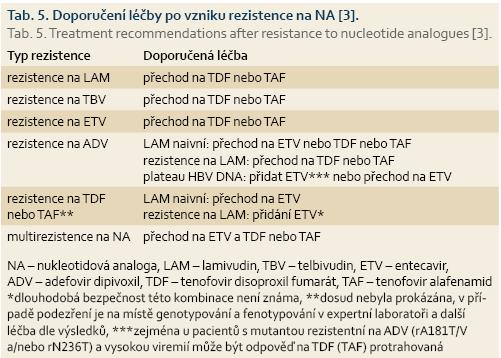
Rezistence HBV na NA je v současnosti řešitelným problémem. Vznik rezistence je spojen s vysokou vstupní hladinou HBV DNA v séru, pomalým poklesem HBV DNA během léčby a předchozí suboptimální terapií NA. Rezistenci lze identifikovat monitorováním sérových hladin HBV DNA nebo optimálně přímo určením rezistentní mutanty viru. Pokud dojde ke vzniku rezistence, musí být zahájena „záchranná“ terapie nejúčinnějším lékem, který nevykazuje zkříženou rezistenci s původně použitým NA. V tab. 5 jsou uvedena doporučení pro následnou léčbu. V případě infekce multirezistentním kmenem HBV je nutné provedené testování genotypové rezistence v referenční laboratoři. Podle výsledků několika klinických studií je kombinace TDF a ETV bezpečnou a účinnou možností „záchranné“ terapie.
11. Monoterapie PEG-IFN
11.1 Úspěšnost léčby PEG-IFN
1. PEG-IFN může být použit k iniciální terapii pacientů s mírnou nebo středně pokročilou hepatitidou B, a to HBeAg pozitivní i HBeAg negativní (I, 2).
2. Standardní délka léčby PEG-IFN je 48 týdnů (I, 1).
3. Prodloužení délky léčby PEG-IFN může být prospěšné u některých pacientů s HBeAg negativní chronickou hepatitidou B (II-1, 2).
PEG-IFN lze léčit pouze pacienty s mírnou a středně pokročilou chronickou hepatitidou B, v pečlivě vybraných případech i pacienty s kompenzovanou jaterní cirhózou, ale bez portální hypertenze. Úspěšnost 12 měsíců léčby PEG-IFN, hodnocená 6 měsíců po skončení této léčby, se u pacientů s HBeAg pozitivní chronickou hepatitidou pohybuje mezi 20 a 30 %. I když u většiny pacientů dojde ke ztrátě HBeAg nebo sérokonverzi HBeAg/anti-HBe již během prvních 6 měsíců léčby PEG-IFN, celkové výsledky 12měsíční léčby jsou lepší než 6měsíční a kratší doba léčby a/nebo snížení dávky PEG-IFN se nedoporučují. Metaanalýza tří velkých klinických studií prokázala současnou ztrátu HBeAg a supresi sérové HBV DNA < 2 000 IU/ml (6 měsíců po skončení léčby) u 23 % léčených. Negativita HBeAg přetrvávala 3 roky po skončení léčby u 81 % pacientů, kteří dosáhli negativní HBeAg 6 měsíců po skončení léčby. Ke ztrátě HBsAg došlo během 12 měsíců léčby PEG-IFN u 3–7 % pacientů. Pravděpodobnost ztráty HBsAg vzrostla po skončení léčby u původně HBeAg pozitivních pacientů, kteří dosáhli SVR. Po iniciální ztrátě HBeAg došlo během 3 let sledování ke ztrátě HBsAg ve 30 % případů. Po léčbě PEG-IFN je ztráta HBsAg nebo sérokonverze HBsAg/anti-HBs většinou trvalá, i když případy séroreverze HBsAg jsou v literatuře popsány.
Úspěšnost léčby nemocných HBeAg negativních klesá s délkou sledovacího období po skončení léčby. V registračních studiích byl PEG-IFN podáván 48 týdnů – BR a VR byly zaznamenány v 60 a 44 % (6 měsíců po skončení léčby), resp. v 31 a 28 % (3 roky po skončení léčby). Úspěšnost léčby byla nižší při infekci genotypy D nebo E – SVR ve 20 %. Ke ztrátě HBsAg dochází u HBeAg negativních pacientů během léčby jen velmi zřídka, ale s rostoucím intervalem po skončení léčby roste i pravděpodobnost ztráty HBsAg – 6 měsíců po léčbě 3 %, za 3 roky 9 % a za 5 let 12 %. Obecně dochází ke ztrátě HBsAg asi u 30 % nemocných, kteří dosáhli SVR.
Ve dvou studiích se srovnávala úspěšnost 48 a 72 (resp. 96) týdnů léčby PEG-IFN. Ve studii evropské (s převahou genotypu D) i čínské (s genotypy B a C) byla pravděpodobnost dosažení SVR při delší léčbě vyšší než při kratší – 29 vs. 12, resp. 50 vs. 16 %. V obou studiích to platilo i pro ztrátu HBsAg – 6 vs. 0, resp. 36 vs. 10 %.
11.2 Monitorování pacientů léčených PEG-IFN
1. Všichni pacienti léčení PEG-IFN by měli být periodicky monitorováni – základem jsou kontroly krevního obrazu, ALT, tyreotropního hormonu (TSH), hladiny HBV DNA v séru a HBsAg (I/II-2, 1).
2. U pacientů vstupně HBeAg pozitivních jsou nutné i pravidelné kontroly HBeAg/anti-HBe (I, 1).
3. Pacienti, kteří dosáhli VR léčbou PEG-IFN, musí být dlouhodobě sledováni vzhledem k nebezpečí vzniku relapsu (II-2, 1).
Během celého období léčby PEG-IFN by měly být krevní obraz a ALT kontrolovány každý měsíc, TSH 1× za 3 měsíce. Sérová hladina HBV DNA (event. i hladina HBsAg) by měla být kontrolována u všech pacientů po 3, 6 a 12 měsících léčby a 6 a 12 měsíců po léčbě. Ve stejných intervalech se provádí i kontroly HBeAg/anti-HBe u pacientů se vstupní HBeAg pozitivitou.
11.3 Predikce odpovědi na léčbu PEG-IFN
Před léčbou je vyšší pravděpodobnost dosažení sérokonverze HBeAg/anti-HBe u nemocných, kteří mají před léčbou relativně nízkou viremii, vysokou aktivitu ALT (> 2–5× ULN) a histologicky vysokou zánětlivou aktivitu. U pacientů infikovaných genotypy A nebo B dochází při léčbě PEG-IFN častěji k sérokonverzi HBeAg/anti-HBe a ztrátě HBsAg než při infekci genotypy C nebo D. Nezávislými pozitivními předpoklady pro úspěšnou léčbu HBeAg negativní chronické hepatitidy B jsou vysoká aktivita ALT, nízká viremie, mladší věk, ženské pohlaví a určitý genotyp HBV (genotyp B a C lépe než genotyp D). Pozitivní i negativní předpovědní hodnota uvedených parametrů je obecně nízká.
V průběhu léčby je nejdůležitějším dosud známým faktorem ovlivňujícím dosažení virologické odpovědi změna hladin HBsAg v séru. Nedostatečný pokles hladiny HBsAg během léčby je indikací k předčasnému ukončení léčby PEG-IFN (stopping rule). Kvantifikované stanovení HBsAg se v současnosti v ČR neprovádí rutinně, proto nelze tento ukazatel v našich podmínkách použít. Je proto nutné řídit se kinetikou sérových hladin HBV DNA. Pokud ve 12. týdnu léčby poklesne HBV DNA < 20 000 IU/ml, je 50% pravděpodobnost dosažení sérokonverze HBeAg/anti-HBe u původně HBeAg pozitivních pacientů a 50% pravděpodobnost dosažení SVR na léčbu u HBeAg negativních. Sérokonverze HBeAg/anti-HBe je častější, pokud během léčby dojde k imunologicky podmíněným vzestupům aktivity ALT (ALT flares) následovaných poklesem sérové hladiny HBV DNA.
Vzhledem k minimálnímu počtu pacientů léčených v posledních letech v ČR PEG-IFN pro chronickou hepatitidu B a nemožnosti monitorovat hladinu HBsAg není účelné v tomto doporučeném postupu podrobně uvádět všechna pravidla pro předčasné ukončení léčby PEG-IFN. V případě potřeby jsou dostupná v doporučeních EASL [3].
11.4 Dlouhodobé výsledky léčby PEG-IFN
1. Surveillance HCC musí pokračovat u pacientů ve vysokém riziku HCC i po dosažení setrvalé odpovědi na léčbu PEG-IFN, dokonce i při ztrátě HBsAg (III, 1).
U většiny pacientů, kteří dosáhnou SVR po léčbě PEG-IFN, přetrvává tato odpověď dlouhodobě, a to nejméně 5 let. U těchto osob zpravidla nedochází k progresi jaterní choroby, naopak se histologický nález oproti stavu před léčbou většinou zlepší. Nebezpečí vzniku HCC však trvá, zejména u pacientů s jaterní cirhózou.
12. Kombinovaná terapie chronické hepatitidy B
12.1 Kombinace NA
1. Léčba kombinací dvou NA s vysokou bariérou pro vznik rezistence (ETV, TDF, TAF) de novo se nedoporučuje (I, 1).
2. Pokud je pacient adherentní k léčbě, a přesto nedojde při léčbě ETV nebo TDF/TAF ke kompletní supresi replikace HBV (plateau), je možné přejít na druhý lék s vysokou bariérou pro vznik rezistence nebo na kombinaci obou léků (III, 2).
Zatím není k dispozici dostatek důkazů z klinických studií, které by prokázaly vyšší účinnost iniciálního podání kombinace dvou NA s vysokou účinností a vysokou bariérou pro vznik rezistence oproti monoterapii jedním takovým NA. Léčba pacientů se suboptimální odpovědí na léčbu ETV, TDF nebo TAF zůstává zatím kontroverzním tématem. U většiny těchto pacientů dochází při pokračování iniciální monoterapie NA k postupnému poklesu hladiny HBV DNA v séru. Podle výsledků dlouhodobých prospektivních klinických studií s velkým počtem zařazených pacientů není tento přístup spojen se zvýšením rizika vzniku rezistence HBV na podávaný lék. Přetrvávání minimální reziduální viremie (pod hranicí možnosti kvantifikovat hladinu HBV DNA v séru) není spojeno s rizikem progrese jaterního onemocnění ani se zvýšeným výskytem HCC u pacientů bez jaterní cirhózy. Na druhé straně u dekompenzovaných cirhotiků je nedosažení HBV DNA < 20 IU/ml významným rizikovým faktorem pro vznik HCC. U pacientů s kompenzovanou cirhózou to však prokázáno nebylo. Klinický význam dlouhodobého přetrvávání nízké viremie (v rozmezí od dolního limitu detekovatelnosti do 2 000 IU/ml) je zatím nejasný. U cirhotiků je v této situaci třeba zvážit kombinaci ETV + TDF/TAF nebo přechod z ETV na TDF/TAF nebo naopak.
12.2 Kombinace NA a PEG-IFN
1. Léčba kombinací NA a PEG-IFN se de novo nedoporučuje (I, 1).
2. U dosud neléčených HBeAg pozitivních pacientů se nedoporučuje krátkodobá léčba NA před nasazením PEG-IFN (II, 1).
3. U pacientů s dlouhodobou supresí chronické hepatitidy B navozenou NA se nedoporučuje přidání PEG-IFN do kombinace s NA ani náhrada NA PEG-IFN.
Kombinace NA s PEG-IFN byla zkoušena v klinických studiích u pacientů naivních i iniciálně léčených NA. Nejsou k dispozici přesvědčivé důkazy, které by podporovaly vyšší účinnost kombinované léčby oproti monoterapii NA nebo PEG-IFN. Pravděpodobnost vymizení HBsAg byla sice po 72 týdnech kombinované terapie TDF a PEG-IFN vyšší než při monoterapii PEG-IFN nebo TDF (9 vs. 3 vs. 0 %), ale úspěšnost byla obecně nízká a jednalo se především o pacienty infikované genotypem A. Přidání PEG-IFN po dosažení dlouhodobé suprese účinkem NA zvyšuje cenu léčby a frekvenci výskytu nežádoucích účinků, proto je nutné pečlivě zvážit potenciální výhody a nevýhody takové strategie u konkrétního pacienta.
13. Léčba pacientů s dekompenzovanou jaterní cirhózou
1. Nemocní s dekompenzovanou jaterní cirhózou a detekovatelnou HBV DNA v séru (bez ohledu na její výši) vyžadují urgentní zahájení antivirové léčby ve specializovaných centrech s napojením na transplantační jednotky. Lékem volby jsou NA s vysokou genetickou bariérou pro vznik rezistence, tedy ETV nebo TDF (I, 1).
2. PEG-IFN je u pacientů s dekompenzovanou cirhózou kontraindikován (II-1, 1).
3. Je nutné pečlivé monitorování tolerance léčby a vzniku vzácných komplikací léčby NA, kterými jsou laktátová acidóza nebo renální dysfunkce (II-2, 1).
Základní strategií léčby dekompenzovaných cirhotiků je dosažení kompletní virové suprese v co nejkratším intervalu. ETV a TDF jsou preferovanými léky u těchto nemocných vzhledem ke své účinnosti a dobrému bezpečnostnímu profilu. Dávka ETV je u pacientů s dekompenzovanou cirhózou 1 mg denně. Vzhledem k příznivému bezpečnostnímu profilu představuje TAF slibnou alternativu léčby v budoucnosti, zejména u pacientů s renálním poškozením, zatím však chybí údaje o účinnosti a bezpečnosti TAF v této indikaci. Podávání NA s nižší účinností a vyšší pravděpodobností vzniku rezistence (LAM, TBV, ADV) se nedoporučuje. Dávkování všech NA se musí korigovat podle renálních funkcí. Obecně udávaným možným nežádoucím účinkem léčby NA u pacientů s dekompenzovanou cirhózou je vznik laktátové acidózy. Z tohoto důvodu je nutné pečlivé monitorování především nemocných s MELD > 22 a poškozenou funkcí ledvin.
Hlavním cílem léčby dekompenzovaných cirhotiků je klinická kompenzace a odstranění nutnosti TJ. Jsou jasné důkazy, že antivirová terapie významně modifikuje přirozený vývoj jaterní cirhózy, zlepšuje jaterní funkce a prodlužuje přežívání. Podle výsledků metaanalýz se u pacientů léčených NA prodlužuje celkové přežívání a přežívání bez TJ o > 80 %. Asi 35 % léčených může být vyřazeno z čekací listiny pro TJ a v nejméně 40–50 % případů dojde k poklesu Child-Pugh skóre o ≥ 2 body. Pacienti s časným zahájením léčby NA mají lepší prognózu než ti, u kterých byla léčba zahájena později. Vysoké vstupní hodnoty Child-Pugh a MELD skóre jsou spojeny s kratším přežíváním – jaterní proces již dospěl do fáze, ze které není možné zlepšení. Nedetekovatelné sérové hladiny HBV DNA je dosaženo během prvního roku léčby ve > 80 % a to je spojeno se snížením rizika vzniku HCC. U všech pacientů s dekompenzovanou cirhózou je indikována celoživotní terapie NA. I přes úspěšnou léčbu NA zůstávají tito pacienti v riziku vzniku HCC, a proto je nutná dlouhodobá surveillance HCC.
14. Prevence rekurence infekce HBV po transplantaci jater
1. Všichni nemocní zařazení na čekací listinu pro TJ kvůli jaterní nemoci spojené s infekcí HBV by měli být léčeni NA (II, 1).
2. Prevencí rekurence infekce HBV po TJ je podávání kombinace hyperimununního imunoglobulinu (HBIG) a účinného NA (II-1, 1).
3. U pacientů s nízkým rizikem rekurence infekce HBV může být ukončeno podávání HBIG, ale profylaxe účinným NA musí pokračovat (II-1, 2).
4. HBsAg negativní příjemci jaterního štěpu od dárce s pozitivitou celkových protilátek anti-HBc jsou v riziku rekurence infekce HBV a měli by dostávat NA jako antivirovou profylaxi (II-2, 1).
Před zavedením NA do praxe byla rekurence infekce HBV po TJ obvyklá a představovala velký problém. Kombinací HBIG a NA se snížilo nebezpečí reinfekce štěpu na < 5 %. U vybraných pacientů, např. HBV DNA negativních v době TJ, lze podávat krátkodobě kombinaci HBIG a NA a potom pokračovat jen v podávání účinného NA. Podobně účinná se ukázala u určitých pacientů jen profylaxe ETV bez HBIG. Naproti tomu doživotní kombinovaná profylaxe HBIG a NA je nutná u pacientů s vysokým rizikem rekurence infekce HBV, zejména při pozitivitě HBV DNA v době TJ, pozitivitě HBeAg, s HCC, s koinfekcí HDV nebo HCV. V souvislosti s profylaxí po TJ je nutné brát do úvahy nefrotoxicitu NA vzhledem k nutnosti současného podávání kalcineurinových inhibitorů. Po TJ je imunitní systém terapeuticky suprimován, tím se vytváří potenciál pro reaktivaci infekce HBV u HBsAg negativního příjemce, který dostal játra od dárce s infekcí HBV v minulosti a má pozitivní anamnestické protilátky anti-HBc. Tito pacienti doživotně dostávají profylaxi, obvykle LAM.
15. Léčba infekce HBV u zvláštních skupin pacientů
15.1 Koinfekce HBV a HIV
1. U všech HIV pozitivních pacientů s koinfekcí HBV by měla být zahájena antiretrovirová terapie (ART) bez ohledu na počet CD4 buněk (II-2, 1).
2. HIV/HBV koinfikovaní pacienti by měli být léčeni ART režimem obsahujícím TDF nebo TAF (I pro TDF, II-1 pro TAF, 1).
U pacientů koinfikovaných HBV/HIV je větší riziko progrese fibrózy, vzniku jaterní cirhózy a HCC. Vzhledem k tomu, že TDF a TAF mají antivirovou aktivitu proti HIV i HBV, měla by ART vždy obsahovat buď TDF, nebo TAF. Ukončení ART obsahující TDF nebo TAF je spojeno s rizikem vzniku akutní exacerbace chronické hepatitidy B (flares) a dekompenzace jaterního onemocnění, proto by se tato léčba neměla přerušovat. Během ART by se měly pečlivě monitorovat toxické účinky léčby, a to zejména po stránce renální, kostní a jaterní. V současnosti jsou k dispozici zatím jen limitovaná data o účinnosti a bezpečnosti léčby TAF u HBV/HIV koinfikovaných osob. V důsledku restituce imunitního systému během ART může dojít k akutní exacerbaci chronické hepatitidy B, proto je nutné pečlivé monitorování jaterních funkcí během prvních měsíců ART.
15.2 Koinfekce HBV a HDV
1. PEG-IFN podávaný nejméně 48 týdnů představuje v současnosti jediný dostupný lék u HBV/HDV koinfikovaných osob s kompenzovaným jaterním onemocněním (I, 1).
2. Pokud jsou u HBV/HDV koinfikovaných patrné známky probíhající replikace HBV, měla by se zvážit současná terapie NA (II-2, 1).
3. Pokud je léčba PEG-IFN dobře tolerována, mělo by se v ní pokračovat po dobu 48 týdnů bez ohledu na odpověď během léčby (II-2, 2).
Infekce HDV je zatím v podmínkách ČR ojedinělá, ale s rostoucím počtem imigrantů může incidence onemocnění narůstat. Cílem léčby je útlum replikace HDV (HBV DNA bývá většinou negativní i metodou PCR v reálném čase kvůli supresivnímu vlivu HDV na replikaci HBV), který je většinou spojen s normalizací ALT a histologickým zlepšením. V klinických studiích byla zaznamenána VR na léčbu během podávání PEG-IFN mezi 17 a 47 %. Po skončení léčby procento HDV RNA negativních s časem výrazně klesá – 24 týdnů po léčbě na zhruba 25 %, v dalším období pak dochází k relapsu nejméně u 1/2 původně odpovídajících pacientů. Proto je nutné dlouhodobé monitorování HDV RNA v séru po skončení léčby PEG-IFN, které má trvat až do ztráty HBsAg. Ztráta HBsAg se bere za ukazatel vyléčení z infekce HDV a dochází k ní zhruba u 10 % pacientů léčených PEG-IFN. Několik studií se snažilo prokázat zvýšenou účinnost prodloužené doby léčby PEG-IFN, ale přesvědčivá data dosud chybějí. Dokonce i po 96 týdnech monoterapie PEG-IFN nebo kombinace PEG-IFN a TDF došlo během 24 týdnů po léčbě k relapsu v 36–39 % případů.
HDV je většinou dominantním virem při koinfekci HBV/HDV, proto je HBV DNA v séru většinou negativní. V případě, že sérová hladina HBV DNA je trvale > 2 000 IU/ml, je indikována léčba NA.
PEG-IFN je kontraindikován u nemocných s dekompenzovaným jaterním onemocněním. Tito pacienti by měli směřovat k TJ. V případě detekovatelné HBV DNA v séru je u těchto nemocných indikována léčba NA.
15.3 Koinfekce HBV a HCV
1. Léčba infekce HCV pomocí přímo působících virostatik (DAA – direct-acting antivirals) může způsobit reaktivaci infekce HBV. Pokud jsou splněna standardní kritéria pro léčbu hepatitidy B, je indikována terapie NA (II, 1).
2. HBsAg pozitivní pacienti by během léčby DAA měli dostávat profylaxi reaktivace infekce HBV do konce 12. týdne po skončení léčby DAA. Pečlivé monitorování je během tohoto období nutné (II-2, 2).
3. HBsAg negativní a anti-HBc pozitivní pacienti by měli být během léčby DAA pečlivě monitorováni a v případě elevace ALT testováni vzhledem k možné reaktivaci infekce HBV (II, 1).
U naprosté většiny nemocných replikace HCV utlumí replikaci HBV, proto je hladina HBV DNA v séru většinou nízká nebo nedetekovatelná metodou PCR v reálném čase. Progrese jaterní choroby je u HBV/HCV koinfikovaných akcelerována, riziko vzniku HCC je zvýšeno. Proto by měli být všichni pacienti se známou infekcí HBV testováni i vzhledem k infekci HCV. Standardní léčbou chronické infekce HCV je dosahováno SVR stejně často jako u pacientů s hepatitidou C bez současné infekce HBV. Existuje potenciální riziko reaktivace infekce HBV po supresi HCV během léčby DAA. Tato reaktivace je zvláště nebezpečná u pacientů s pokročilým jaterním onemocněním. Profylaktická opatření jsou přesně popsána v úvodu této kapitoly.
15.4 Těžký průběh akutní hepatitidy B
1. Více než 95 % dospělých pacientů s akutní hepatitidou B nevyžaduje specifickou léčbu a spontánně se vyléčí (II-2, 1).
2. Pouze pacienti s těžkým průběhem charakterizovaným koagulopatií nebo protrahovanou akutní hepatitidou B by měli být léčeni NA a zvažováni k TJ (II-2, 1).
Hlavním cílem léčby pacientů s akut-ní hepatitidou B je prevence rizika akutního nebo subakutního jaterního selhání. Dalšími cíli jsou zlepšení kvality života zkrácením délky trvání příznaků akutní hepatitidy a snížení rizika chronicity. Charakteristickým rysem těžkého průběhu akutní hepatitidy B je zejména koagulopatie, většinou ve studiích definovaná jako INR (international normalised ratio) > 1,5. Protrahovaný průběh akutní hepatitidy B je většinou definován perzistencí symptomů nebo zřetelného ikteru > 4 týdny. I když randomizované studie chybí, několik kohortových studií demonstrovalo příznivý vliv časně zahájené terapie vysoce účinnými NA na snížení rizika vzniku akutního jaterního selhání, potřeby TJ a snížení mortality. Pokud byla léčba NA zahájena pozdě, při klinických manifestacích jaterního selhání nebo při pokročilé jaterní encefalopatii, příznivý efekt antivirové terapie prokázán nebyl. V této indikaci jsou k dispozici příznivá data o léčbě TDF, ETV a dokonce i LAM, ale podání léků s vyšší genetickou bariérou k rezistenci je vhodnější. Proto by léčba LAM měla být zahájena pouze v případě, že není možné nebo přípustné podávat ETV nebo TDF. Lze předpokládat možnost použití TAF v této indikaci, zatím však ještě není k dispozici dostatek dat pro takové doporučení. Délka léčby nebyla stanovena, ale doporučuje se pokračovat nejméně 3 měsíce po sérokonverzi HBsAg/anti-HBs nebo 12 měsíců po sérokonverzi HBeAg/anti-HBe. Pokud nelze odlišit akutní hepatitidu B a reaktivaci chronické hepatitidy B, je na místě léčba NA.
15.5 Děti
1. U většiny dětí má chronická hepatitida B mírný průběh a standardní terapeutická kritéria nejsou většinou splněna. Proto musí být indikace k léčbě pečlivě zvážena (II-3, 1).
2. V případě splnění obecných indikací pro léčbu je možné léčit i tuto věkovou skupinu ETV, TDF, TAF nebo PEG-IFN (II-2, 2).
Díky plošné vakcinaci proti HBV v naprosté většině zemí světa výskyt infekce HBV v dětské populaci celosvětově významně poklesl a stále klesá. V klinických studiích bylo prokázáno, že bezpečnost a účinnost konvenčního IFN-α, LAM, ADV, ETV a TDF je u dětí srovnatelná s dospělými pacienty.
Léčba konvenčním IFN je schválena u dětí ve věku ≥ 3 roky (ostatní indikační kritéria jsou stejná jako u dospělých), PEG-IFN není u dětí s chronickou hepatitidou B schválen. Doporučená dávka IFN-α je 6 MU/m2, max. 10 MU, podávaná 3× týdně. Doba léčby je stejná jako u dospělých pacientů. TDF je schválen podle souhrnu údajů o přípravku pro léčbu dětí od 12 let, ETV od 2 let věku. Dávka LAM byla stanovena na 3 mg/kg/den, max. však 100 mg denně. V klinické studii bylo prokázáno, že denní dávka ADV 0,3 mg/kg u dětí ve věku 2–6 let a 10 mg u starších dětí vede ke stejným léčebným výsledkům jako dávka 10 mg denně u dospělých pacientů a je stejně dobře tolerována. Lamivudin a ADV jsou v ČR registrovány pouze pro léčbu chronické hepatitidy B u dospělých pacientů.
15.6 Zdravotníci
1. Pouze kvůli infekci HBV nelze zdravotníkům zakázat studium medicíny nebo vykonávání praxe, vč. chirurgie, stomatologie a příbuzných oborů (III, 1).
2. Zdravotníci se sérovou hladinou HBV DNA > 200 IU/ml vykonávající invazivní zákroky mají být léčeni NA k redukování rizika přenosu infekce HBV (II-2, 2).
Zdravotníci provádějící invazivní zákroky by měli být léčeni účinným NA s vysokou genetickou bariérou proti vzniku rezistence (ETV, TDF, TAF), aby u nich klesla viremie pod hranici detekovatelnosti PCR v reálném čase nebo alespoň < 200 IU/ml, a to i v případě, když nesplňují standardní indikace pro antivirovou léčbu. Přitom je nutné pečlivé monitorování adherence a účinnosti léčby – viremie může významně fluktuovat.
15.7 Těhotné ženy
1. Screening HBsAg v 1. trimestru gravidity je jednoznačně doporučen (I, 1).
Podle americké klasifikace US Food and Drug Administration Pharmaceutical Pregnancy Categories, která rozlišuje pět kategorií léků (A, B, C, D, X) podle možného ovlivnění těhotenství, patří TBV a TDF do kategorie B (tedy s druhým nejnižším rizikem) a LAM, ADV, ETV do kategorie C. Nejvíce informací o bezpečnosti NA pochází od HIV pozitivních žen léčených léky účinnými současně proti infekci HIV i HBV. Protivirová léčba u gravidních žen by neměla být zahajována, pokud to není vzhledem k aktivitě a pokročilosti jaterního procesu nezbytné. Preferovaný je v těhotenství TDF, protože má vysokou genetickou bariéru proti vzniku rezistence a k dispozici je nejvíce informací o bezpečném podávání během těhotenství. Bezpečnost léčby ETV v těhotenství není známa. IFN-α (PEG i konvenční) je v graviditě kontraindikován.
15.8 Ženy plánující těhotenství
1. U ženy plánující těhotenství v blízké budoucnosti, která nemá pokročilou jaterní fibrózu, je rozumné odložit začátek antivirové léčby až po porodu, event. až po ukončení kojení (II-2, 2).
2. U těhotných žen s pokročilou fibrózou nebo cirhózou (v důsledku chronické hepatitidy B) je doporučena léčba TDF (II-2, 1).
V případě pokročilé fibrózy nebo cirhózy je na místě okamžité zahájení léčby, pokud lze těhotenství plánovat do budoucna. Přednost by měla mít časově omezené léčba PEG-IFN, pokud nejsou přítomny její kontraindikace. Nutností je adekvátní antikoncepce během této léčby. Pokud není možné léčit PEG-IFN nebo tato léčba selhala, je nutná léčba NA. Vzhledem k předpokládané nutnosti léčby i během event. těhotenství v budoucnosti má přednost v této indikaci TDF.
15.9 Ženy, které neplánovaně otěhotněly během antivirové léčby
Pokud otěhotní žena již léčená TDF, pokračuje se v této léčbě, v případě léčby ETV nebo jiným NA se přechází na TDF (II-2, 1).
Pokud neočekávaně otěhotní žena během antivirové léčby, je nutné nově posoudit terapeutické indikace. Stejný postup platí, pokud je chronická hepatitida B diagnostikována během těhotenství. Pokud se jedná o ženu s pokročilou fibrózou nebo cirhózou, je nutné pokračovat v léčbě za těchto podmínek:
-
PEG-IFN musí být vysazen a nahrazen NA,
- NA kategorie rizika C (ETV, ADV) by měla být nahrazena NA kategorie B, preferovaný je v této indikaci TDF, protože má vysokou účinnost a genetickou bariéru proti vzniku rezistence a k dispozici je nejvíce informací o bezpečném podávání během těhotenství.
15.10 Prevence perinatálního přenosu HBV u hyperviremických matek
U všech těhotných žen s vysokou sérovou HBV DNA (> 200 000 IU/ml) by měla probíhat profylaxe TDF, která začíná ve 24.–28. gestačním týdnu a pokračuje 12 týdnů po porodu (I, 1).
Prevence perinatálního přenosu HBV standardní kombinací pasivní a aktivní imunizace aplikované do 12 hod po porodu je spolehlivá u matek s nízkou viremií, ale nemusí být dostatečně účinná u matek s vysokou viremií, u kterých redukuje riziko perinatálního přenosu infekce z > 90 % na < 10 %. K selhání dochází téměř výhradně u žen s hladinou HBV DNA v séru > 200 000 IU/ml, které jsou většinou HBeAg pozitivní. Mnohem méně často se vysoká viremie vyskytuje u HBeAg negativních žen s normální aktivitou ALT. Profylaktické podávání LAM, TBV nebo TDF v posledním trimestru u pacientek s vysokou HBV DNA v séru zvyšuje účinnost pasivní a aktivní imunizace proti HBV. Přednost má v této indikaci TDF vzhledem k bezpečnosti a účinnosti. TDF je indikován u gravidních žen s HBV DNA > 200 000 IU/ml od 24. do 28. týdne gravidity. Pokud byla léčba NA pouze z důvodu prevence perinatálního přenosu, může být ukončena během prvních 3 měsíců po narození dítěte.
15.11 Kojící matky
Kojení není kontraindikováno u neléčených HBsAg pozitivních matek nebo při léčbě nebo profylaxi TDF (III, 2).
HBsAg lze v mateřském mléce prokázat, ale kojení není kontraindikováno u HBsAg pozitivních matek, zejména při standardní pasivní a aktivní imunizaci novorozence. Bezpečnost léčby NA při kojení není známa. TDF přechází do mateřského mléka, ale jeho orální biologická dostupnost je limitována, a děti jsou proto při kojení exponovány jen malé dávce léku. Přesto nelze léčbu TDF při kojení doporučit, protože nejsou známy účinky léku na novorozence a kojence.
15.12 Pacienti na pravidelné dialyzační léčbě a po transplantaci ledviny
1. Všichni pacienti podstupující pravidelnou dialyzační léčbu (PDL) a pacienti po transplantaci ledviny (TL) by měli být testováni na přítomnost markerů infekce HBV (II-2, 1).
2. HBsAg pozitivní pacienti v PDL vyžadující léčbu by měli být léčeni ETV nebo TAF (II-2, 1).
3. Všichni HBsAg pozitivní příjemci ledviny by měli dostat ETV nebo TAF jako profylaxi nebo léčbu (II-2, 1).
4. HBsAg negativní a anti-HBc pozitivní příjemci ledviny by měli být po transplantaci monitorováni vzhledem k infekci HBV (III, 1).
Infekce HBV je dosud relativně častá mezi pacienty v PDL a u pacientů po TL je příčinou jejich signifikantní morbidity a mortality. Všichni tito pacienti by měli být testováni na přítomnost markerů infekce HBV, séronegativní osoby musí být vakcinovány preferovaně intenzifikovaným režimem vzhledem ke snížené imunitě. Všichni HBsAg pozitivní nemocní by měli být odesláni ke specialistovi, hepatologovi nebo infektologovi, k došetření a stanovení fáze infekce HBV.
Pouze monitorování je indikováno u pacientů v PDL s chronickou infekcí HBV bez známek chronické hepatitidy B. Toto doporučení platí i pro osoby HBsAg negativní, anti-HBc pozitivní. Naopak v případě HBeAg pozitivní nebo negativní chronické hepatitidy B je léčba NA nutná, a to nezávisle na transplantačním programu. U NA naivních pacientů je preferován ETV. TAF lze použít u NA naivních i již NA léčených/rezistentních nemocných. Redukce dávky ETV a TDF je nutná při eGFR < 50 ml/min, u TAF až < 15 ml/min. Protože dialýza snižuje aktivitu ALT, je třeba tento fakt zohlednit při indikacích léčby.
Po TL není možná léčba IFN-α (PEG nebo konvenčním) – hrozí rejekce štěpu. Vzhledem k nutnosti trvalé imununosuprese po TL musí každý HBsAg pozitivní pacient dostávat účinný NA. Podle výše iniciální viremie je podání NA profylaktické nebo terapeutické. ETV je preferovaným lékem pro naivní pacienty. TDF nemá být v této indikaci podáván vzhledem k potenciální nefrotoxicitě, pouze v případě rezistence k NA a nedostupnosti TAF. U NA naivních i již NA léčených/rezistentních nemocných lze pravděpodobně použít TAF, ale zatím není k dispozici dostatek údajů o bezpečnosti a účinnosti. Léčba LAM není indikována vzhledem k vysokému riziku vzniku rezistence. Profylaxe či léčba NA musí probíhat dlouhodobě, čímž se redukuje výskyt renálních komplikací a prodlužuje se přežívání. Renální funkce musí být pečlivě monitorovány během podávání NA. V případě neočekávaného zhoršení renálních funkcí je nutná změna dávkování nebo nahrazení léku jiným. Je nutná dobrá kompenzace arteriální hypertenze a diabetu u příjemců ledviny. HBsAg negativní, anti-HBc pozitivní příjemci ledviny nevyžadují profylaxi a obvykle ani léčbu. Je třeba monitorovat HBsAg, protože bylo popsáno několik případů séroreverze. Pokud k ní dojde, je nutné okamžité zahájení léčby ETV nebo TDF, bez ohledu na aktivitu ALT.
15.13 Pacienti s extrahepatálními projevy infekce HBV
1. Pacienti s replikací HBV a EHM by měli být léčeni NA (II-2, 1).
2. Pokud jsou přítomny EHM vzniklé na autoimunitním podkladě, je PEG-IFN kontraindikován (III, 1).
Antivirová léčba HBsAg pozitivních pacientů s aktivní replikací HBV a EHM může vést k poklesu závažnosti nebo úplnému vymizení mimojaterních projevů infekce, kterými jsou vaskulitida, kožní purpura, polyarteritis nodosa, artralgie, periferní neuropatie a glomerulonefritida. I když chybí kontrolované studie, řada kazuistik dokumentuje účinnost a bezpečnost léčby NA. PEG-IFN může zhoršit mimojaterní projevy, jejichž podkladem je autoimunitní mechanizmus, proto je v u těchto EHM kontraindikován.
V některých speciálních situacích může být účinná plazmaferéza, kortikosteroidy nebo jiná imunosupresivní léčba podávaná současně s NA.
16. Profylaxe reaktivace a rekurence infekce HBV
1. Před podáním chemoterapie nebo imunosupresivní léčby je vždy nutné testování přítomnosti markerů HBV (I, 1).
2. Všichni HBsAg pozitivní pacienti by měli dostat ETV, TDF nebo TAF jako léčbu nebo profylaxi (II-2, 1).
3. HBsAg negativní, anti-HBc pozitivní osoby by měly dostat anti-HBV profylaxi, pokud jsou ve vysokém riziku rekurence infekce HBV (II-2, 1).
Replikace HBV sama o sobě nevede k destrukci infikovaných hepatocytů, virus není ve většině případů cytopatogenní. Imunosupresivní léčba sice sníží imunitní reakci namířenou proti infikovaným hepatocytům, na druhou stranu oslabí imunitní kontrolu replikace viru. Zvyšuje se podíl infikovaných hepatocytů, replikace HBV výrazně stoupá a dosáhne úrovně, kdy již vede k přímému poškození infikovaných hepatocytů, a HBV se tím stává cytopatogenní. Klinickým korelátem popsaných pochodů je rozvoj fibrotizující cholestatické hepatitidy, což je závažné život ohrožující onemocnění, během několika týdnů vede bez účinné léčby u většiny případů k selhání jater. Stav, kdy imunosupresivní léčba vede k výraznému nárůstu replikace HBV a vzplanutí hepatitidy u dosud inaktivního nosiče HBsAg, se označuje jako reaktivace chronické hepatitidy B. Rekurencí se rozumí stav, kdy se pacient, který prodělal hepatitidu B a vymizel u něj HBsAg ze séra, stane znovu HBsAg pozitivním a replikace HBV rychle roste. Virová nukleová kyselina totiž perzistuje trvale v hepatocytech ve formě tzv. cccDNA, a to i u pacientů, kteří se stali HBsAg negativními. K úplné eliminaci HBV nikdy nedojde. Stav dříve nazývaný eliminací viru je jen účinnou imunitní kontrolou replikace s poklesem viremie pod hranici detekovatelnosti. Ztráta imunitní kontroly replikace viru vlivem imunosupresivní léčby tak vede k rekurenci hepatitidy B. Z uvedených důvodů je nezbytné, aby byl u všech pacientů před zahájením chemoterapie nebo imunosupresivní terapie proveden screening HBsAg, anti-HBs a anti-HBc. U séronegativních pacientů je indikována vakcinace. Vzhledem k tomu, že jde o pacienty imunosuprimované, je možno zvážit aplikaci vyšších dávek a více dávek běžných vakcín nebo vakcíny s vyšší účinností, ale v ČR je uvedená vakcinace schválena jen pro pacienty se selháním ledvin.
K reaktivaci replikace HBV dochází u 20–50 % inaktivních nosičů HBsAg podstupujících imunosupresivní či protinádorovou terapii. Reaktivace replikace HBV je častější, pokud chemoterapeutické režimy obsahují rituximab samostatně nebo v kombinaci s kortikosteroidy. Reaktivací hepatitidy B jsou ohroženi nejvíce pacienti s maligními lymfomy léčení rituximabem, ale i pacienti se solidními tumory, pacienti po transplantaci kostní dřeně, pacienti po orgánových transplantacích, dále pacienti s autoimunními chorobami léčení klasickými imunosupresivy a nově i anti-TNF a jinými typy biologické léčby. Reaktivace byla popsána i po transarteriální chemoembolizaci HCC. Reaktivace hepatitidy B obvykle přichází po 2–4 cyklech chemoterapie a klinický obraz kolísá od asymptomatického zvýšení aktivity aminotransferáz (50 %) k obrazu těžké akutní hepatitidy s ikterem (10 %), nejzávažnější variantou je fulminantní selhání jater (5 %).
V současné době je u pacientů HBsAg pozitivních preferována léčba preemptivní, která se zahajuje nejméně týden před chemoterapií nebo imunosupresí bez ohledu na výši hladiny HBV DNA v séru. U pacientů s nízkou vstupní viremií (HBV DNA v séru < 2 000 IU/ml) se doporučuje podávat protivirové léky ještě 12 měsíců po skončení imunosupresivní či protinádorové terapie (18 měsíců po skončení léčby rituximabem). Ukončení léčby je možné jen u pacientů, u kterých se nepředpokládá opakování chemoterapie. V opačném případě je nutná léčba celoživotní. Léčba pacientů s vysokou vstupní viremií (> 2 000 IU/ml) musí pokračovat až do dosažení stejných cílových kritérií jako u imunokompetentních pacientů. Pokud je k profylaxi použit LAM, zůstává u pacientů s nízkou viremií (< 2 000 IU/ml) reziduální riziko reaktivace infekce HBV kolem 10 %, u pacientů s vyšší viremií je toto riziko ještě významnější. Proto by měli mít přednost NA s vyšší účinností a vyšší genetickou bariérou pro vznik rezistence (ETV, TDF, TAF). Během profylaxe se kontrolují ALT a HBV DNA každých 3–6 měsíců a nejméně 12 měsíců po skončení profylaxe NA. K významné části reaktivací dochází až po vysazení NA.
U pacientů s pozitivitou anti-HBc protilátek a negativitou HBsAg je nezbytné před zahájením imunosuprese stanovit HBV DNA v séru. V případě pozitivity HBV DNA (okultní infekce HBV) je na místě stejný postup jako u HBsAg pozitivních osob.
U pacientů s vysokým nebezpečím rekurence infekce HBV (> 10 %), tj. při léčbě rituximabem, u příjemců kostní dřeně a kmenových buněk, je nutné okamžité zahájení profylaktického podávání NA i při negativitě HBV DNA v séru. Profylaxe musí trvat nejméně 18 měsíců po ukončení chemoterapie a monitorování pokračovat nejméně 12 měsíců po vysazení NA. Profylakticky lze použít LAM, i když několik případů vzniku rezistence na LAM je v literatuře dokumentováno. Proto je třeba v případě plánovaného dlouhodobého podávání vysoce účinné imunosupresivní terapie zvážit podání ETV, TDF nebo TAF.
U pacientů se středním (< 10 %) nebo nízkým (< 1 %) rizikem rekurence je nutné monitorování aktivity ALT a přítomnosti HBsAg a/nebo HBV DNA v séru v intervalu 1–3 měsíců podle typu imunosupresivní terapie a přítomnosti komorbidit. Hlavním virologickým projevem rekurence je znovuobjevení se HBsAg v séru (séroreverze) provázené konstantně exacerbací hepatitidy (flare). Naproti tomu opětovná pozitivita sérové HBV DNA je provázena séroreverzí a exacerbací hepatitidy jen asi v 1/2 případů. V případě rekurence infekce HBV, charakterizované detekovatelností sérové HBV DNA nebo séroreverzí HBsAg, je nezbytné okamžité zahájení léčby NA (ETV, TDF nebo TAF), a to nejlépe ještě před vzestupem aktivity ALT. Séroreverze HBsAg může vést k těžké, dokonce fatální, akutní hepatitidě.
17. Způsob dispenzarizace pacientů s infekcí HBV
V ČR je ze zákona nařízena povinná izolace nemocných s akutní hepatitidou na infekčních klinikách či odděleních. Dále jsou pacienti nejméně 12 měsíců kontrolováni v jaterních poradnách při těchto pracovištích. Pokud infekce přejde do chronicity, je nutná dlouhodobá, event. celoživotní dispenzarizace v jaterních poradnách infekčních, gastroenterologických nebo interních pracovišť. V případě vzniku HCC na gastroenterologii a onkologii. Oprávnění poskytovat antivirovou léčbu chronické hepatitidy B mají pouze pracoviště garantovaná ČHS a SIL ČLS JEP.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Datum schválení výborem SIL ČLS JEP: 21. 9. 2017. prof. MUDr. Petr Husa, CSc.
Klinika infekčních chorob
LF MU a FN Brno
Jihlavská 20
625 00 Brno
husa.petr@fnbrno.cz

Literatura
1. Husa P, Šperl J, Urbánek P et al. Doporučený postup diagnostiky a léčby chronické hepatitidy B. Gastroent Hepatol 2014; 68 (6): 514–526. doi: 10.14735/amgh2014 514.
2. Husa P, Šperl J, Urbánek P et al. Doporučený postup diagnostiky a léčby chronické hepatitidy B. Klin Mikrobiol Infekc Lek 2014; 20 (4): 121–132.
3. European Association for the Study of the Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection. J Hepatol 2017; 67 (2): 370–398. doi: 10.1016/j.hep.2017.03. 021.
4. Nemecek V, Castkova J, Fritz P et al. The 2001 serological survey in the Czech Republic – viral hepatitis. Cent Eur J Public Health 2003; 11 (Suppl): S54–S61.
5. Zdravotní ústav se sídlem v Ostravě, Zdravotní ústav se sídlem v Ústí nad Labem. Víceúčelový sérologický přehled (spalničky, příušnice, pertuse, virová hepatitida B) SP 2013, ČR. Závěrečná zpráva. CEM SZÚ 2014; 23 (Příloha 1): 1–152.
6. Státní zdravotní ústav. Infekce v ČR – EPIDAT. [online]. Dostupné z: www.szu.cz/publikace/data/infekce-v-cr.